Clear Sky Science · fr
Oxydoréductases métaboliques : régulateurs centraux des paysages épigénétiques de la pluripotence
Comment le carburant cellulaire façonne l’identité cellulaire
Toutes les cellules de votre corps portent essentiellement le même ADN, et pourtant les neurones, les cellules sanguines et les cellules de la peau se distinguent nettement par leur forme et leur fonction. Cet article explore un lien surprenant entre la façon dont les cellules traitent leur carburant et la manière dont elles décident du type cellulaire qu’elles deviendront. Il explique comment une famille d’enzymes, les oxydoréductases, qui gère normalement l’énergie et les nutriments, participe aussi à l’écriture et à l’effacement des marques chimiques sur l’ADN et les protéines qui contrôlent l’expression des gènes. Comprendre cette connexion pourrait modifier notre vision des cellules souches, du vieillissement et même du cancer.
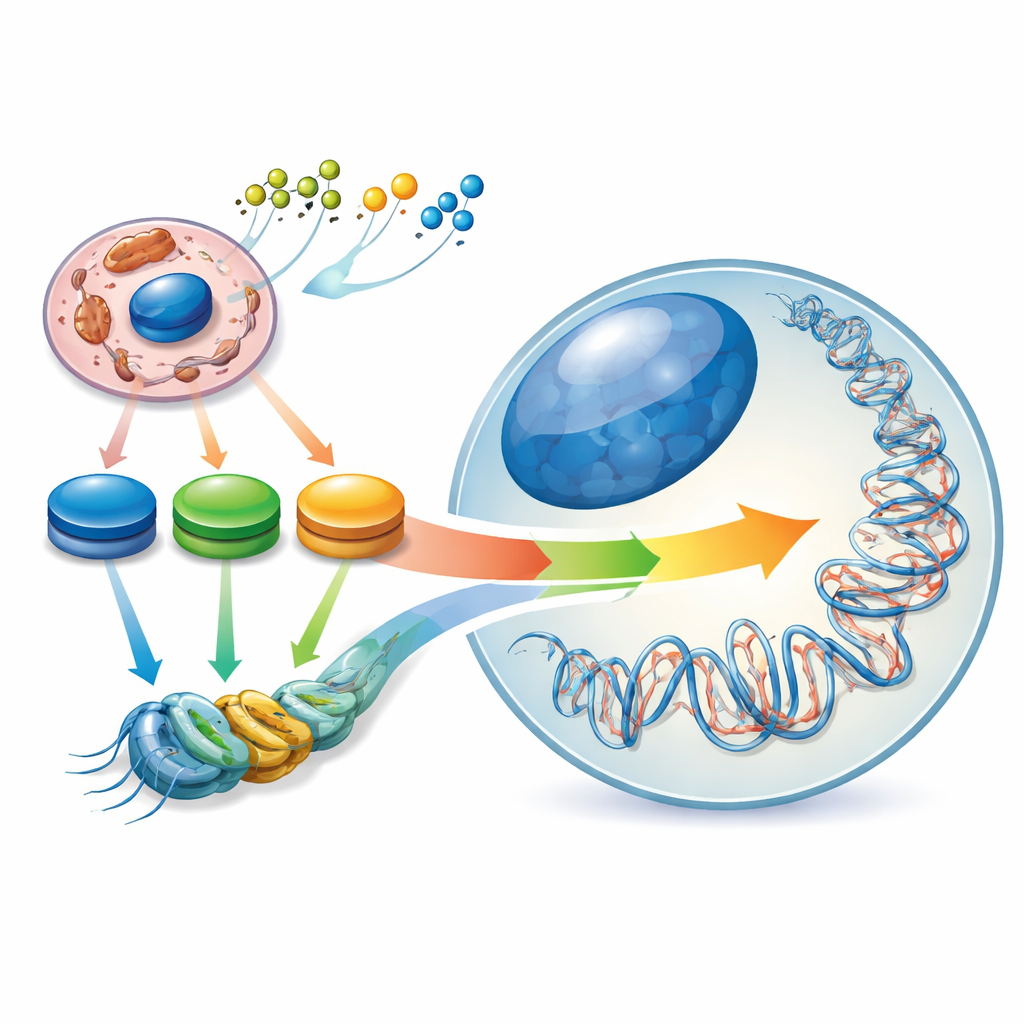
Le paysage caché à l’intérieur de nos gènes
Les cellules souches sont particulières parce qu’elles peuvent soit s’auto-renouveler, soit se différencier en de nombreux types cellulaires. Elles gèrent cet équilibre via un « paysage épigénétique » interne : des motifs d’étiquettes chimiques sur l’ADN et les protéines qui l’emballent, agissant comme des variateurs d’intensité pour les gènes. Les auteurs décrivent ce paysage comme modelé par un « contour énergétique » intracellulaire : des crêtes et des vallées dans les niveaux de molécules métaboliques clés telles que l’acétyl-CoA, le NAD⁺/NADH et l’α‑cétoglutarate. Lorsque la cellule souche passe d’un état naïf à un état plus engagé, son métabolisme central du carbone est reconfiguré, et le paysage épigénétique évolue avec lui. Ainsi, les changements dans l’utilisation du carburant cellulaire ne sont pas seulement des conséquences de l’identité cellulaire : ils contribuent activement à la déterminer.
Des enzymes qui transforment la nourriture en signaux épigénétiques
Les oxydoréductases catalysent des réactions d’oxydoréduction et occupent des carrefours métaboliques clés. Nombre d’entre elles génèrent des « métabolites épigénétiques », des molécules servant de matières premières ou de cofacteurs pour les enzymes qui marquent l’ADN et les histones. Par exemple, des déshydrogénases de la glycolyse et du cycle TCA produisent de l’acétyl‑CoA pour l’acétylation des histones, du NAD⁺/NADH et du NADPH qui influencent les déacétylases, et de l’α‑cétoglutarate qui alimente les déméthylases de l’ADN et des histones. En contrôlant la disponibilité de ces métabolites, les oxydoréductases définissent l’éventail des modifications épigénétiques possibles. Différents états des cellules souches reposent sur différents mélanges métaboliques : les cellules souches pluripotentes naïves puisent à la fois dans les sucres et les lipides, les cellules pluripotentes primées s’appuient fortement sur la glycolyse et la glutamine, et de nombreuses cellules souches adultes favorisent la β‑oxydation des acides gras et la phosphorylation oxydative.
Éditeurs directs de l’ADN, de l’ARN et des histones
Certaines oxydoréductases vont au‑delà de l’approvisionnement en précurseurs et réécrivent directement les marques épigénétiques. Des enzymes dépendantes du fer et de l’α‑cétoglutarate, comme les protéines TET et les déméthylases JMJD, retirent des groupes méthyle de l’ADN et des histones, remodelant l’activité génique. Des enzymes apparentées, ALKBH5 et FTO, effacent des marques méthyles sur l’ARN, influençant la durée de vie des messages et leur traduction. Un autre groupe, LSD1 et LSD2, utilise un cofacteur flavine pour déméthyler des lysines spécifiques des histones. Parce que toutes ces enzymes exigent des cofacteurs métaboliques et de l’oxygène, leur activité est extrêmement sensible à l’état énergétique et redox de la cellule. La revue montre comment des variations d’α‑cétoglutarate, de succinate ou la présence de métabolites mutants dans le cancer peuvent faire basculer l’équilibre entre une chromatine ouverte et flexible et des états réprimés fortement verrouillés.
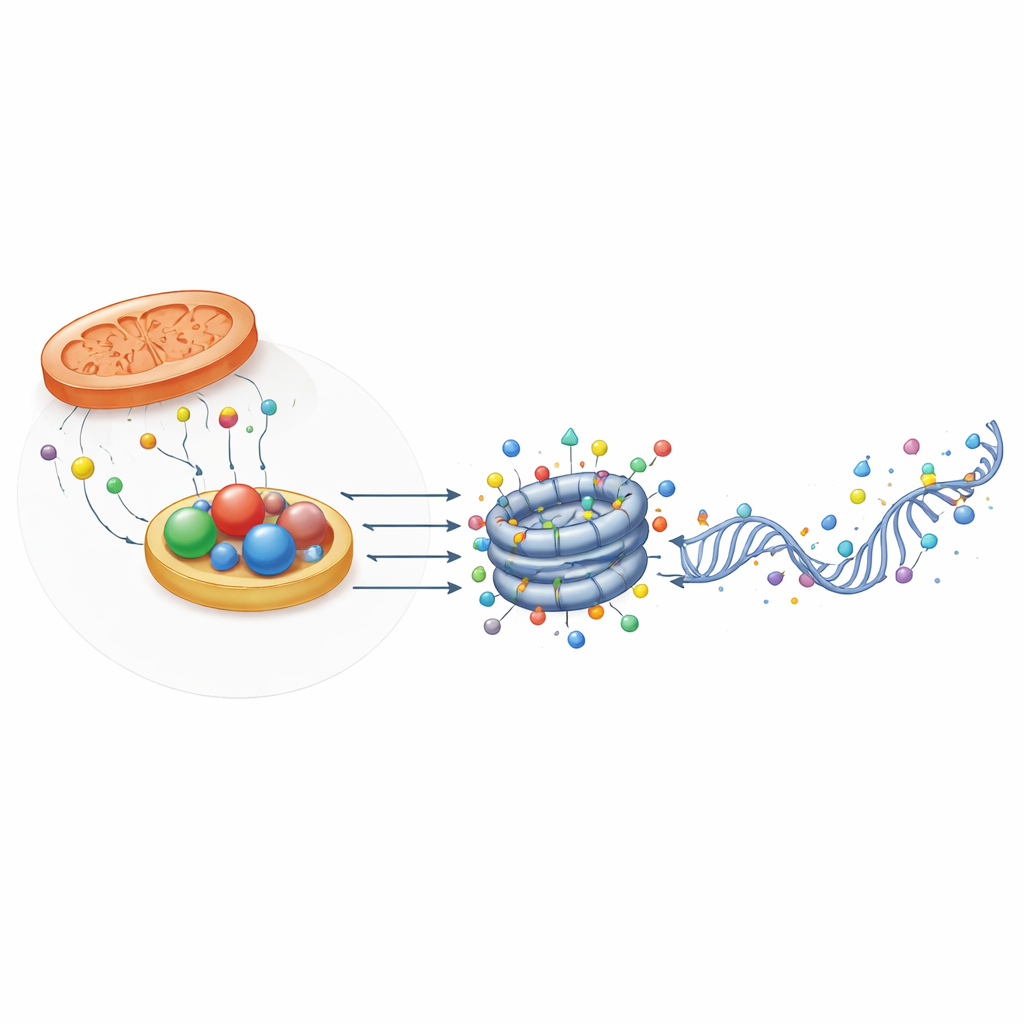
Aides structurales qui détectent l’état redox
De façon intrigante, tous les protéines liées aux oxydoréductases n’agissent pas comme des enzymes. Certaines, telles que CTBP et NPAC/GLYR1, conservent le repli structural qui lie le NADH mais présentent peu ou pas d’activité catalytique. Elles forment plutôt des échafaudages multiprotéiques qui rapprochent facteurs de transcription et modificateurs de la chromatine sur des régions géniques spécifiques. Leur assemblage dépend de la liaison au NAD(H), ce qui leur permet d’agir comme capteurs physiques de l’état redox cellulaire. Dans les cellules souches embryonnaires de souris, CTBP2 aide à préparer les gènes de pluripotence à l’extinction pendant la différenciation en recrutant des complexes qui retirent des marques acétyl et méthyle, tandis que NPAC/GLYR1 s’associe à LSD2 et à l’ARN polymérase II pour coordonner l’élongation transcriptionnelle et l’épissage alternatif. Ces rôles non enzymatiques ajoutent une couche supplémentaire par laquelle le métabolisme influence le contrôle des gènes.
Pourquoi cela compte pour la santé et la maladie
Les auteurs concluent que les oxydoréductases tissent ensemble métabolisme et régulation génique à trois niveaux : elles génèrent des métabolites clés, effacent directement des marques chimiques sur l’ADN, l’ARN et les histones, et servent d’échafaudages réorganisant la machinerie de la chromatine. Ensemble, ces fonctions transforment l’utilisation du carburant par une cellule en instructions durables sur les gènes à exprimer, contribuant à maintenir la pluripotence ou à promouvoir la différenciation. Ce cadre aide à expliquer pourquoi des mutations métaboliques peuvent reprogrammer des cellules vers des états proches du cancer, et pourquoi ajuster les nutriments ou les enzymes métaboliques peut modifier le comportement des cellules souches. À mesure que les chercheurs explorent ces liens plus en détail, les oxydoréductases apparaissent comme des cibles prometteuses pour des thérapies régénératives et des stratégies anticancéreuses visant à remodeler le paysage épigénétique en reconfigurant la gestion de l’énergie par la cellule.
Citation: Lee, HT., Roe, JS. & Youn, HD. Metabolic oxidoreductases: central regulators of the epigenetic landscapes in stemness. Exp Mol Med 58, 1017–1037 (2026). https://doi.org/10.1038/s12276-026-01687-2
Mots-clés: métabolisme des cellules souches, régulation épigénétique, enzymes oxydoréductases, remodelage de la chromatine, cellules souches cancéreuses