Clear Sky Science · sv
Simulationsbaserad inferens vid den teoretiska gränsen för snabb, robust mikrostukturell MRT med minimal diffusionsdata
Varför snabbare hjärnavbildning spelar roll
Magnetresonanstomografi (MRT) kan avslöja fina detaljer i hjärnvävnad, men de mest informativa undersökningarna är ofta långsamma och brusiga. Långa skanningstider är obekväma för patienter, svåra att planera på belastade sjukhus och nästan omöjliga för barn eller mycket sjuka personer. Denna studie ställer en enkel fråga med stora konsekvenser: kan vi använda smarta datorbaserade simuleringar och artificiell intelligens för att pressa ut samma rika information ur mycket kortare, rörigare diffusions-MRT-undersökningar, utan att offra tillförlitligheten?
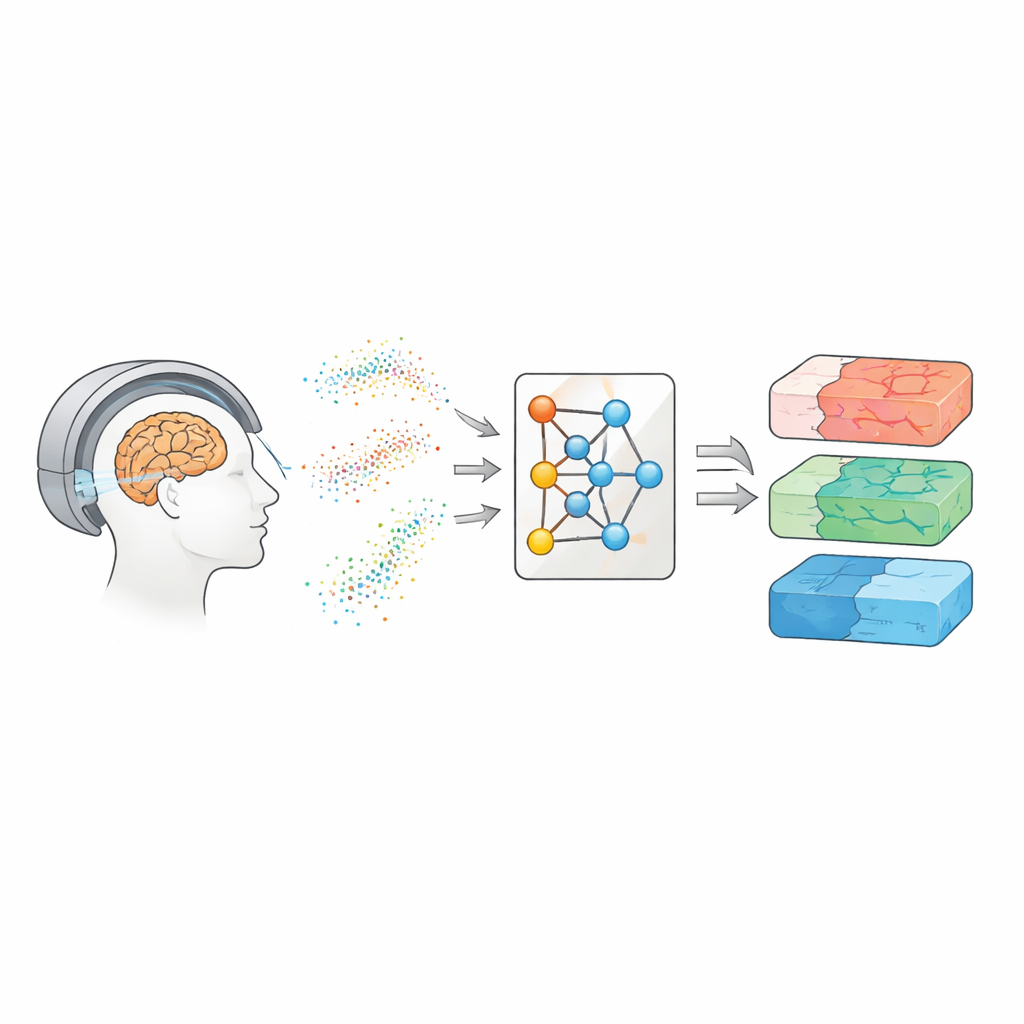
Att se in i hjärnan med rörligt vatten
Diffusions-MRT följer hur vattenmolekyler skuttar och vandrar genom hjärnvävnad. Eftersom vatten rör sig olika längs nervfibrer, genom cellkroppar eller runt skadade områden, kan dessa rörelsemönster fungera som ett fingeravtryck för hjärnans mikroskopiska struktur. Under årens lopp har forskare byggt flera modellfamiljer för att översätta diffusionssignaler till kartor över vävnadsegenskaper. Enklare metoder, som diffusions-tensoravbildning, sammanfattar hur lätt vatten rör sig och hur riktad den rörelsen är. Mer avancerade metoder, som diffusions-kurtosavbildning och biofysiska modeller som CHARMED och AxCaliber, försöker fånga detaljer som fibertäthet och till och med typiska axondiametrar. Dessa kartor skulle kunna fungera som ”virtuella biopsier” och ge ledtrådar om sjukdomar utan kirurgi — men de kräver vanligtvis många upprepade mätningar och långa skanningar.
Trögheten vid traditionell anpassning
Att omvandla råa diffusionsmätningar till meningsfulla kartor är ett matematiskt anpassningsproblem: modellens parametrar justeras tills den förutsagda signalen stämmer överens med vad skannern registrerade. De vanligaste verktygen idag, som icke-linjära minsta kvadratmetoder, gör detta genom att minimera kvadratsumman av skillnaderna mellan modell och data. Även om dessa metoder är enkla och allmänt tillgängliga, fungerar de bäst när det finns betydligt fler mätningar än strikt nödvändigt — det motsvarar att ta tio gånger fler foton för att vara på den säkra sidan. De har också problem när bruset är högt eller när startgissningar är dåliga, vilket är vanligt i kliniska data. Nyare statistiska angreppssätt kan hjälpa, men är ofta långsamma, känsliga för antaganden om brus och sällan använda utanför forskningsmiljöer.
Lära från simuleringar istället för patienter
Författarna tar en annan väg: istället för att lära direkt från patientskanningar utbildar de ett neuralt nätverk med helt simulerade data. De drar många möjliga kombinationer av modellparametrar, använder känd fysik för diffusion för att generera syntetiska signaler, lägger på realistiskt brus och tränar sedan en så kallad neural posterior-estimator. Detta nätverk lär sig att producera en full sannolikhetsfördelning över de parametrar som kan ha gett upphov till en given signal, vilket naturligt ger både en bästa gissning och en osäkerhetsuppskattning. För att göra metoden flexibel över olika skanningsinställningar matar teamet inte in råa mätningar. Istället komprimerar de varje signal till kompakta, fysikinformerade egenskaper som sammanfattar hur den varierar med gradientstyrka, riktning och diffusionstid. Dessa egenskaper fångar signalens kärna samtidigt som de förblir i stor utsträckning oberoende av exakt förvärvsprotokoll.
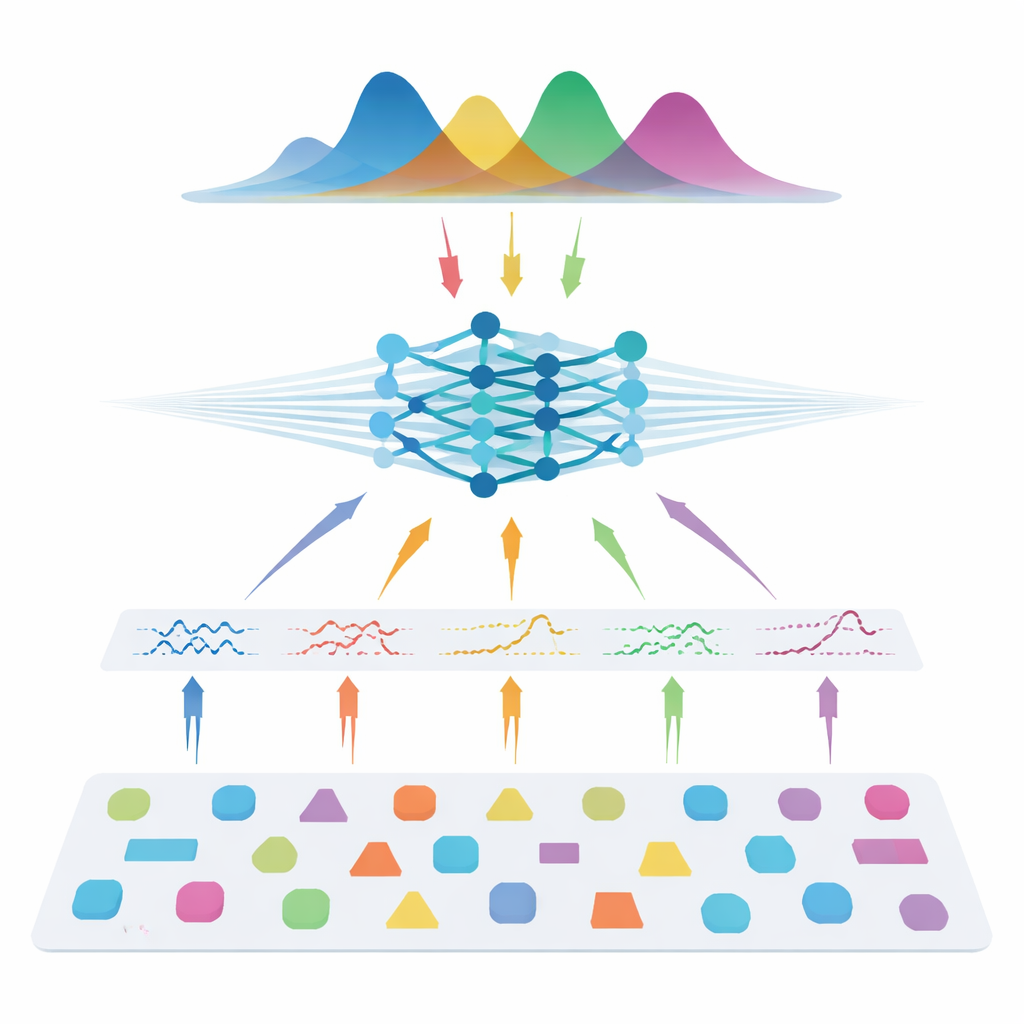
Matchar det bästa med en bråkdel av datan
När systemet väl är tränat testas det både på syntetiska data med känd ”jordspårning” och på flera människodatamängder, inklusive friska frivilliga och personer med multipel skleros. Över alla tre modellfamiljerna — diffusions-tensoravbildning, diffusions-kurtosavbildning och AxCaliber — återfår den simulationsbaserade metoden centrala mikrostukturella mått noggrant även när den använder så få som 7–22 mätningar istället för fullständiga protokoll med 69–271 mätningar. Det kan innebära upp till 90 % färre skanningar. Under brusiga förhållanden eller när antalet mätningar är kraftigt reducerat, överträffar den nya metoden konsekvent standardanpassning, och producerar renare kartor som bevarar viktig struktur. Den upptäcker också förväntade förändringar i multipel skleros-lesioner och återfinner kända mönster av axonstorlekar i hjärnbalken, vilket tyder på att den generaliserar väl till både frisk och sjuk vävnad.
Vad detta betyder för patienter och kliniker
För icke-specialister är slutsatsen att författarna visar hur man kan få i stort sett samma mikroskopiska bild av hjärnvävnad från mycket kortare och potentiellt sämre diffusions-MRT-undersökningar genom att i stor utsträckning förlita sig på simuleringar och avancerad inferens. Istället för att be skannern om mer data, ber de datorer att utnyttja mindre data bättre. Detta kan förkorta undersökningstider, utöka tillgången till avancerad avbildning i vanliga sjukhus och till och med rädda äldre studier som förvärvades med suboptimala inställningar. Eftersom metoden tränas uteslutande på simulerade signaler är den också integritetsvänlig och enklare att dela och skala upp. Om den antas i stor skala skulle denna typ av simulationsbaserad inferens kunna minska klyftan mellan spetsforskningsprotokoll och vardaglig klinisk MRT, och föra virtuella vävnadsbiopsier närmare standardvård.
Citering: Eggl, M.F., De Santis, S. Simulation-based inference at the theoretical limit for fast, robust microstructural MRI with minimal diffusion data. Commun Med 6, 275 (2026). https://doi.org/10.1038/s43856-026-01614-6
Nyckelord: diffusions-MRT, hjärnans mikrostuktur, simulationsbaserad inferens, neurala nätverk, kortare skanningstid