Clear Sky Science · pl
Wnioskowanie oparte na symulacjach na granicy teoretycznej dla szybkiego, odpornego obrazowania mikrostrukturalnego metodą MRI przy minimalnych danych dyfuzyjnych
Dlaczego szybsze skany mózgu mają znaczenie
Rezonans magnetyczny (MRI) może ujawnić drobne szczegóły tkanki mózgowej, ale najbardziej informacyjne badania często są wolne i zaszumione. Długie czasy skanowania są niewygodne dla pacjentów, trudne do zaplanowania w zatłoczonych szpitalach i niemal niemożliwe dla dzieci czy osób bardzo chorych. W badaniu postawiono proste pytanie o dalekosiężnych konsekwencjach: czy można użyć inteligentnych symulacji komputerowych i sztucznej inteligencji, by wydobyć tę samą bogatą informację z dużo krótszych, mniej dokładnych skanów MRI dyfuzyjnego, bez utraty wiarygodności?
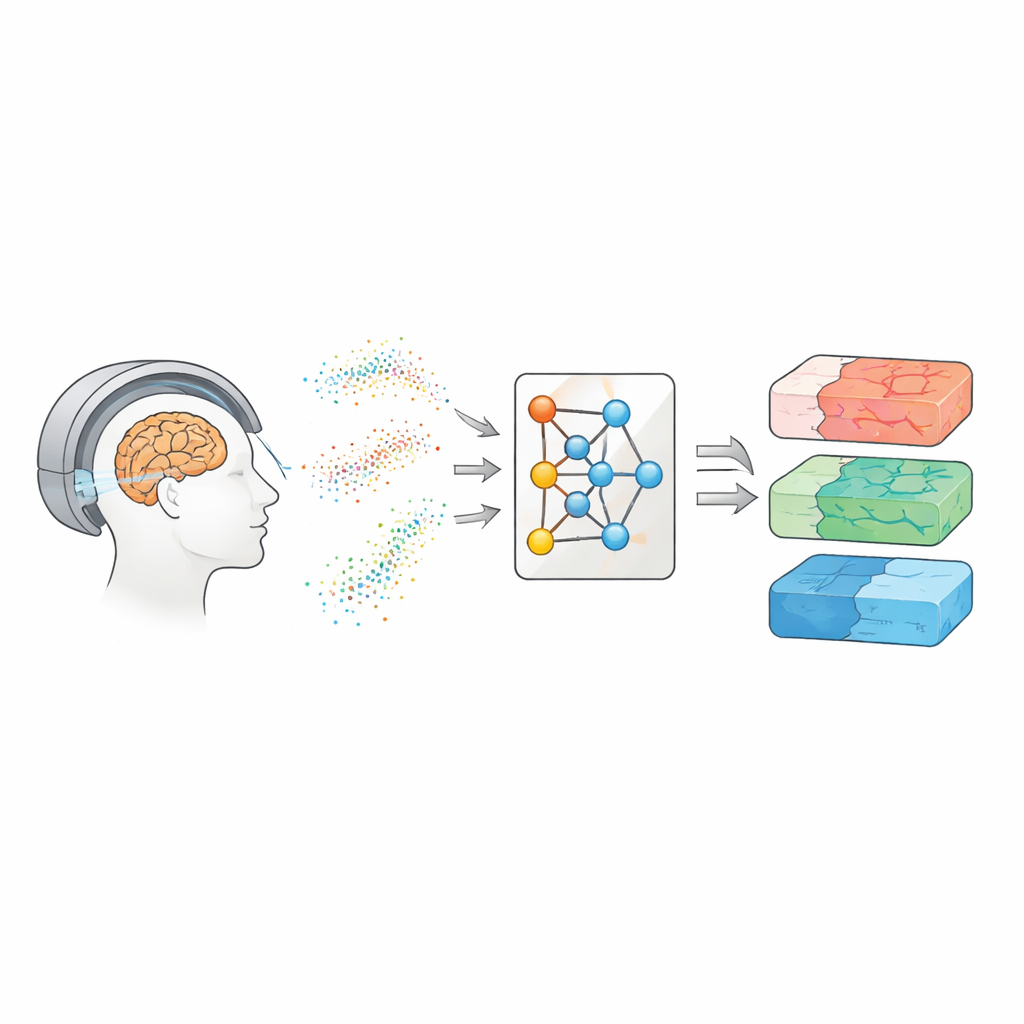
Zajrzeć do wnętrza mózgu za pomocą poruszającej się wody
MRI dyfuzyjne śledzi, jak cząsteczki wody trzęsą się i przemieszczają w tkance mózgowej. Ponieważ woda porusza się inaczej wzdłuż włókien nerwowych, przez ciała komórek lub wokół uszkodzonych obszarów, te wzorce mogą działać jak odcisk palca mikrostruktury mózgu. Na przestrzeni lat naukowcy stworzyli kilka rodzin modeli, które tłumaczą sygnały dyfuzyjne na mapy właściwości tkanki. Prostsze podejścia, takie jak obrazowanie tensora dyfuzji, podsumowują, jak łatwo porusza się woda i jak kierunkowy jest ten ruch. Bardziej zaawansowane metody, jak obrazowanie kurtosis dyfuzji czy modele biofizyczne typu CHARMED i AxCaliber, dążą do uchwycenia detali, takich jak gęstość włókien czy typowe średnice aksonów. Te mapy mogłyby służyć jako „wirtualne biopsje”, dostarczając wskazówek o chorobie bez operacji — ale zwykle wymagają wielu powtórzeń pomiarów i długich skanów.
Wąskie gardło tradycyjnego dopasowywania
Przekształcenie surowych pomiarów dyfuzyjnych w sensowne mapy to problem dopasowywania matematycznego: parametry modelu są dostosowywane, aż przewidziany sygnał zgadza się z tym, co zarejestrował skaner. Najczęściej stosowane narzędzia, jak nieliniowe metody najmniejszych kwadratów, robią to przez minimalizację kwadratu różnicy między modelem a danymi. Choć proste i powszechnie dostępne, metody te działają najlepiej, gdy jest o wiele więcej pomiarów niż absolutnie potrzebnych — to odpowiednik robienia dziesięciu razy więcej zdjęć „na wszelki wypadek”. Słabo radzą sobie też przy dużym szumie lub złych początkowych zgadach, co jest powszechne w danych klinicznych. Nowsze podejścia statystyczne mogą pomóc, ale często są wolne, wrażliwe na założenia dotyczące szumu i rzadko stosowane poza ośrodkami badawczymi.
Uczenie się z symulacji zamiast od pacjentów
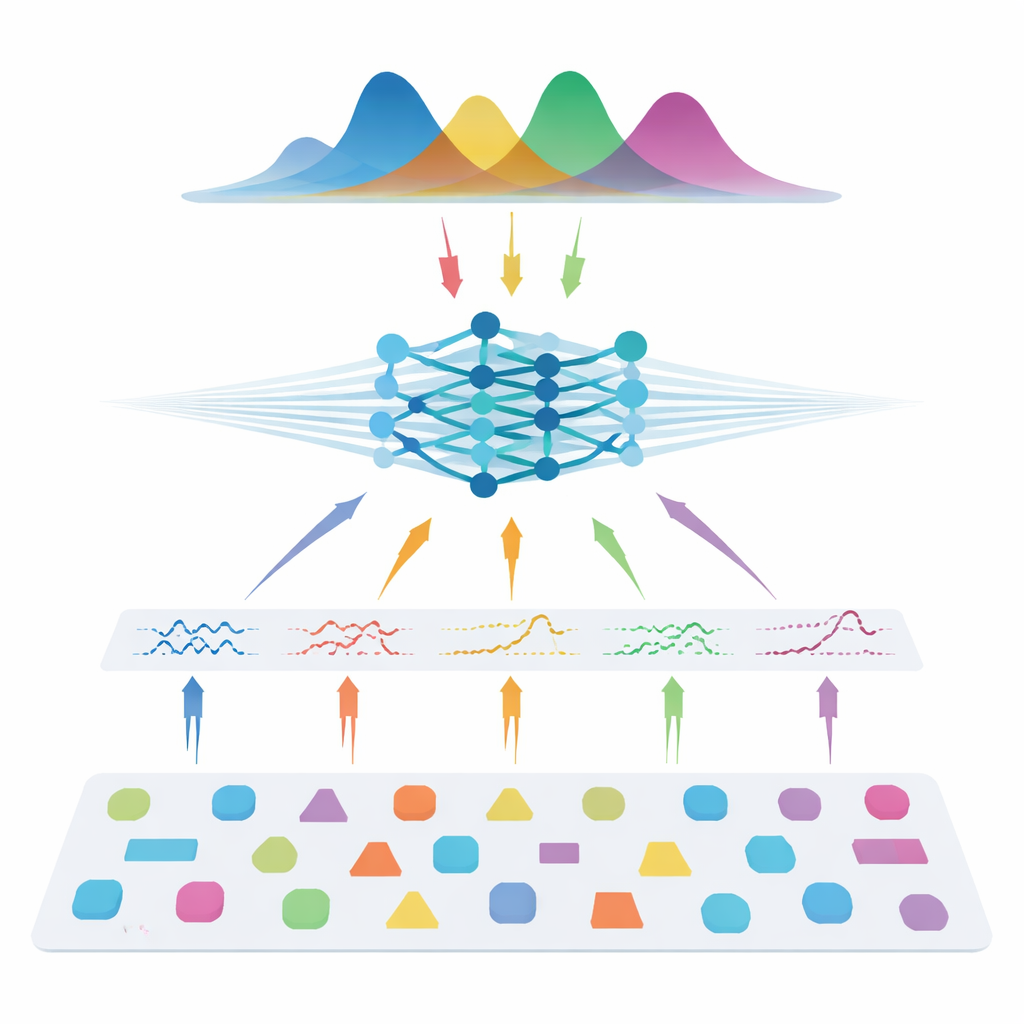
Autorzy wybierają inną drogę: zamiast uczyć się bezpośrednio z badań pacjentów, uczą sieć neuronową wyłącznie na danych symulowanych. Losują wiele możliwych kombinacji parametrów modelu, wykorzystują znaną fizykę dyfuzji do generowania syntetycznych sygnałów, dodają realistyczny szum, a następnie trenują tzw. estymator rozkładu posterior. Sieć uczy się wypisywać pełny rozkład prawdopodobieństwa parametrów, które mogły wygenerować dany sygnał, naturalnie dostarczając zarówno najlepsze oszacowanie, jak i miarę niepewności. Aby metoda była elastyczna wobec różnych ustawień skanera, zespół nie podaje sieci surowych pomiarów. Zamiast tego kompresują każdy sygnał do zwartej, inspirowanej fizyką reprezentacji cech, które podsumowują, jak sygnał zmienia się z siłą gradientu, kierunkiem i czasem dyfuzji. Te cechy chwytają istotę sygnału, pozostając w dużej mierze niezależne od dokładnego schematu akwizycji.
Równanie z najlepszymi przy ułamku danych
Po przeszkoleniu system testowano zarówno na danych syntetycznych ze znaną „prawdą”, jak i na kilku zestawach ludzkich danych, obejmujących ochotników zdrowych oraz osoby z stwardnieniem rozsianym. We wszystkich trzech rodzinach modeli — obrazowaniu tensora dyfuzji, obrazowaniu kurtosis dyfuzji i AxCaliber — podejście oparte na symulacjach odtwarza kluczowe metryki mikrostrukturalne dokładnie, nawet przy użyciu zaledwie 7–22 pomiarów zamiast pełnych protokołów z 69–271 pomiarami. To może oznaczać do 90% krótsze skany. W warunkach dużego szumu lub przy znacznym ograniczeniu liczby pomiarów nowa metoda konsekwentnie przewyższa standardowe dopasowywanie, generując czyściejsze mapy, które zachowują istotną strukturę. Wykrywa też oczekiwane zmiany wewnątrz zmian chorobowych stwardnienia rozsianego i odtwarza znane wzorce rozmiarów aksonów w obrębie spoidła wielkiego, co sugeruje dobrą generalizację zarówno do tkanki zdrowej, jak i chorobowej.
Co to oznacza dla pacjentów i klinik
Dla osób niezaznajomionych z tematem główna konkluzja jest taka, że autorzy pokazują, jak uzyskać niemal ten sam mikroskopijny obraz tkanki mózgowej z dużo krótszych i potencjalnie gorszej jakości skanów MRI dyfuzyjnego, mocno polegając na symulacjach i zaawansowanym wnioskowaniu. Zamiast prosić skaner o więcej danych, proszą komputery, by lepiej wykorzystały mniej danych. Może to skrócić czas badania, poszerzyć dostęp do zaawansowanego obrazowania w rutynowych szpitalach, a nawet uratować starsze badania wykonane w suboptymalnych warunkach. Ponieważ metoda jest trenowana wyłącznie na sygnałach symulowanych, jest też przyjazna dla prywatności i łatwiejsza do dzielenia oraz skalowania. Jeśli zyska szerokie zastosowanie, taki sposób wnioskowania opartego na symulacjach mógłby pomóc zniwelować przepaść między najnowocześniejszymi protokołami badawczymi a codziennym MRI klinicznym, przybliżając wirtualne biopsje tkanki do standardowej opieki.
Cytowanie: Eggl, M.F., De Santis, S. Simulation-based inference at the theoretical limit for fast, robust microstructural MRI with minimal diffusion data. Commun Med 6, 275 (2026). https://doi.org/10.1038/s43856-026-01614-6
Słowa kluczowe: MRI dyfuzyjne, mikrostruktura mózgu, wnioskowanie oparte na symulacjach, sieci neuronowe, skrócenie czasu skanu