Clear Sky Science · sv
Effekten av vävnadsdetektion på diagnostiska AI-algoritmer i prostatelektronisk patologi
Varför det första steget i cancer‑AI är viktigt
När sjukhus i allt större utsträckning använder artificiell intelligens för att hjälpa till att tolka prostatabiopsier, finns ett tyst men avgörande steg som ofta förbises: att helt enkelt hitta var vävnaden finns på en digital bild. Om detta första steg misslyckas och viktiga vävnadsområden förbises, kan även mycket avancerade canceridentifierande AI‑system ledas fel. Denna studie undersöker hur mycket detta grundläggande steg faktiskt påverkar den samlade prestandan och om moderna AI‑metoder kan upptäcka vävnad säkrare än äldre, regelbaserade metoder.
Från glaslammel till digital bild
I digital patologi skannas tunna skivor av prostatavävnad till högupplösta bilder. Innan någon cancergraderingsalgoritm kan börja arbeta måste systemet separera vävnad från tom bakgrund. Traditionellt görs detta med enkla regler baserade på färg och ljusstyrka, till exempel genom att sätta en tröskel för vilka pixlar som sannolikt är vävnad. Nyare system tränar istället AI‑modeller för att känna igen vävnadens former och mönster, på samma sätt som för mer komplexa uppgifter. Frågan är om denna uppgradering i ”rördragningsarbetet” faktiskt förbättrar cancergraderingen i verkliga kliniska miljöer, eller främst minskar sällsynta men allvarliga fel.
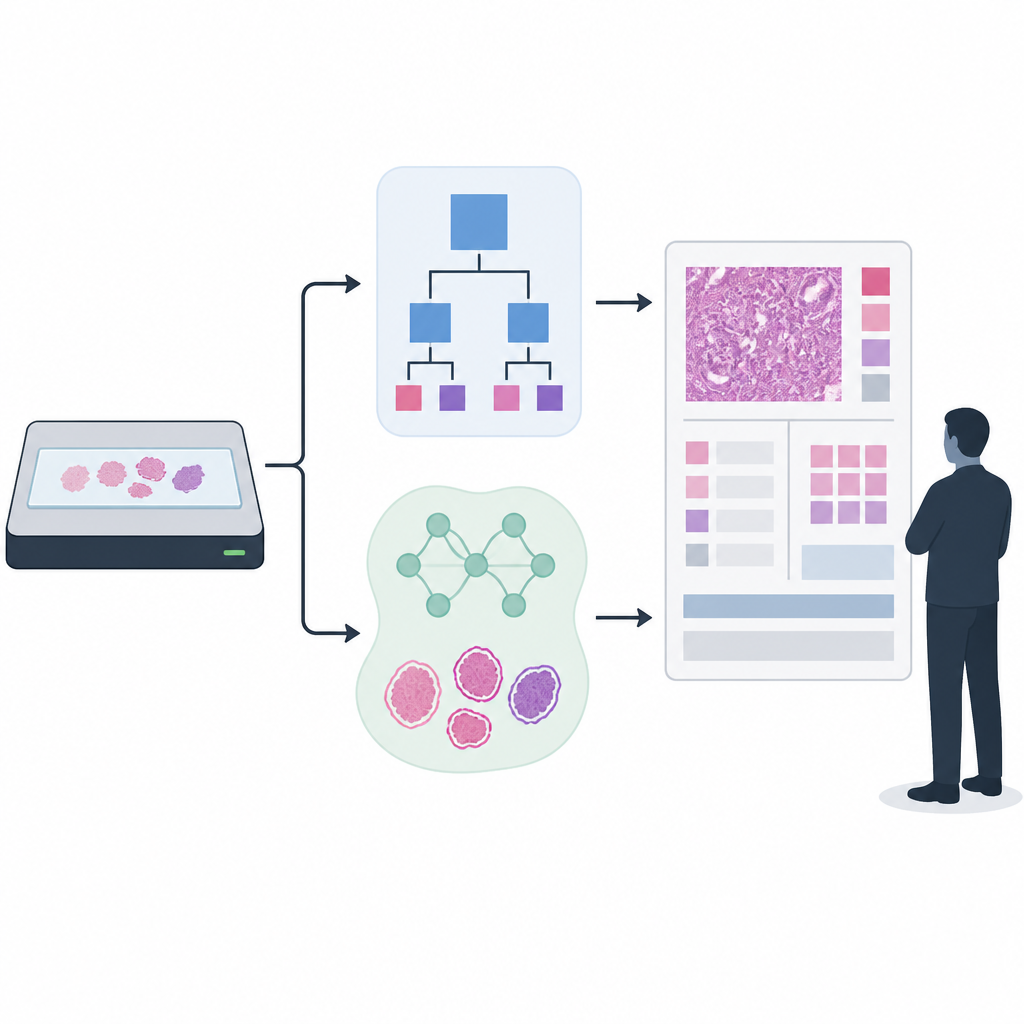
Bygga och testa två detektionsmetoder
Forskarnas fokus låg på prostatacancergraderingen, där biopsier tilldelas Gleason‑poäng och ISUP‑grader som styr behandlingsbeslut. De jämförde en länge använd regelbaserad vävnadsdetektor med en nyare AI‑modell byggd på ett UNet++‑segmenteringsnätverk. För att träna och utvärdera vävnadsdetektorn använde de mer än 33 000 skannade skivor från flera sjukhus och skannertyper, och kombinerade automatiskt genererade vävnadsomrissningar med mindre uppsättningar som noggrant kontrollerats och förbättrats av experter. För den efterföljande cancergraderingen användes en toppmodern AI som tränats på över 55 000 skivor och sedan testats över 13 kliniska platser med 13 olika skannrar, för att spegla den röriga mångfalden i verklig klinisk praxis.
Hur väl varje metod ser vävnaden
När de enbart tittade på hur exakt varje metod markerade vävnadspixlar presterade båda väl i genomsnitt. Den AI‑baserade detektorn fångade något mer verklig vävnad totalt sett, medan den klassiska metoden var något bättre på att undvika bakgrundsområden. Den avgörande skillnaden framträdde på sällsynta avvikande skivor med ovanligt utseende. I dessa svåra fall missade den regelbaserade metoden ibland stora vävnadsbitar helt, medan AI‑detektorn generellt bevarade mer av vävnaden. På över 27 000 utvärderingsskivor minskade antalet fullständiga fel — där ingen vävnad detekterades alls — från 118 med den klassiska metoden till 24 med den AI‑baserade detektorn, vilket tyder på att AI kan erbjuda en säkerhetsfördel genom att reducera katastrofala missar.
Förbättrar bättre vävnadsdetektion cancergraderingen?
Forskarna frågade sedan om dessa skillnader i vävnadskartor faktiskt förändrade de slutliga cancergrader som den efterföljande AI:n producerade. För att vara rättvisa analyserade de endast skivor där båda detektionsmetoderna hittade åtminstone viss vävnad, och jämförde överensstämmelsen mellan AI‑förutsagda grader och de som patologer tilldelat. På denna stora uppsättning skivor var den övergripande graderingsprestandan mycket likartad oavsett om systemet använde regelbaserad eller AI‑baserad vävnadsdetektion, med överlappande konfidensintervall över alla kliniska kohorter. Med andra ord, för typiska skivor begränsade inte det initiala detektionssteget tydligt noggrannheten hos en stark modern graderingsmodell, även när en äldre, enklare detektor användes.
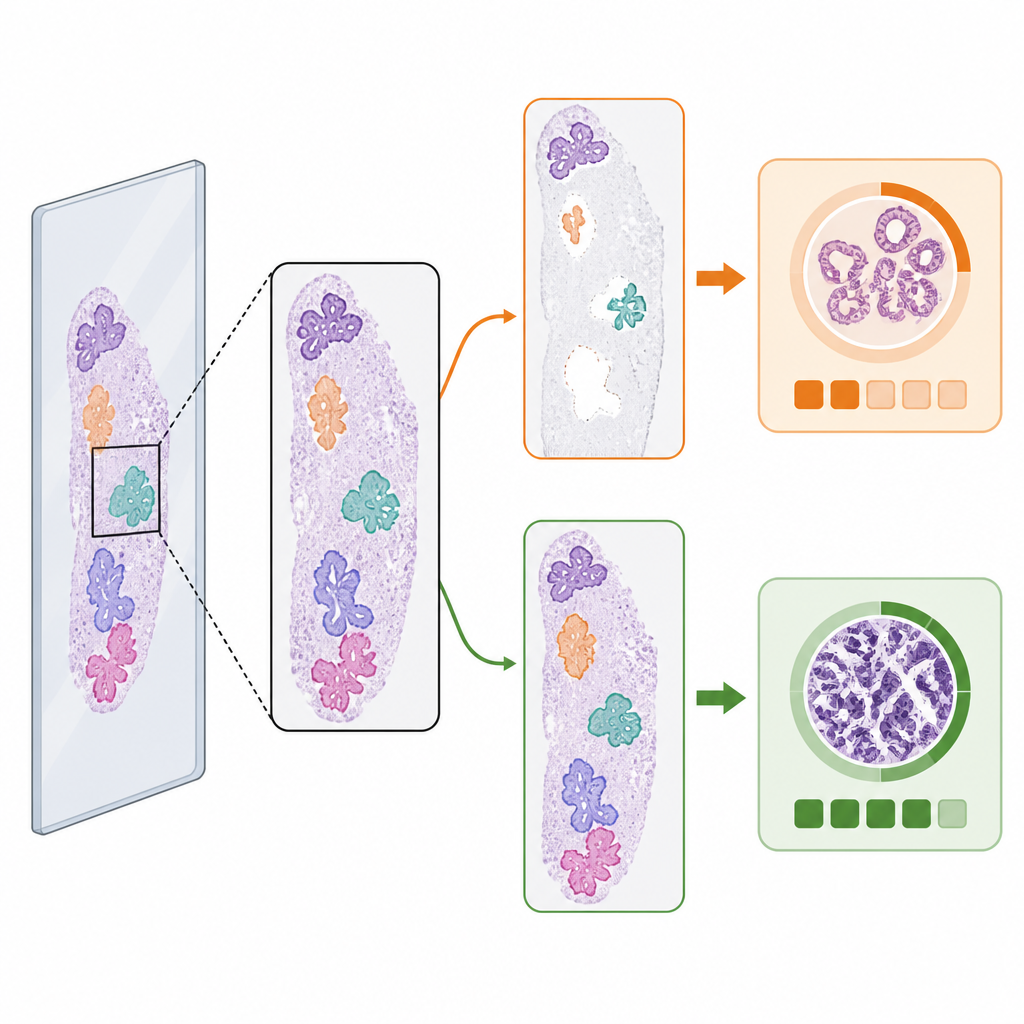
När första steget ändrar svaret
Trots liknande medelvärden påverkade valet av vävnadsdetektor den förutsagda cancergraden i en liten men viktig andel fall. Bland maligna skivor med per‑skiva referensgradering hade 3,5 procent olika ISUP‑gradsprediktioner beroende på vilken vävnadsdetektor som användes. I ungefär lika många av dessa ledde AI‑detektorn till rätt grad när den klassiska metoden inte gjorde det, och vice versa. Visuella exempel visade varför: om en detektor missade en stor bit tumörbärande vävnad eller felaktigt identifierade skräp som vävnad, kunde graderings‑AI:n drivas mot en lägre eller högre riskkategori. Dessa ”randfall” belyser hur subtila förändringar i vilka bildpatchar som når graderingsmodellen kan förändra dess slutliga beslut.
Vad detta betyder för framtidens cancer‑AI
För nu antyder studien att i högkvalitativa, flersajtiga dataset för prostatabiopsier förändrar inte den exakta metoden för vävnadsdetektion i hög grad den genomsnittliga noggrannheten hos avancerad AI‑baserad graderingsprogramvara. Däremot minskar AI‑baserad vävnadsdetektion tydligt andelen fullständiga fel och kan påverka resultaten i en liten delmängd av maligna fall där saknad vävnad kan vara mest skadlig. Författarna menar att vävnadsdetektion bör behandlas som en integrerad, granskbar del av diagnostiska AI‑system, med tydlig visualisering för patologer och fortsatt forskning i robusta, effektiva modeller i takt med att efterföljande AI:er blir ännu mer precisa.
Citering: Boman, S.E., Mulliqi, N., Blilie, A. et al. The impact of tissue detection on diagnostic artificial intelligence algorithms in prostate digital pathology. Sci Rep 16, 14968 (2026). https://doi.org/10.1038/s41598-026-52148-9
Nyckelord: digital patologi, prostatacancer, vävnadsdetektion, Gleason‑graderning, diagnostisk AI