Clear Sky Science · it
L'impatto del rilevamento del tessuto sugli algoritmi diagnostici di intelligenza artificiale nella patologia digitale della prostata
Perché il primo passaggio nell'AI per il cancro è importante
Con l'aumento dell'uso dell'intelligenza artificiale per leggere le biopsie prostatiche negli ospedali, un passaggio silenzioso ma cruciale spesso passa inosservato: individuare semplicemente dove si trova il tessuto su una lama digitale. Se questo primo passaggio fallisce e vengono trascurati pezzi importanti di tessuto, anche l'AI più sofisticata per rilevare il cancro può essere fuorviata. Questo studio si interroga su quanto conti davvero quel passaggio di base per le prestazioni complessive e se le moderne soluzioni AI possano fare un lavoro più sicuro rispetto ai metodi più vecchi basati su regole nel riconoscere il tessuto fin dall'inizio.
Dalla vetrino alla immagine digitale
Nella patologia digitale, sottili sezioni di tessuto prostatico vengono scansionate in immagini ad alta risoluzione. Prima che qualsiasi algoritmo di stadiazione del cancro possa operare, il sistema deve separare il tessuto dallo sfondo vuoto. Tradizionalmente ciò si ottiene con regole semplici basate sul colore e sulla luminosità, ad esempio impostando una soglia per decidere quali pixel siano probabilmente tessuto. I sistemi più recenti invece addestrano modelli AI a riconoscere forme e pattern di tessuto, come avviene per compiti più complessi. La domanda è se questo aggiornamento nella “tubatura” della pipeline migliori effettivamente la stadiazione del cancro nel mondo reale o riduca principalmente i rari ma gravi fallimenti.
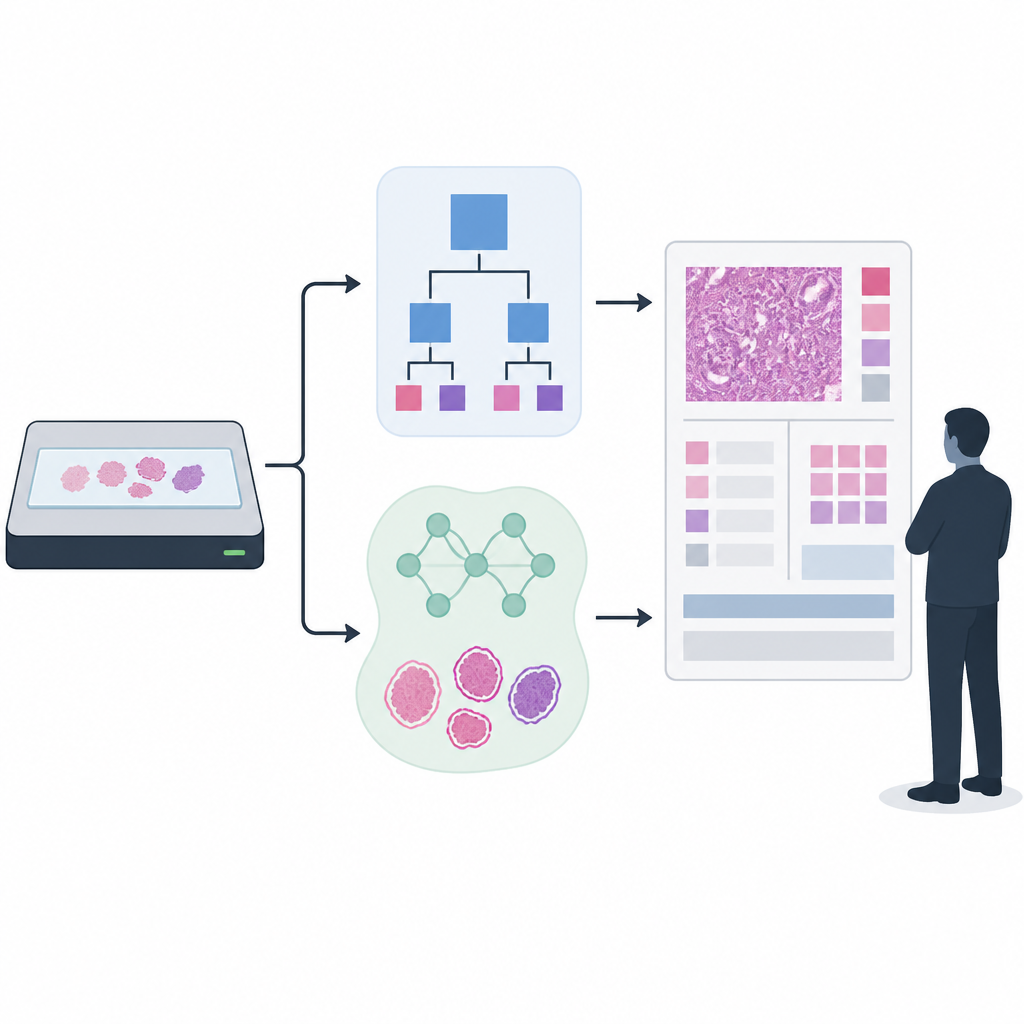
Costruire e testare due approcci di rilevamento
I ricercatori si sono concentrati sulla stadiazione del cancro prostatico, in cui alle biopsie vengono assegnati punteggi Gleason e gradi ISUP che guidano le decisioni terapeutiche. Hanno confrontato un rilevatore di tessuto basato su regole, di lunga data, con un modello AI più recente costruito su una rete di segmentazione UNet++. Per addestrare e valutare il rilevatore di tessuto hanno utilizzato oltre 33.000 vetrini scansionati provenienti da diversi ospedali e tipi di scanner, combinando contorni del tessuto generati automaticamente con insiemi più piccoli che erano stati accuratamente controllati e perfezionati da esperti. Per la stadiazione a valle hanno applicato un'AI all'avanguardia addestrata su più di 55.000 vetrini e poi testata in 13 siti clinici utilizzando 13 scanner diversi, rispecchiando la disomogeneità della pratica clinica reale.
Quanto bene ogni metodo vede il tessuto
Se analizzati solo in termini di accuratezza nel marcare i pixel di tessuto, entrambi i metodi hanno mostrato buone prestazioni in media. Il rilevatore basato su AI ha catturato leggermente più tessuto vero nel complesso, mentre il metodo classico è stato un po' migliore nell'evitare le aree di sfondo. La differenza cruciale è emersa nelle rare diapositive outlier con aspetto insolito. In questi casi difficili, il metodo basato su regole a volte ha mancato interi grandi frammenti di tessuto, mentre il rilevatore AI generalmente ne conservava una quantità maggiore. Su oltre 27.000 vetrini di valutazione, il numero di fallimenti completi in cui non è stato rilevato alcun tessuto è passato da 118 con il metodo classico a 24 con il rilevatore basato su AI, suggerendo che l'AI possa offrire un vantaggio di sicurezza riducendo omissioni catastrofiche.
Un migliore rilevamento del tessuto migliora la stadiazione del cancro?
Il team ha poi verificato se queste differenze nelle mappe di tessuto modificassero effettivamente i gradi finali prodotti dall'AI a valle. Per equità hanno analizzato solo i vetrini in cui entrambi i metodi di rilevamento avevano trovato almeno del tessuto e hanno confrontato l'accordo tra i gradi predetti dall'AI e quelli assegnati dai patologi. Su questo ampio insieme di vetrini, le prestazioni complessive di stadiazione sono state molto simili sia che il sistema usasse il rilevamento basato su regole sia quello AI, con intervalli di confidenza sovrapposti in tutte le coorti cliniche. In altre parole, per i vetrini tipici il passaggio iniziale di rilevamento non limitava in modo evidente l'accuratezza di un modello di stadiazione moderno e performante, anche quando si impiegava un rilevatore più semplice e datato.
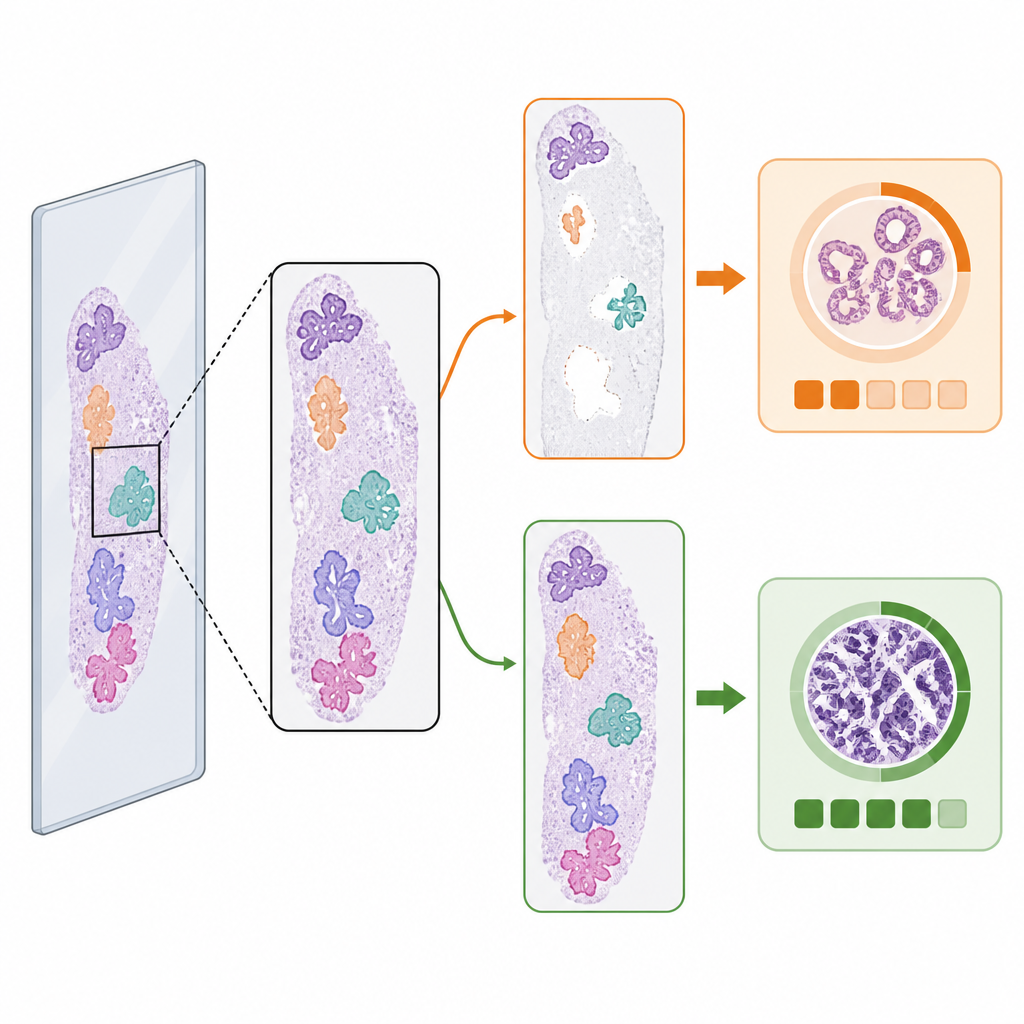
Quando il primo passaggio cambia la risposta
Nonostante le medie simili, la scelta del rilevatore di tessuto ha cambiato il grado di tumore predetto in una piccola ma importante frazione di casi. Tra i vetrini maligni con stadiazione di riferimento per vetrino, il 3,5 percento ha mostrato previsioni di grado ISUP diverse a seconda del rilevatore utilizzato. In numeri approssimativamente uguali, il rilevatore AI ha portato al grado corretto quando il metodo classico non l'ha fatto, e viceversa. Gli esempi visivi hanno mostrato il perché: se un rilevatore perdeva un'ampia porzione di tessuto contenente tumore o identificava erroneamente detriti come tessuto, l'AI di stadiazione poteva essere spinta verso una categoria di rischio più bassa o più alta. Questi “casi limite” evidenziano come cambiamenti sottili nelle porzioni di immagine che raggiungono il modello di stadiazione possano alterarne la decisione finale.
Cosa significa per l'AI oncologica futura
Per ora, lo studio suggerisce che in dataset di biopsie prostatiche di alta qualità e multi‑sito, il metodo esatto usato per il rilevamento del tessuto non modifica in modo marcato l'accuratezza media della stadiazione AI avanzata. Tuttavia, il rilevamento del tessuto basato su AI riduce chiaramente il tasso di fallimenti completi e può influenzare i risultati in un piccolo sottoinsieme di casi maligni, dove la perdita di tessuto potrebbe essere più dannosa. Gli autori sostengono che il rilevamento del tessuto debba essere trattato come una componente integrata e verificabile dei sistemi diagnostici AI, con visualizzazioni chiare per i patologi e ulteriore ricerca su modelli robusti ed efficienti man mano che le AI a valle diventano ancora più precise.
Citazione: Boman, S.E., Mulliqi, N., Blilie, A. et al. The impact of tissue detection on diagnostic artificial intelligence algorithms in prostate digital pathology. Sci Rep 16, 14968 (2026). https://doi.org/10.1038/s41598-026-52148-9
Parole chiave: patologia digitale, cancro alla prostata, rilevamento del tessuto, stadiazione Gleason, AI diagnostica