Clear Sky Science · nl
De impact van weefseldetectie op diagnostische AI-algoritmen in de digitale pathologie van de prostaat
Waarom de eerste stap in kanker-AI ertoe doet
Nu ziekenhuizen steeds vaker kunstmatige intelligentie inzetten om prostaatbiopsieën te beoordelen, is er een stille maar cruciale stap die vaak onopgemerkt blijft: simpelweg bepalen waar het weefsel op een digitale plakplaat zit. Als die eerste stap faalt en belangrijke weefselstukken worden gemist, kan zelfs de slimste kankerdetecterende AI op het verkeerde been worden gezet. Deze studie onderzoekt hoeveel die fundamentele stap werkelijk uitmaakt voor de algehele prestaties, en of moderne AI veiliger te werk kan gaan dan oudere, regelgebaseerde methoden bij het opsporen van weefsel.
Van glazen preparaat naar digitale afbeelding
In de digitale pathologie worden dunne plakjes prostaatweefsel ingescand tot hoge resolutie afbeeldingen. Voordat een tumorclassificatie-algoritme aan de slag kan, moet het systeem weefsel van lege achtergrond scheiden. Traditioneel gebeurt dat met eenvoudige regels op basis van kleur en helderheid, bijvoorbeeld door een drempel te kiezen om te bepalen welke pixels waarschijnlijk weefsel zijn. Nieuwere systemen trainen daarentegen AI-modellen om weefselvormen en -patronen te herkennen, zoals ze dat ook bij complexere taken doen. De vraag is of deze upgrade in de ‘leidingen’ van de pijplijn daadwerkelijk de klinische tumorklassificatie verbetert, of vooral zeldzame maar ernstige fouten terugdringt.
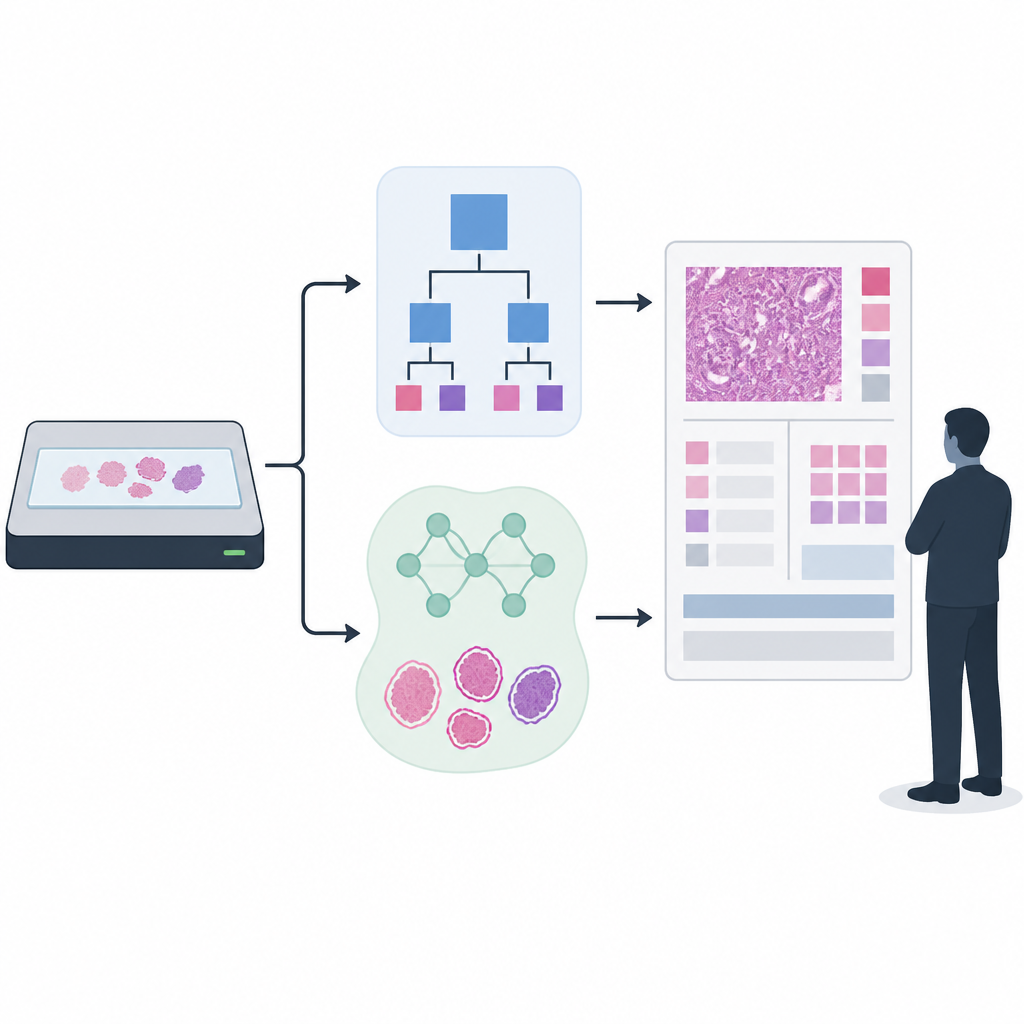
Opbouwen en testen van twee detectiebenaderingen
De onderzoekers richtten zich op prostaatkankerclassificatie, waarbij biopsieën Gleason-scores en ISUP-graden krijgen toegewezen die behandelbeslissingen sturen. Ze vergeleken een veelgebruikte regelgebaseerde weefseldetector met een nieuwere AI die was opgebouwd rond een UNet++-segmentatienetwerk. Om de detectoren te trainen en te evalueren gebruikten ze meer dan 33.000 ingescande slides van meerdere ziekenhuizen en scantypes, waarbij automatisch gegenereerde weefselcontouren werden gecombineerd met kleinere sets die door experts handmatig waren gecontroleerd en verfijnd. Voor de daaropvolgende tumorclassificatie pasten ze een state-of-the-art AI toe die op meer dan 55.000 slides was getraind en vervolgens getest werd over 13 klinische locaties met 13 verschillende scanners, wat de rommelige diversiteit van de klinische praktijk weerspiegelt.
Hoe goed ziet elke methode het weefsel
Wanneer ze alleen keken naar hoe nauwkeurig elke methode weefselpixels markeerde, presteerden beide gemiddeld goed. De AI-gebaseerde detector ving iets meer echt weefsel in het algemeen, terwijl de klassieke methode iets beter was in het vermijden van achtergrondgebieden. Het cruciale verschil verscheen bij zeldzame outlier-slides met een atypische verschijning. Bij die moeilijke gevallen miste de regelgebaseerde methode soms grote delen weefsel helemaal, terwijl de AI-detector doorgaans meer ervan behield. Over meer dan 27.000 evaluatieslides daalde het aantal volledige falen — waarbij helemaal geen weefsel werd gedetecteerd — van 118 met de klassieke methode naar 24 met de AI-detector, wat suggereert dat AI een veiligheidsvoordeel kan bieden door catastrofale missers te verminderen.
Leidt betere weefseldetectie tot betere kankerrapportage?
Het team vroeg zich vervolgens af of die verschillen in weefselskaarten inderdaad de uiteindelijke door de downstream-AI geproduceerde tumorgraden veranderden. Om eerlijk te vergelijken, analyseerden ze alleen slides waarop beide detectiemethoden ten minste enig weefsel vonden, en vergeleken ze de overeenstemming tussen AI-voorspelde gradaties en die van pathologen. Op deze grote set slides was de algehele classificatieprestatie zeer vergelijkbaar, ongeacht of het systeem regelgebaseerde of AI-weefseldetectie gebruikte, met overlappende betrouwbaarheidsintervallen in alle klinische cohorten. Met andere woorden: voor typische slides leek de initiële detectiestap de nauwkeurigheid van een sterk modern classificatiemodel niet duidelijk te limiteren, zelfs niet wanneer een oudere, eenvoudigere detector werd gebruikt.
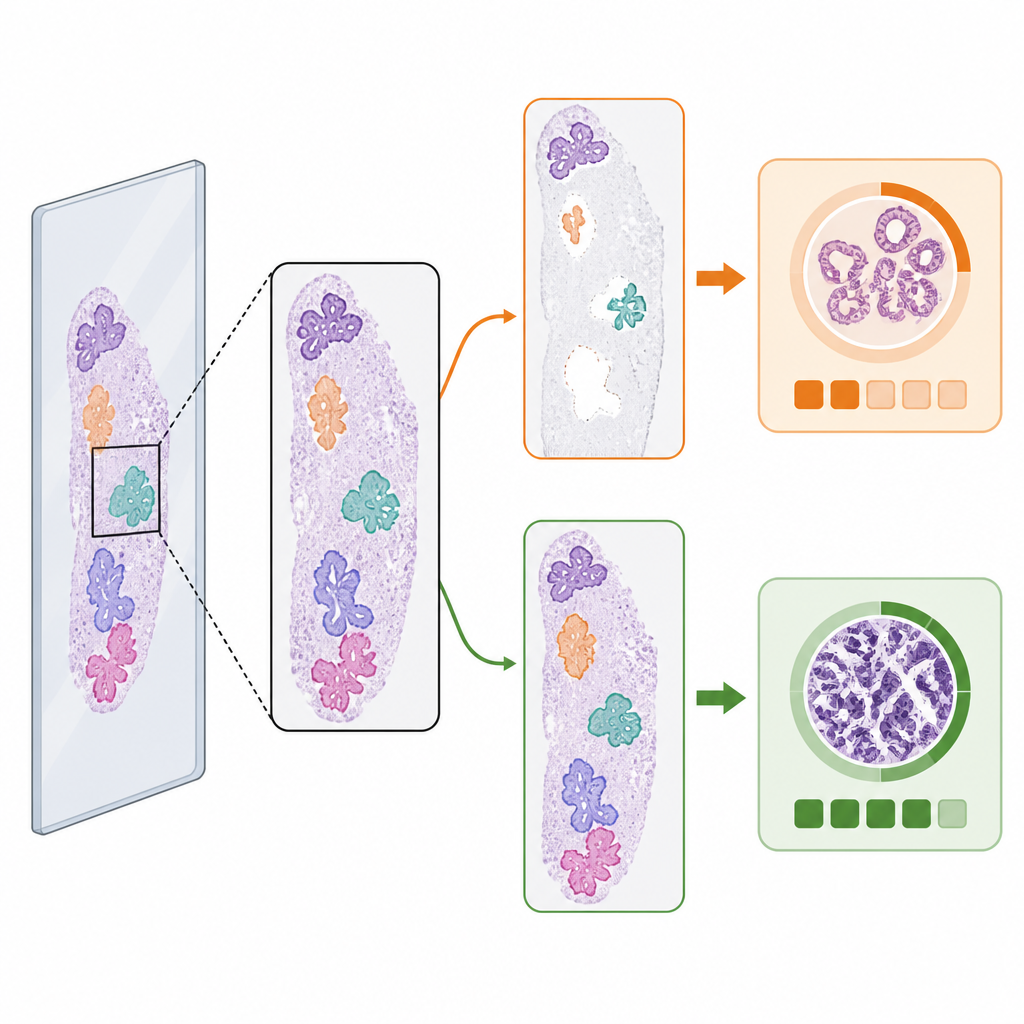
Wanneer de eerste stap het antwoord verandert
Ondanks de vergelijkbare gemiddelden veranderde de keuze van de weefseldetector de voorspelde tumorgraad in een klein maar belangrijk deel van de gevallen. Onder maligne slides met per-slide referentieclassificatie hadden 3,5 procent verschillende ISUP-voorspellingen afhankelijk van welke detector werd gebruikt. Ongeveer in gelijke aantallen leidde de AI-detector tot de juiste graad waar de klassieke methode dat niet deed, en andersom. Visuele voorbeelden lieten zien waarom: als een detector een groot stuk tumorhoudend weefsel miste of vuil/debris als weefsel foutief classificeerde, kon de classificatie-AI naar een lagere of hogere risicocategorie worden geduwd. Deze ‘randgevallen’ benadrukken hoe subtiele veranderingen in welke afbeeldingspatches de classificatiemodel bereiken de uiteindelijke beslissing kunnen beïnvloeden.
Wat dit betekent voor toekomstige kanker-AI
Voorlopig suggereert de studie dat in hoogwaardige, multisite prostaatbiopsiegegevens de exacte methode voor weefseldetectie de gemiddelde nauwkeurigheid van geavanceerde AI-classificatie niet sterk verandert. Toch verlaagt AI-weefseldetectie duidelijk het aandeel volledige falen en kan het de uitkomst beïnvloeden in een kleine subset van maligne gevallen, waar ontbrekend weefsel het meest schadelijk kan zijn. De auteurs stellen dat weefseldetectie moet worden behandeld als een integraal, controleerbaar onderdeel van diagnostische AI-systemen, met duidelijke visualisatie voor pathologen en voortgezet onderzoek naar robuuste, efficiënte modellen naarmate downstream-AI’s nog preciezer worden.
Bronvermelding: Boman, S.E., Mulliqi, N., Blilie, A. et al. The impact of tissue detection on diagnostic artificial intelligence algorithms in prostate digital pathology. Sci Rep 16, 14968 (2026). https://doi.org/10.1038/s41598-026-52148-9
Trefwoorden: digitale pathologie, prostaatkanker, weefseldetectie, Gleason-classificatie, diagnostische AI