Clear Sky Science · he
השפעת גילוי רקמות על אלגוריתמים של בינה מלאכותית לאבחון בפתולוגיה דיגיטלית של הערמונית
מדוע הצעד הראשון ב-AI לסרטן חשוב
כשבתי חולים משתמשים יותר ויותר בבינה מלאכותית לסיוע בקריאת ביופסיות של הערמונית, צעד שקט אך קריטי לעיתים קרובות אינו זוכה לתשומת לב: פשוט למצוא היכן הרקמה נמצאת על השקופית הדיגיטלית. אם הצעד הראשון הזה נכשל וחלקים חשובים של רקמה נשכחים, אפילו ה-AI החכם ביותר לגילוי סרטן עלול להטעות. המחקר הזה שואל עד כמה אותו צעד בסיסי משפיע באמת על הביצועים הכוללים, והאם מערכות מודרניות מבוססות AI יכולות לזהות רקמות בצורה בטוחה יותר מאשר שיטות מבוססות-חוקים ישנות.
משקופית זכוכית לתמונה דיגיטלית
בפתולוגיה דיגיטלית, פרוסות דקות של רקמת הערמונית נסרקות לתמונות ברזולוציה גבוהה. לפני שכל אלגוריתם לדירוג סרטן יכול להתחיל בעבודתו, המערכת חייבת להפריד בין רקמה לרקע ריק. באופן מסורתי הדבר נעשה בכללים פשוטים המבוססים על צבע ובהירות, כמו קביעת סף להחלטה אילו פיקסלים סבירים להיות רקמה. מערכות חדשות יותר מאמנות במקום זאת מודלים של בינה מלאכותית לזהות צורות ודפוסים של רקמה, בדומה למשימות מורכבות יותר. השאלה היא האם השדרוג הזה ב"תשתית" של הצינור אכן משפר דירוג סרטן בעולם האמיתי, או בעיקר מקטין כשלים נדירים אך חמורים.
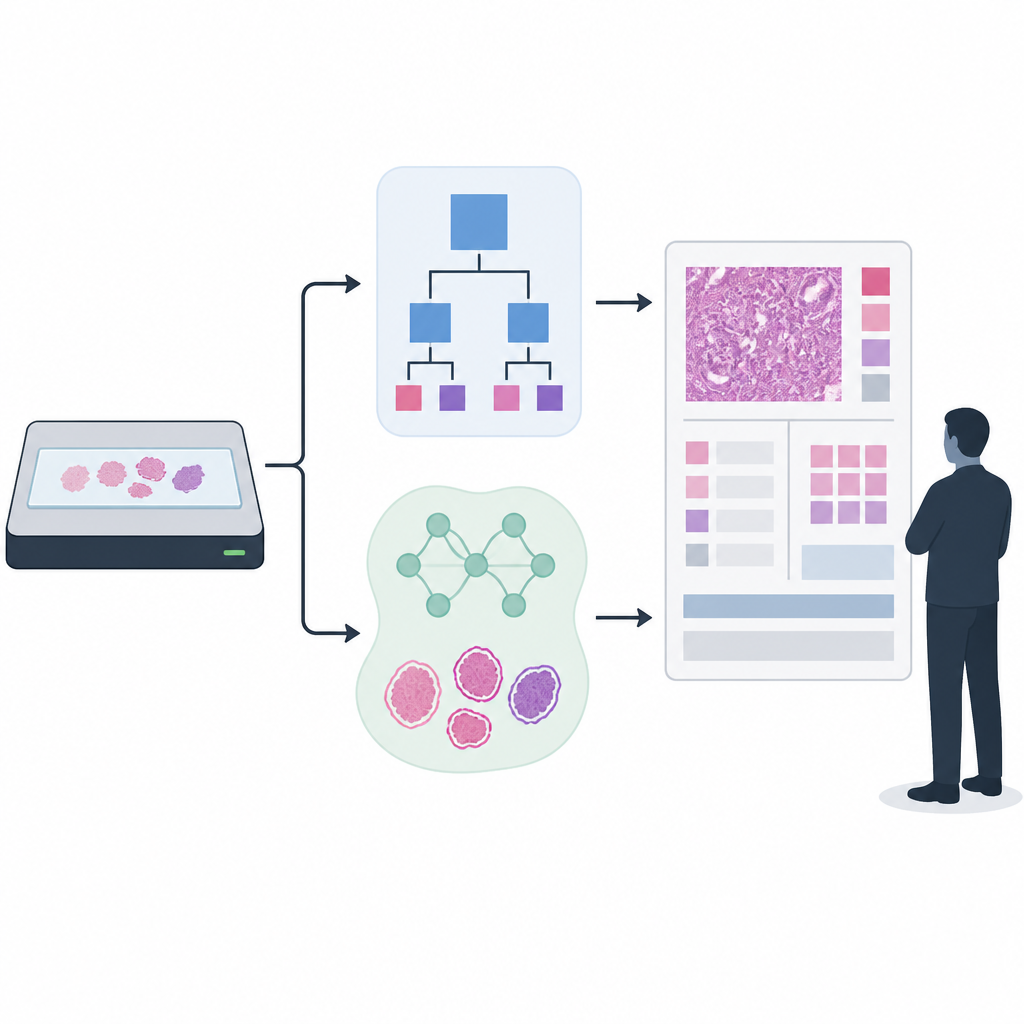
בניית ובחינת שתי גישות גילוי
חוקרי המאמר התמקדו בדירוג סרטן הערמונית, שבו ביופסיות מקבלות ציוני גליסון ודירוגי ISUP שמנחים החלטות טיפוליות. הם השוו גלאי רקמות מבוסס-חוקים שהשתמשו בו זמן רב עם מודל AI חדש יותר שבנוי על רשת סגמנטציה UNet++. לאימון והערכת גלאי הרקמות השתמשו ביותר מ-33,000 שקופיות נסרקות ממספר בתי חולים וסוגי סורקים, ושילבו מתארי רקמה שנוצרו אוטומטית עם קבוצות קטנות יותר שנבדקו ושופרו במאמץ ידני על ידי מומחים. לדירוג הסרטן בהמשך, יישמו AI עכשווי שאומן על יותר מ-55,000 שקופיות ונבדק ב-13 אתרים קליניים באמצעות 13 סורקים שונים, כדי לשקף את הגיוון הבלתי אסתטי של הפרקטיקה הקלינית האמיתית.
כמה טוב כל שיטה רואה את הרקמה
כאשר בדקו רק עד כמה כל שיטה סומנה במדויק פיקסלי רקמה, שתיהן הופיעו היטב בממוצע. הגלאי מבוסס ה-AI תפס מעט יותר רקמה אמיתית בסך הכל, בעוד שהשיטה הקלאסית היתה מעט טובה יותר במניעת זיהוי אזורים שלרקע. ההבדל הקריטי הופיע בשקופיות מיעוט חורגות בעלות הופעה בלתי שגרתית. במקרים קשים אלה, השיטה מבוססת-החוקים לפעמים פספסה חלקים גדולים של רקמה לחלוטין, בעוד שהגלאי ה-AI בדרך כלל שמר על מרבם. על פני יותר מ-27,000 שקופיות הערכה, מספר הכשלונות המוחלטים שבהם לא נתגלתה כלל רקמה ירד מ-118 בשיטה הקלאסית ל-24 עם הגלאי המבוסס AI, מה שמרמז ש-AI עשוי להציע יתרון בטיחותי על ידי הפחתת החסרות קטסטרופליות.
האם גילוי רקמות טוב יותר משפר דירוג סרטן?
הקבוצה שאלת האם ההבדלים במפות הרקמה אכן שינו את ציוני הסרטן הסופיים שייצר ה-AI בהמשך. מטעמי הוגנות הם מנתחו רק שקופיות שבהן שתי שיטות גילוי הרקמות מצאו לפחות חלק מהותי של רקמה, והשוו את ההסכמה בין הדירוגים שחזו ה-AI ואת אלה שהוקצו על ידי פתולוגים. בקבוצת השקופיות הגדולה הזו, ביצועי הדירוג הכוללים היו דומים מאוד בין השימוש בגילוי מבוסס-חוקים ובשימוש בגילוי מבוסס-AI, עם מרווחי ביטחון חופפים בכל הקוהורטים הקליניים. במילים אחרות, עבור שקופיות טיפוסיות, שלב הזיהוי ההתחלתי לא הגביל באופן ברור את הדיוק של מודל דירוג מודרני חזק, אפילו כאשר נעשה שימוש בגלאי ישן ופשוט יותר.
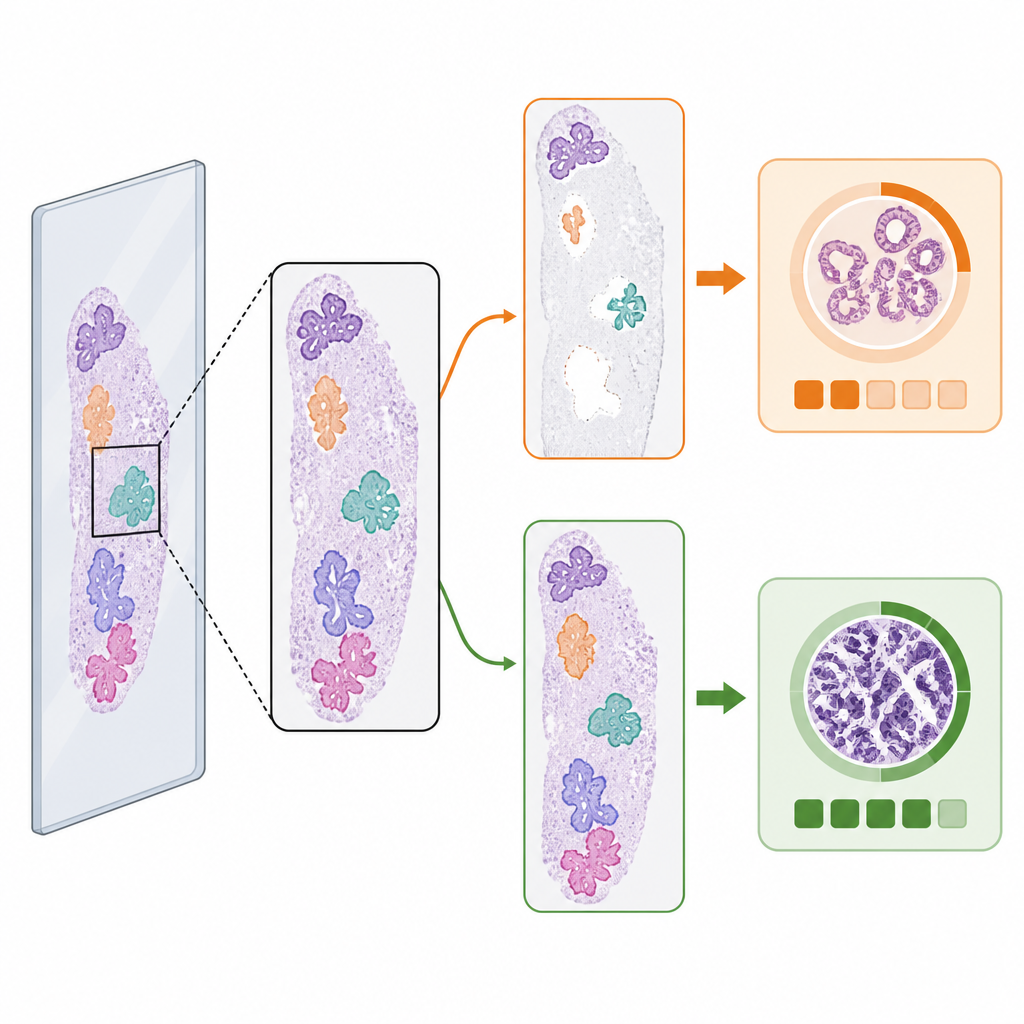
מתי הצעד הראשון משנה את התוצאה
למרות הממוצעים הדומים, בחירת גלאי הרקמות שינתה את דירוג הסרטן החזוי בחלק קטן אך חשוב מהמקרים. בקרב שקופיות ממאירות עם דירוג ייחוס לכל שקופית, ב-3.5 אחוזים היו תחזיות דירוג ISUP שונות בהתאם לאיזה גלאי רקמות שימשו. במספרים הקרובים זה לזה במקרים אלה, הגלאי המבוסס AI הוביל לדירוג הנכון כאשר השיטה הקלאסית לא עשתה זאת, ולהיפך. דוגמאות ויזואליות הראו מדוע: אם גלאי אחד פספס חתיכה גדולה של רקמת גידול או זיהה פסולת בטעות כרקמה, אלגוריתם הדירוג יכול להיות נדחף לקטגוריית סיכון נמוכה או גבוהה יותר. "מקרי קצה" אלה מדגישים כיצד שינויים עדינים באילו חתיכות תמונה מגיעות למודל הדירוג יכולים לשנות את החלטתו הסופית.
מה זה אומר עבור עתיד ה-AI לסרטן
כיום המחקר מציע שבמאגרי ביופסיות ערמונית איכותיים ורב-אתריים, השיטה המדויקת שבה משתמשים לגילוי רקמות אינה משנה באופן חזק את הדיוק הממוצע של דירוג מתקדם מבוסס-AI. עם זאת, גילוי רקמות מבוסס- AI מקטין בבירור את שיעור הכשלים המוחלטים ויכול להשפיע על תוצאות בחלק קטן ממקרי הממאירות, שבהם החסרת רקמה עלולה להיות המזיקה ביותר. המחברים טוענים שגילוי הרקמות צריך להיחשב כחלק אינטגראלי ובר-בדיקה של מערכות AI לאבחון, עם ויזואליזציה ברורה עבור פתולוגים ומחקר מתמשך במודלים חסינים ויעילים ככל שה-AI היסודי ימשיך להיות מדויק יותר.
ציטוט: Boman, S.E., Mulliqi, N., Blilie, A. et al. The impact of tissue detection on diagnostic artificial intelligence algorithms in prostate digital pathology. Sci Rep 16, 14968 (2026). https://doi.org/10.1038/s41598-026-52148-9
מילות מפתח: פתולוגיה דיגיטלית, סרטן הערמונית, גילוי רקמות, דירוג גליסון, בינת אבחון