Clear Sky Science · es
El impacto de la detección de tejido en los algoritmos de inteligencia artificial diagnóstica en la patología digital de la próstata
Por qué importa el primer paso en la IA para el cáncer
A medida que los hospitales usan cada vez más la inteligencia artificial para ayudar a interpretar biopsias de próstata, hay un paso silencioso pero crucial que a menudo pasa desapercibido: localizar dónde está el tejido en una lámina digital. Si ese primer paso falla y se pasan por alto fragmentos importantes de tejido, incluso la IA más avanzada para detectar cáncer puede desviarse. Este estudio pregunta cuánto influye realmente ese paso básico en el rendimiento global y si la IA moderna puede hacer un trabajo más seguro que los métodos antiguos basados en reglas a la hora de detectar tejido.
De la lámina de vidrio a la imagen digital
En la patología digital, se escanean en imágenes de alta resolución finas secciones de tejido prostático. Antes de que cualquier algoritmo de gradado pueda comenzar a trabajar, el sistema debe separar el tejido del fondo vacío. Tradicionalmente, esto se hace con reglas simples basadas en color y brillo, por ejemplo fijando un umbral para decidir qué píxeles son probablemente tejido. Los sistemas más nuevos, en cambio, entrenan modelos de IA para reconocer formas y patrones de tejido, de forma similar a como se aplican en tareas más complejas. La cuestión es si esta mejora en la “plomería” del flujo de trabajo mejora realmente el gradado del cáncer en la práctica clínica o si principalmente reduce fallos raros pero graves.
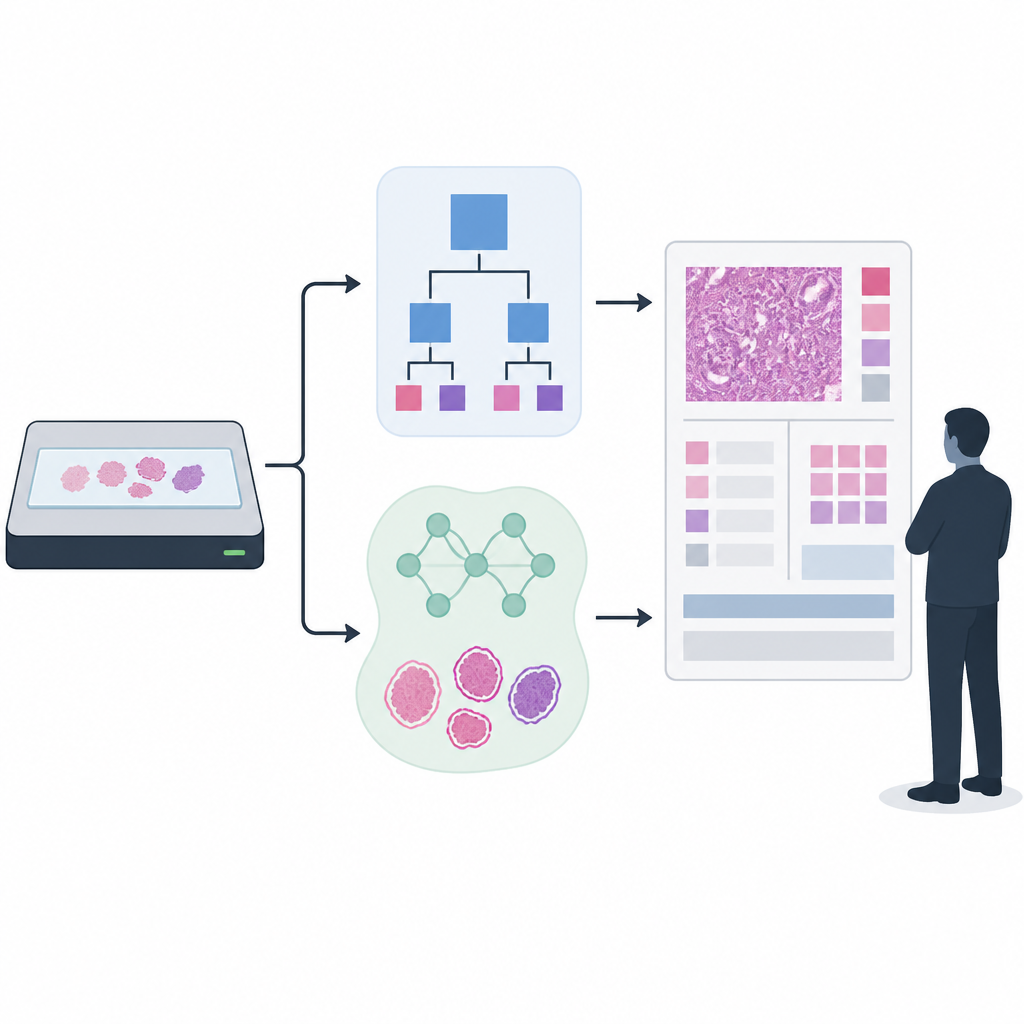
Construcción y prueba de dos enfoques de detección
Los investigadores se centraron en el gradado del cáncer de próstata, en el que las biopsias reciben puntuaciones de Gleason y grados ISUP que guían las decisiones terapéuticas. Compararon un detector de tejido basado en reglas, usado durante mucho tiempo, con un modelo de IA más reciente construido sobre una red de segmentación de imágenes UNet++. Para entrenar y evaluar el detector de tejido usaron más de 33.000 láminas escaneadas de varios hospitales y tipos de escáner, combinando contornos de tejido generados automáticamente con conjuntos más pequeños que fueron revisados y refinados manualmente por expertos. Para el gradado del cáncer posterior aplicaron una IA de última generación entrenada con más de 55.000 láminas y luego probada en 13 centros clínicos usando 13 escáneres diferentes, reflejando la diversidad desordenada de la práctica clínica real.
Qué tan bien ve cada método el tejido
Cuando miraron únicamente la precisión con la que cada método marcaba píxeles de tejido, ambos funcionaron bien en promedio. El detector basado en IA capturó un poco más de tejido verdadero en general, mientras que el método clásico fue algo mejor evitando marcar el fondo. La diferencia crucial apareció en láminas atípicas y raras con apariencia inusual. En estos casos difíciles, el método basado en reglas a veces dejó de detectar grandes porciones de tejido por completo, mientras que el detector de IA generalmente conservó más tejido. En más de 27.000 láminas de evaluación, el número de fallos completos en los que no se detectó tejido en absoluto cayó de 118 con el método clásico a 24 con el detector basado en IA, lo que sugiere que la IA puede ofrecer una ventaja de seguridad al reducir omisiones catastróficas.
¿Mejora el gradado del cáncer con una mejor detección de tejido?
El equipo preguntó después si estas diferencias en los mapas de tejido cambiaban realmente los grados finales de cáncer producidos por la IA posterior. Para ser justos, solo analizaron láminas en las que ambos métodos de detección encontraron al menos algo de tejido y compararon el acuerdo entre los grados predichos por la IA y los asignados por patólogos. En este gran conjunto de láminas, el rendimiento global del gradado fue muy similar tanto si el sistema usaba detección de tejido basada en reglas como si usaba IA, con intervalos de confianza solapados en todas las cohortes clínicas. En otras palabras, para las láminas típicas, el paso inicial de detección no limitó claramente la precisión de un modelo de gradado moderno y potente, incluso cuando se empleó un detector más antiguo y simple.
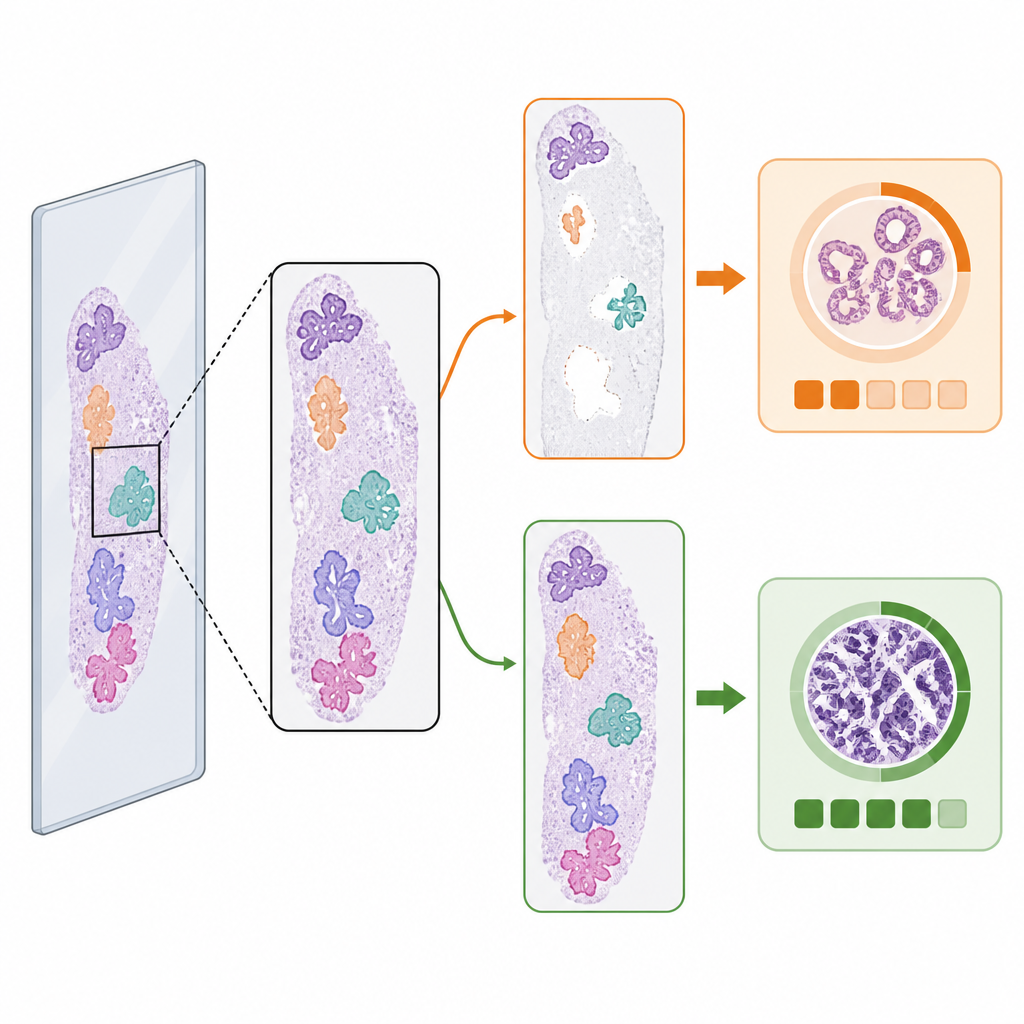
Cuando el primer paso cambia la respuesta
A pesar de promedios similares, la elección del detector de tejido sí cambió el grado de cáncer predicho en una pequeña pero importante fracción de casos. Entre las láminas malignas con gradado de referencia por lámina, el 3,5 por ciento presentó predicciones de grado ISUP diferentes según el detector de tejido utilizado. En aproximadamente igual número de esos casos, el detector de IA condujo al grado correcto cuando el método clásico no lo hizo, y a la inversa en otros. Ejemplos visuales mostraron por qué: si un detector omitía una gran porción de tejido que contenía tumor o identificaba restos como tejido, la IA de gradado podía verse empujada hacia una categoría de riesgo más baja o más alta. Estos “casos límite” subrayan cómo cambios sutiles en qué fragmentos de imagen llegan al modelo de gradado pueden alterar su decisión final.
Qué significa esto para la futura IA en cáncer
Por ahora, el estudio sugiere que en conjuntos de datos de alta calidad y multicéntricos de biopsias prostáticas, el método exacto usado para la detección de tejido no cambia de forma marcada la precisión media del gradado avanzado basado en IA. Sin embargo, la detección de tejido mediante IA reduce claramente la tasa de fallos completos y puede influir en los resultados en un pequeño subconjunto de casos malignos, donde la omisión de tejido podría ser más perjudicial. Los autores sostienen que la detección de tejido debe tratarse como una parte integral y auditable de los sistemas de IA diagnóstica, con visualización clara para los patólogos y continua investigación en modelos robustos y eficientes a medida que las IAs posteriores se vuelven aún más precisas.
Cita: Boman, S.E., Mulliqi, N., Blilie, A. et al. The impact of tissue detection on diagnostic artificial intelligence algorithms in prostate digital pathology. Sci Rep 16, 14968 (2026). https://doi.org/10.1038/s41598-026-52148-9
Palabras clave: patología digital, cáncer de próstata, detección de tejido, gradado de Gleason, IA diagnóstica