Clear Sky Science · pl
Wpływ wykrywania tkanek na diagnostyczne algorytmy sztucznej inteligencji w cyfrowej patologii gruczołu krokowego
Dlaczego pierwszy krok w AI onkologicznej ma znaczenie
W miarę jak szpitale coraz częściej wykorzystują sztuczną inteligencję do wspomagania odczytu biopsji prostaty, cisza i pozornie prozaiczny, lecz kluczowy etap często pozostaje niezauważony: po prostu zlokalizować, gdzie na cyfrowym preparacie znajduje się tkanka. Jeśli ten pierwszy krok zawiedzie i ważne fragmenty tkanki zostaną pominięte, nawet najbardziej zaawansowane AI wykrywające nowotwory może zostać wprowadzona w błąd. W tym badaniu pytano, jak bardzo ten podstawowy etap faktycznie wpływa na ogólną wydajność oraz czy nowoczesne AI potrafi bezpieczniej wykrywać tkankę niż starsze metody oparte na regułach.
Od szkiełka do obrazu cyfrowego
W patologii cyfrowej cienkie przekroje tkanki prostaty są skanowane do obrazów o wysokiej rozdzielczości. Zanim którykolwiek algorytm oceny nowotworu zacznie działać, system musi odróżnić tkankę od pustego tła. Tradycyjnie robi się to prostymi regułami opartymi na kolorze i jasności, na przykład ustalając próg decydujący, które piksele prawdopodobnie reprezentują tkankę. Nowsze systemy zamiast tego trenują modele AI do rozpoznawania kształtów i wzorców tkanki, podobnie jak w innych złożonych zadaniach. Pytanie brzmi, czy ta modernizacja „instalacji” rzeczywiście poprawia ocenę nowotworów w praktyce klinicznej, czy głównie zmniejsza rzadkie, lecz poważne awarie.
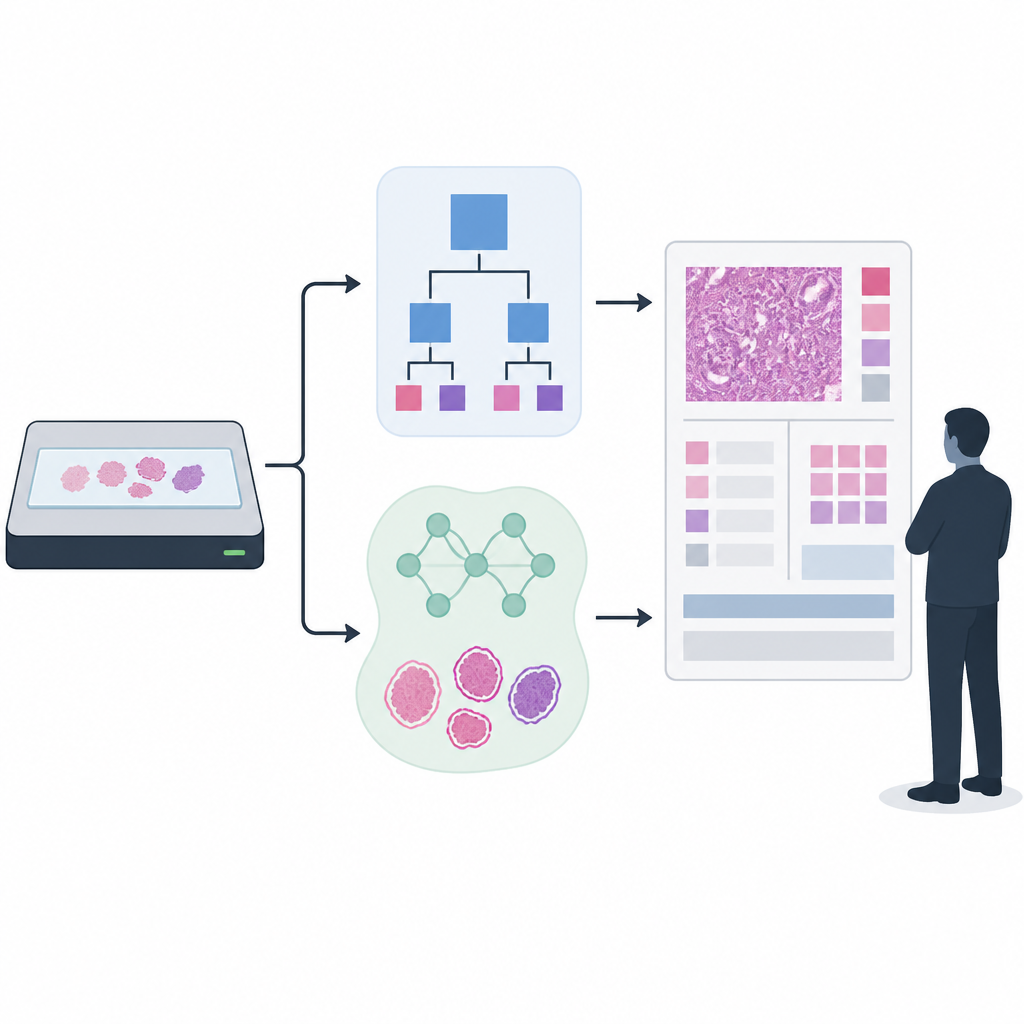
Budowa i testowanie dwóch podejść do detekcji
Naukowcy skupili się na ocenie stopnia zaawansowania raka prostaty, w której biopsje otrzymują wyniki Gleasona i stopnie ISUP, kierujące decyzjami terapeutycznymi. Porównali długo stosowany detektor oparty na regułach z nowszym modelem AI zbudowanym na sieci segmentacyjnej UNet++. Do trenowania i oceny detektora tkanek użyli ponad 33 000 zeskanowanych preparatów z kilku szpitali i typów skanerów, łącząc automatycznie wygenerowane obrysy tkanek z mniejszymi zestawami starannie sprawdzanymi i poprawianymi przez ekspertów. Do oceny dalszej części potoku — czyli klasyfikacji nowotworu — zastosowali nowoczesne AI wytrenowane na ponad 55 000 preparatach, a następnie przetestowane w 13 ośrodkach klinicznych na 13 różnych skanerach, odzwierciedlając chaotyczną różnorodność praktyki klinicznej.
Jak dobrze każda metoda widzi tkankę
Gdy oceniano wyłącznie, jak dokładnie każda metoda oznacza piksele tkankowe, obie sprawdziły się dobrze przeciętnie. Detektor oparty na AI wychwytywał nieco więcej rzeczywistej tkanki ogólnie, podczas gdy metoda klasyczna lepiej unikała obszarów tła. Kluczowa różnica pojawiła się w rzadkich slajdach‑odchyleniach o nietypowym wyglądzie. W tych trudnych przypadkach metoda oparta na regułach czasem całkowicie pomijała duże fragmenty tkanki, podczas gdy detektor AI zwykle zachowywał ich więcej. Wśród ponad 27 000 slajdów ewaluacyjnych liczba całkowitych awarii, w których w ogóle nie wykryto tkanki, spadła z 118 przy metodzie klasycznej do 24 przy detektorze opartym na AI, co sugeruje, że AI może oferować przewagę bezpieczeństwa poprzez zmniejszenie katastrofalnych pominięć.
Czy lepsze wykrywanie tkanek poprawia ocenę nowotworu?
Zespół następnie zapytał, czy te różnice w mapach tkanek faktycznie zmieniają końcowe oceny nowotworu wydawane przez dalsze AI. Dla uczciwości analizowano tylko preparaty, w których obie metody wykrywania znalazły przynajmniej część tkanki, i porównano zgodność między stopniami przewidywanymi przez AI a tymi nadawanymi przez patologów. W tym dużym zbiorze wynik ogólny oceny był bardzo podobny, niezależnie od tego, czy system korzystał z wykrywania opartego na regułach, czy na AI, z zachodzącymi na siebie przedziałami ufności we wszystkich kohortach klinicznych. Innymi słowy, dla typowych slajdów początkowy etap detekcji nie ograniczał wyraźnie dokładności silnego, nowoczesnego modelu oceniającego, nawet gdy użyto starszego, prostszego detektora.
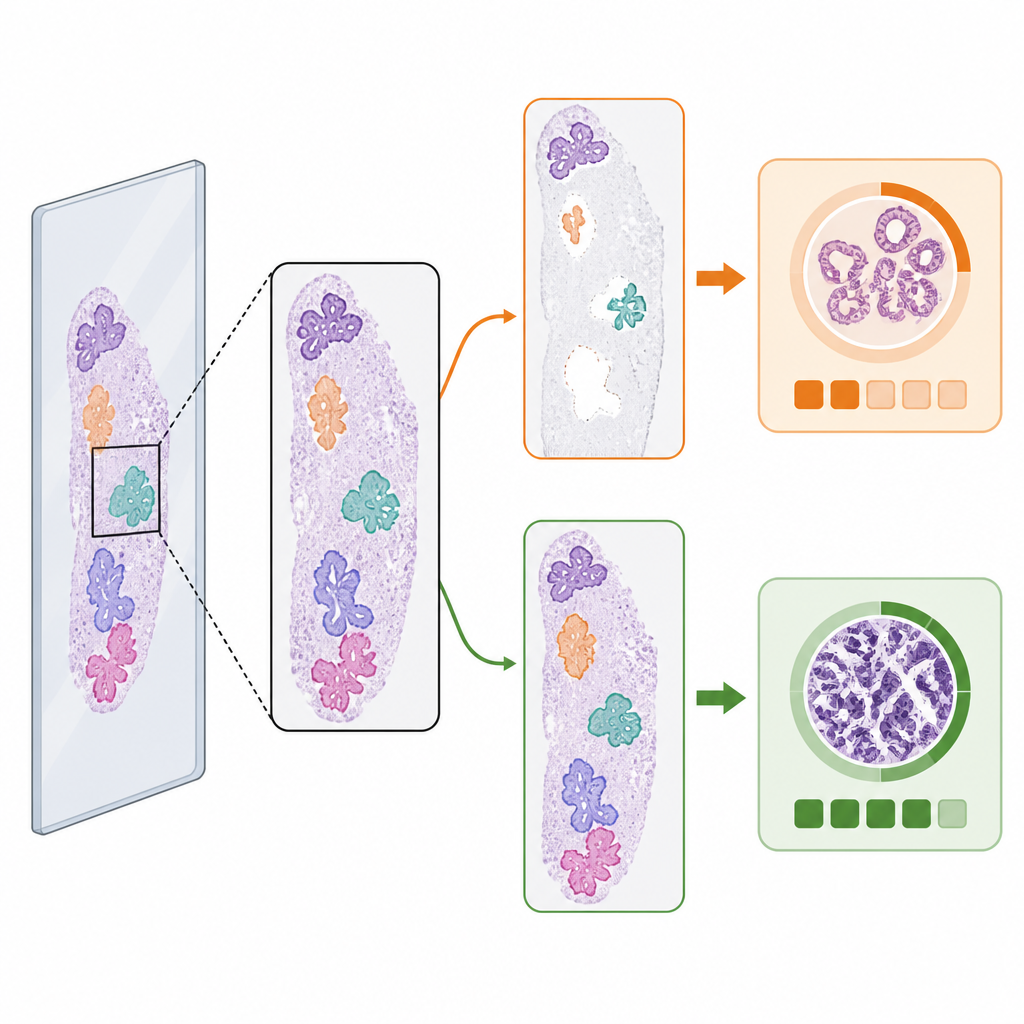
Kiedy pierwszy krok zmienia odpowiedź
Pomimo podobnych średnich, wybór detektora tkanek zmieniał przewidywany stopień nowotworu w niewielkim, lecz istotnym odsetku przypadków. Wśród złośliwych slajdów z odniesieniem per‑slajdowym 3,5 procent miało różne przewidywania stopnia ISUP w zależności od użytego detektora tkanek. W mniej więcej równych liczbach zdarzało się, że detektor AI dawał poprawną ocenę, gdy metoda klasyczna tego nie robiła, i odwrotnie. Przykłady wizualne pokazywały, dlaczego: jeśli jeden detektor pominął duży fragment tkanki zawierającej guz lub błędnie potraktował zanieczyszczenia jako tkankę, AI oceniające mogło zostać przesunięte w kierunku niższej lub wyższej kategorii ryzyka. Te „przypadki brzegowe” uwypuklają, jak subtelne zmiany w tym, które fragmenty obrazu trafiają do modelu oceniającego, mogą zmienić jego ostateczną decyzję.
Co to oznacza dla przyszłości AI w onkologii
Na razie badanie sugeruje, że w wysokiej jakości, wielomiejscowych zestawach biopsji prostaty dokładna metoda wykrywania tkanek nie zmienia znacząco średniej trafności zaawansowanej oceny AI. Jednak wykrywanie tkanek oparte na AI wyraźnie zmniejsza częstość całkowitych awarii i może wpłynąć na wyniki w niewielkiej podgrupie złośliwych przypadków, w których pominięcie tkanki może być najbardziej szkodliwe. Autorzy argumentują, że wykrywanie tkanek powinno być traktowane jako integralna, audytowalna część diagnostycznych systemów AI, z wyraźną wizualizacją dla patologów oraz dalszymi badaniami nad odpornymi i wydajnymi modelami w miarę jak downstreamowe AI stają się jeszcze bardziej precyzyjne.
Cytowanie: Boman, S.E., Mulliqi, N., Blilie, A. et al. The impact of tissue detection on diagnostic artificial intelligence algorithms in prostate digital pathology. Sci Rep 16, 14968 (2026). https://doi.org/10.1038/s41598-026-52148-9
Słowa kluczowe: patologia cyfrowa, rak prostaty, wykrywanie tkanek, skoring Gleasona, diagnostyczna AI