Clear Sky Science · de
Die Auswirkung der Gewebeerkennung auf diagnostische KI‑Algorithmen in der digitalen Prostatapathologie
Warum der erste Schritt in der Krebs‑KI wichtig ist
Da Krankenhäuser vermehrt künstliche Intelligenz zur Unterstützung bei der Befundung von Prostatabiopsien einsetzen, bleibt ein leiser, aber entscheidender Schritt oft unbeachtet: einfach zu erkennen, wo sich das Gewebe auf einem digitalen Slide befindet. Scheitert dieser erste Schritt und werden wichtige Gewebeteile übersehen, kann selbst die ausgefeilteste Krebs‑KI fehlgeleitet werden. Diese Studie fragt, wie stark dieser grundlegende Schritt die Gesamtergebnisse beeinflusst und ob moderne KI‑Systeme bei der Geweiserkennung sicherer arbeiten als ältere, regelbasierte Methoden.
Vom Glasobjektträger zum Digitalbild
In der digitalen Pathologie werden dünne Prostatagewebeschnitte in hochauflösende Bilder gescannt. Bevor ein Algorithmus zur Krebsbewertung arbeiten kann, muss das System Gewebe vom leeren Hintergrund trennen. Traditionell geschieht das mit einfachen Regeln, die auf Farbe und Helligkeit beruhen, etwa durch das Festlegen eines Schwellenwerts zur Unterscheidung von tendenziell Gewebe‑Pixeln. Neuere Systeme trainieren stattdessen KI‑Modelle, um Gewebeformen und ‑muster zu erkennen, ähnlich wie bei komplexeren Aufgaben. Fraglich ist, ob dieses Upgrade in der „Rohrleitung“ der Pipeline die krebsbezogene Bewertung in der Praxis tatsächlich verbessert oder vor allem seltene, aber gravierende Ausfälle reduziert.
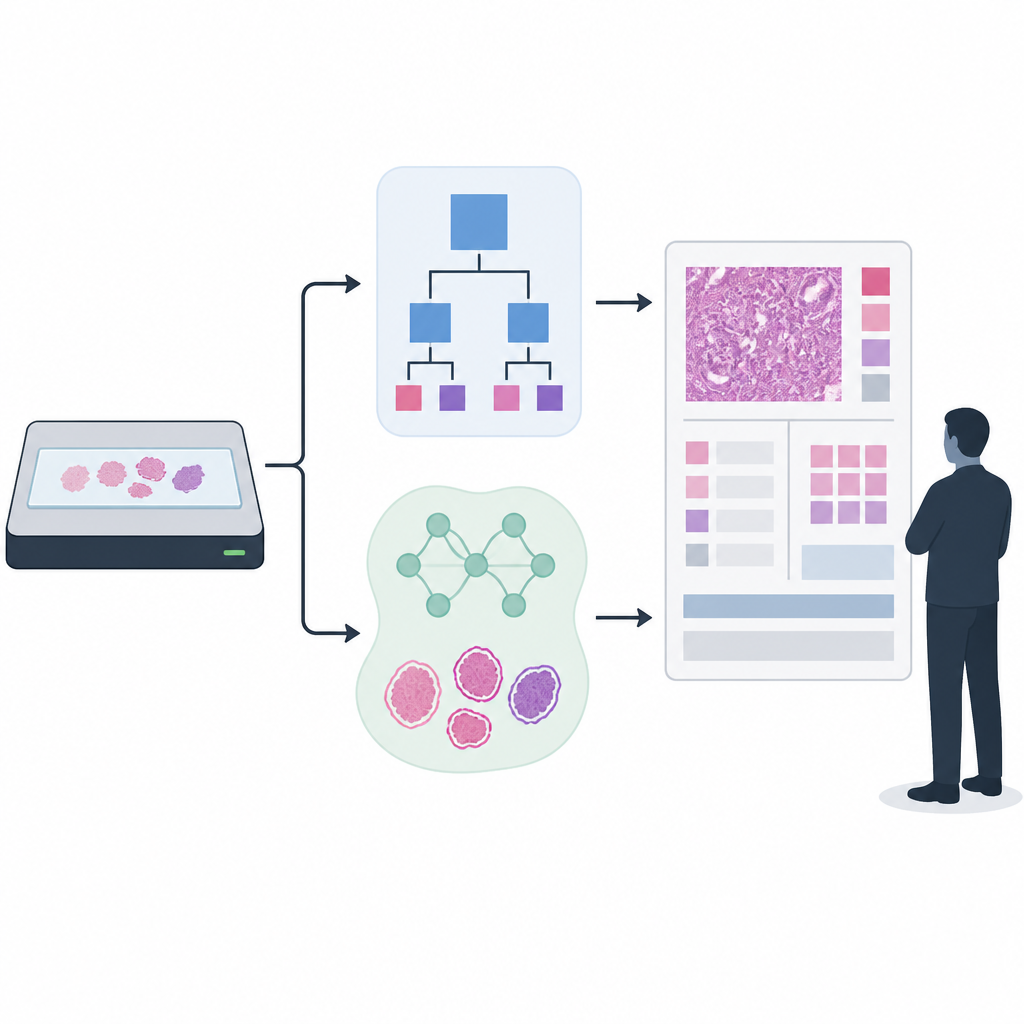
Aufbau und Test zweier Erkennungsansätze
Die Forschenden konzentrierten sich auf die Prostatakrebsbewertung, bei der Biopsien Gleason‑Scores und ISUP‑Grade erhalten, die Therapieentscheidungen leiten. Sie verglichen einen lang verwendeten regelbasierten Gewebeerkenner mit einem neueren KI‑Modell, das auf einem UNet++‑Segmentierungsnetzwerk basiert. Zum Trainieren und Evaluieren des Gewebeerkenners nutzten sie mehr als 33.000 gescannte Slides aus mehreren Krankenhäusern und Scannertypen, kombiniert mit automatisch generierten Gewebeumrissen und kleineren Mengen, die von Experten mühsam geprüft und verfeinert wurden. Für die nachgelagerte Krebsbewertung setzten sie eine hochmoderne KI ein, die auf über 55.000 Slides trainiert worden war und anschließend an 13 klinischen Standorten mit 13 verschiedenen Scannern getestet wurde, um die heterogene Realität klinischer Praxis abzubilden.
Wie gut jede Methode das Gewebe erkennt
Betrachtet man allein die Genauigkeit, mit der jede Methode Gewebe‑Pixel markierte, schnitten beide im Mittel gut ab. Der KI‑basierte Detektor erfasste insgesamt geringfügig mehr echtes Gewebe, während die klassische Methode etwas besser darin war, Hintergrundflächen zu vermeiden. Der entscheidende Unterschied zeigte sich bei seltenen Ausreißer‑Slides mit ungewöhnlichem Erscheinungsbild. In diesen schwierigen Fällen verpasste die regelbasierte Methode manchmal große Gewebestücke vollständig, während der KI‑Detektor in der Regel mehr davon erhalten ließ. Bei über 27.000 Bewertungs‑Slides sank die Zahl kompletter Ausfälle, bei denen gar kein Gewebe erkannt wurde, von 118 mit der klassischen Methode auf 24 mit dem KI‑basierten Detektor, was darauf hindeutet, dass KI einen Sicherheitsvorteil bieten kann, indem sie katastrophale Fehlschläge reduziert.
Verbessert bessere Gewebeerkennung die Krebsbewertung?
Das Team fragte dann, ob diese Unterschiede in den Gewebe‑Karten die endgültigen Krebsgrade des nachgelagerten KI‑Systems tatsächlich veränderten. Der Fairness halber analysierten sie nur Slides, bei denen beide Gewebeerkennungsmethoden mindestens etwas Gewebe fanden, und verglichen die Übereinstimmung zwischen KI‑vorhergesagten Graden und den von Pathologen vergebenen Graden. In diesem großen Slidesatz war die Gesamtleistung der Bewertung sehr ähnlich, unabhängig davon, ob ein regelbasierter oder ein KI‑gestützter Gewebeerkenner verwendet wurde, mit sich überlappenden Konfidenzintervallen in allen klinischen Kohorten. Mit anderen Worten: Bei typischen Slides begrenzte der anfängliche Erkennungsschritt die Genauigkeit eines starken modernen Bewertungsmodells nicht eindeutig, selbst wenn ein älterer, einfacherer Detektor zum Einsatz kam.
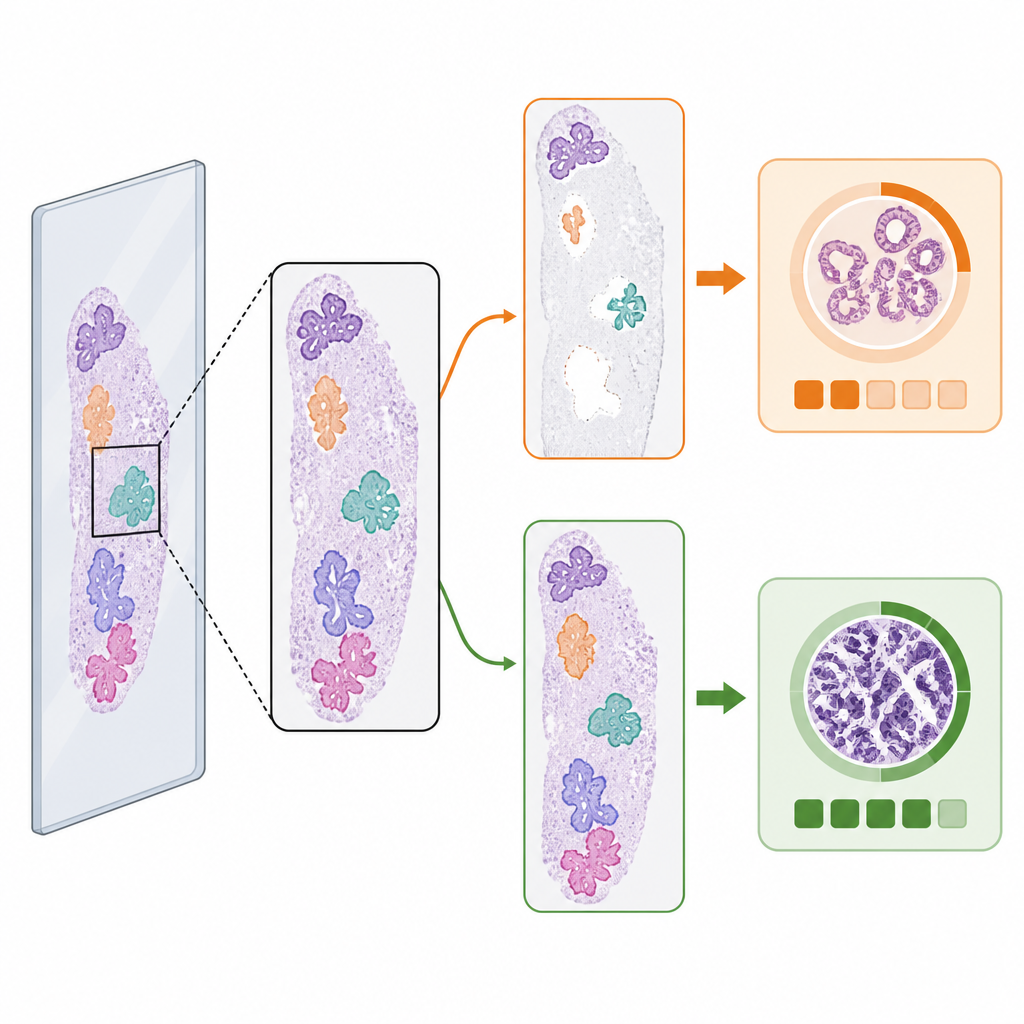
Wenn der erste Schritt die Antwort verändert
Trotz ähnlicher Durchschnitte veränderte die Wahl des Gewebeerkenners die vorhergesagte Krebsstufe in einem kleinen, aber wichtigen Teil der Fälle. Unter malignen Slides mit pro‑Slide Referenzbewertung hatten 3,5 Prozent unterschiedliche ISUP‑Grade je nachdem, welcher Gewebeerkenner verwendet wurde. Bei etwa gleicher Anzahl dieser Fälle führte der KI‑Detektor zur korrekten Bewertung, wenn die klassische Methode dies nicht tat, und umgekehrt. Visuelle Beispiele zeigten, warum: Wenn ein Detektor ein großes, tumorführendes Gewebestück verfehlte oder Schmutz als Gewebe identifizierte, konnte die Bewertungs‑KI in eine niedrigere oder höhere Risikokategorie gedrängt werden. Diese „Randfälle“ verdeutlichen, wie subtile Änderungen darin, welche Bildausschnitte das Bewertungsmodell erreichen, dessen abschließende Entscheidung beeinflussen können.
Was das für die künftige Krebs‑KI bedeutet
Die Studie legt nahe, dass in hochwertigen, multizentrischen Prostatabiopsie‑Datensätzen die genaue Methode der Gewebeerkennung die durchschnittliche Genauigkeit fortgeschrittener KI‑basierter Bewertungen nicht stark verändert. Gleichzeitig reduziert die KI‑basierte Gewebeerkennung klar die Rate kompletter Ausfälle und kann in einer kleinen Teilmenge maligner Fälle die Ergebnisse beeinflussen, in denen fehlendes Gewebe am schädlichsten wäre. Die Autoren argumentieren, dass die Gewebeerkennung als integraler, prüfbarer Bestandteil diagnostischer KI‑Systeme behandelt werden sollte, mit klarer Visualisierung für Pathologen und fortgesetzter Forschung zu robusten, effizienten Modellen, während nachgelagerte KIs noch präziser werden.
Zitation: Boman, S.E., Mulliqi, N., Blilie, A. et al. The impact of tissue detection on diagnostic artificial intelligence algorithms in prostate digital pathology. Sci Rep 16, 14968 (2026). https://doi.org/10.1038/s41598-026-52148-9
Schlüsselwörter: digitale Pathologie, Prostatakrebs, Gewebeerkennung, Gleason‑Bewertung, diagnostische KI