Clear Sky Science · ar
تأثير كشف الأنسجة على خوارزميات الذكاء الاصطناعي التشخيصية في علم الأمراض الرقمي للبروستات
لماذا تهم الخطوة الأولى في ذكاء السرطان الاصطناعي
مع اعتماد المستشفيات بشكل متزايد على الذكاء الاصطناعي للمساعدة في قراءة خزعات البروستات، هناك خطوة هادئة لكنها حاسمة غالبًا ما تمر دون ملاحظة: ببساطة تحديد مكان النسيج على الشريحة الرقمية. إذا فشلت هذه الخطوة الأولى وفُقدت أجزاء مهمة من النسيج، حتى أكثر أنظمة كشف السرطان ذكاءً يمكن أن تُقاد إلى نتيجة خاطئة. تسأل هذه الدراسة إلى أي مدى تهم هذه الخطوة الأساسية في الأداء الكلي، وما إذا كان الذكاء الاصطناعي الحديث يقوم بعمل أكثر أمانًا من الطرق القديمة القائمة على قواعد ثابتة في اكتشاف الأنسجة أولاً.
من الشريحة الزجاجية إلى الصورة الرقمية
في علم الأمراض الرقمي، تُمسح شرائح رقيقة من نسيج البروستات إلى صور عالية الدقة. قبل أن يبدأ أي خوارزمية لتصنيف السرطان عملها، يجب على النظام فصل النسيج عن الخلفية الفارغة. تقليديًا يُنفّذ ذلك بواسطة قواعد بسيطة تستند إلى اللون والسطوع، مثل تعيين حد لتحديد أي البكسلات من المرجح أن تكون نسيجًا. تستخدم الأنظمة الأحدث بدلاً من ذلك نماذج ذكاء اصطناعي لتعرّف أشكال وأنماط الأنسجة، كما تفعل في مهام أكثر تعقيدًا. والسؤال هو ما إذا كان هذا التحديث في "بنية" خط المعالجة يحسّن حقًا التصنيف السريري الواقعي للسرطان، أم أنه يقلل أساسًا من حالات الفشل النادرة لكن الخطيرة.
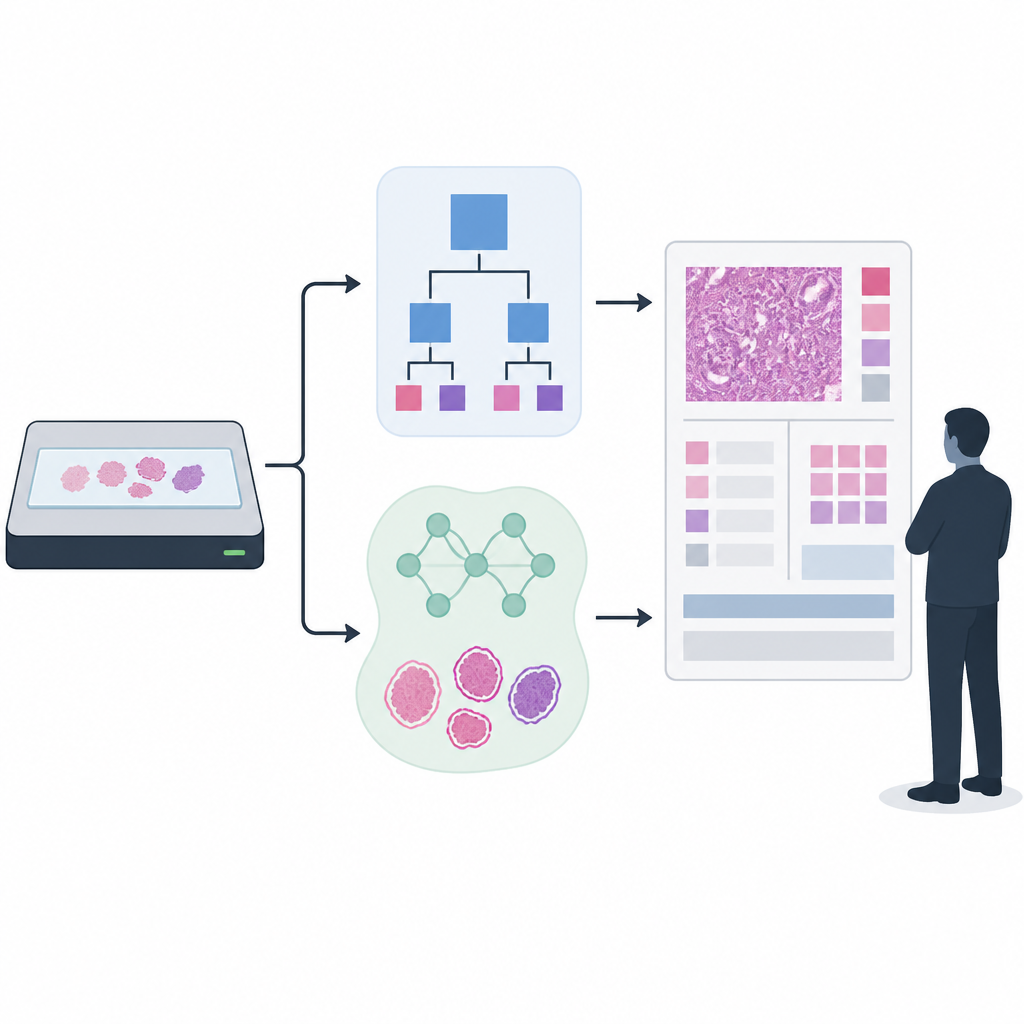
بناء واختبار نهجين للكشف
ركز الباحثون على تصنيف سرطان البروستات، حيث تُمنح الخزعات درجات غليسون ودرجات ISUP التي توجه قرارات العلاج. قارنوا كاشف نسيج تقليدي قائم على قواعد مستخدم منذ وقت طويل مع نموذج ذكاء اصطناعي أحدث مبني على شبكة تجزئة صور UNet++. لتدريب وتقييم كاشف النسيج، استخدموا أكثر من 33,000 شريحة ممسوحة ضوئيًا من عدة مستشفيات وأنواع ماسحات ضوئية، جامعِينَ مخططات حدود نسيج مولدة آليًا مع مجموعات أصغر تم التحقق منها وتعديلها بعناء من قبل خبراء. ولتصنيف السرطان اللاحق، طبّقوا ذكاءً اصطناعيًا حديثًا تم تدريبه على أكثر من 55,000 شريحة ثم اختبر عبر 13 موقعًا سريريًا باستخدام 13 ماسحًا مختلفًا، مما يعكس التنوع المعقّد للممارسة السريرية الحقيقية.
مدى دقة كل طريقة في رؤية النسيج
عند النظر فقط إلى مدى دقة كل طريقة في تمييز بكسلات النسيج، أدت كلتاهما أداءً جيدًا في المتوسط. التقط الكاشف المعتمد على الذكاء الاصطناعي قدراً طفيفًا أكبر من النسيج الحقيقي بشكل عام، بينما كانت الطريقة الكلاسيكية أفضل قليلاً في تجنّب مناطق الخلفية. بدا الاختلاف الحاسم في الشرائح الشاذة النادرة ذات المظهر غير المعتاد. في هذه الحالات الصعبة، كانت الطريقة القائمة على القواعد أحيانًا تفقد كتلًا كبيرة من النسيج بالكامل، بينما حافظ كاشف الذكاء الاصطناعي عمومًا على جزء أكبر منها. عبر أكثر من 27,000 شريحة تقييمية، انخفض عدد حالات الفشل الكامل التي لم يُكتشف فيها أي نسيج على الإطلاق من 118 مع الطريقة الكلاسيكية إلى 24 مع الكاشف المعتمد على الذكاء الاصطناعي، مما يشير إلى أن الذكاء الاصطناعي قد يوفر ميزة أمان بتقليل حالات الفشل الكارثية.
هل يحسّن كشف النسيج الأفضل تصنيف السرطان؟
سأل الفريق بعد ذلك ما إذا كانت هذه الاختلافات في خرائط النسيج تغيّر بالفعل الدرجات النهائية للسرطان التي ينتجها الذكاء الاصطناعي اللاحق. ومن أجل الإنصاف، حلّلوا فقط الشرائح التي وجد فيها كلا كاشفي النسيج بعض الأنسجة، وقارنوا الاتفاق بين الدرجات المتوقعة بالذكاء الاصطناعي وتلك المعطاة من قبل الأطباء الشرعيين. على هذه المجموعة الكبيرة من الشرائح، كان أداء التصنيف العام متشابهًا جدًا سواء استخدم النظام كشف نسيج قائمًا على قواعد أم كشفًا معتمداً على الذكاء الاصطناعي، مع تداخل فترات الثقة عبر جميع التجمعات السريرية. بعبارة أخرى، بالنسبة للشرائح النمطية، لم تحدُّ الخطوة الأولى للكشف بوضوح من دقة نموذج التصنيف الحديث القوي، حتى عندما استُخدمت طريقة أقدم وأبسط للكشف.
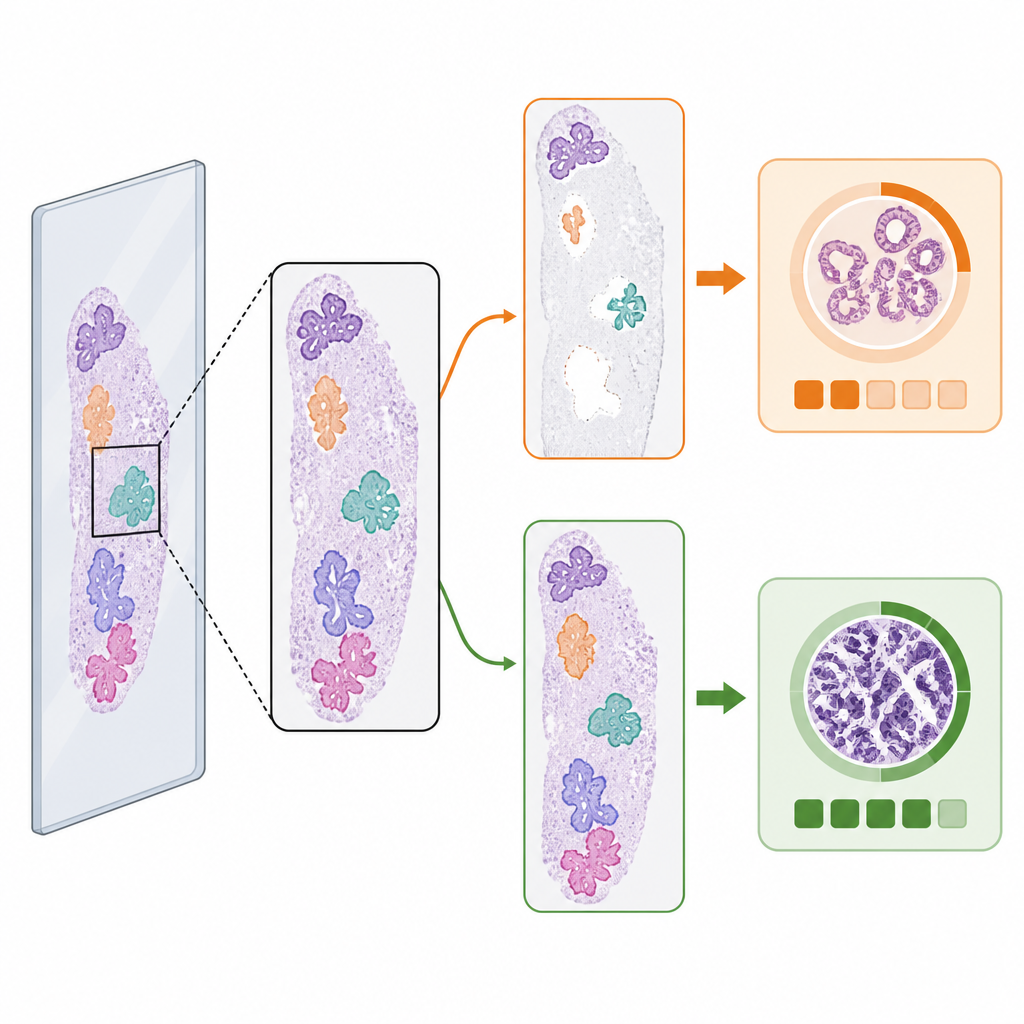
عندما تغيّر الخطوة الأولى النتيجة
على الرغم من المتوسطات المتقاربة، غيّر اختيار كاشف النسيج الدرجة المتوقعة للسرطان في جزء صغير ولكن مهم من الحالات. بين الشرائح الخبيثة التي تملُّها درجات مرجعية لكل شريحة، كانت هناك اختلافات في توقعات درجة ISUP في 3.5 بالمئة اعتمادًا على أي كاشف نسيج استُخدم. في أعداد متقاربة من هذه الحالات، قاد كاشف الذكاء الاصطناعي إلى الدرجة الصحيحة حينما لم تفعل الطريقة الكلاسيكية، والعكس صحيح في حالات أخرى. أظهرت أمثلة بصرية السبب: إذا فات كاشف ما قطعة كبيرة من النسيج المحتوي على ورم أو حدد حطامًا خطأً كنسيج، يمكن أن يدفع ذلك خوارزمية التصنيف نحو فئة مخاطرة أقل أو أعلى. تبرز هذه "الحالات الحدية" كيف أن تغييرات بسيطة في أي مقاطع الصورة تصل إلى نموذج التصنيف يمكن أن تغيّر قراره النهائي.
ماذا يعني هذا لمستقبل ذكاء السرطان الاصطناعي
في الوقت الحالي، تشير الدراسة إلى أنه في مجموعات بيانات خزعات البروستات عالية الجودة ومتعددة المواقع، لا تغير الطريقة الدقيقة المستخدمة لكشف الأنسجة بشكل قوي الدقة المتوسطة لتصنيف حديث قائم على الذكاء الاصطناعي. ومع ذلك، يقلل كشف الأنسجة المعتمد على الذكاء الاصطناعي بوضوح من معدل حالات الفشل الكاملة ويمكن أن يؤثر على النتائج في مجموعة فرعية صغيرة من الحالات الخبيثة، حيث قد يكون فقدان النسيج الأكثر ضررًا. يجادل المؤلفون بأن كشف الأنسجة يجب أن يُعامل كجزء متكامل وقابل للتدقيق من أنظمة الذكاء الاصطناعي التشخيصية، مع تصور واضح للأطباء الشرعيين ومواصلة البحث في نماذج فعالة ومتينة مع تزايد دقة نماذج المعالجة اللاحقة.
الاستشهاد: Boman, S.E., Mulliqi, N., Blilie, A. et al. The impact of tissue detection on diagnostic artificial intelligence algorithms in prostate digital pathology. Sci Rep 16, 14968 (2026). https://doi.org/10.1038/s41598-026-52148-9
الكلمات المفتاحية: علم الأمراض الرقمي, سرطان البروستات, كشف الأنسجة, تصنيف غليسون, الذكاء الاصطناعي التشخيصي