Clear Sky Science · sv
Upskattning av major patologisk respons hos patienter med icke-småcellig lungcancer efter neoadjuvant behandling med MMT-net
Hjälper läkare att se om behandlingen lyckats
När personer med lungcancer får starka behandlingar innan operation behöver läkare veta hur väl dessa terapier fungerat i tumören. I dag bygger den bedömningen på patologer som mödosamt granskar enorma digitala mikroskopbilder för hand. Denna studie presenterar ett nytt verktyg med artificiell intelligens, kallat MMT-Net, som snabbt och precist kan uppskatta hur stor del av en lungtumör som har förstörts av behandlingen — vilket potentiellt kan göra vården snabbare, mer konsekvent och mer personlig.
Varför det är viktigt att mäta vad som återstår
För patienter med icke-småcellig lungcancer använder läkare ofta läkemedel och strålning före operation för att krympa eller försvaga tumören. Efter operation uppskattar patologer den så kallade ”major patologiska responsen” genom att kontrollera vilken andel av tumörens säng som fortfarande innehåller levande cancerceller. Om bara en liten mängd — ungefär en tiondel eller mindre — återstår tenderar patienter att leva längre och få ett bättre utfall. Moderna digitala preparat kan dock innehålla miljarder pixlar, och behandlingen kan lämna kvar en förvirrande blandning av död vävnad, ärrliknande områden och spridda överlevande celler. Att manuellt granska dessa enorma bilder är långsamt, utmattande och känsligt för variation mellan experter.
Att lära datorer att läsa cancerslides
Forskarna byggde MMT-Net för att hjälpa patologer i denna krävande uppgift. Systemet analyserar helbildsaker (whole slide images) av lungtumörer som redan behandlats. Istället för att förlita sig på standardmodeller för datorseende tränade på vardagsfotografier lät de först nätverket lära sig patologins visuella ”språk” på egen hand med tusentals odöpta vävnadsbitar. Detta självstyrda inlärningssteg hjälper modellen att känna igen subtila mönster som är specifika för färgade mikroskopbilder, snarare än katter, bilar eller landskap.
Att se nära och långt samtidigt
MMT-Net efterliknar också hur mänskliga experter zoomar in och ut när de läser ett preparat. Systemet tar små bildlappor i tre förstoringar: låg förstoring för att fånga övergripande arkitektur, medel för att se skademönster och hög förstoring för att inspektera enskilda celler. En specialiserad attention-mekanism sammanfogar sedan dessa vyer, vilket gör att modellen kan väga detaljinformation och bred kontext tillsammans. En transformer-modul — ursprungligen utvecklad för språköversättning — använder dessa sammanflätade egenskaper för att sortera varje lapp i tre kategorier: kvarvarande levande tumör, behandlingsrelaterad ärrliknande stromal vävnad, eller död och keratiniserad materia. Genom att summera över hela preparatet uppskattar MMT-Net andelen levande tumörceller, den nyckelstorhet som läkare använder för att bedöma respons.
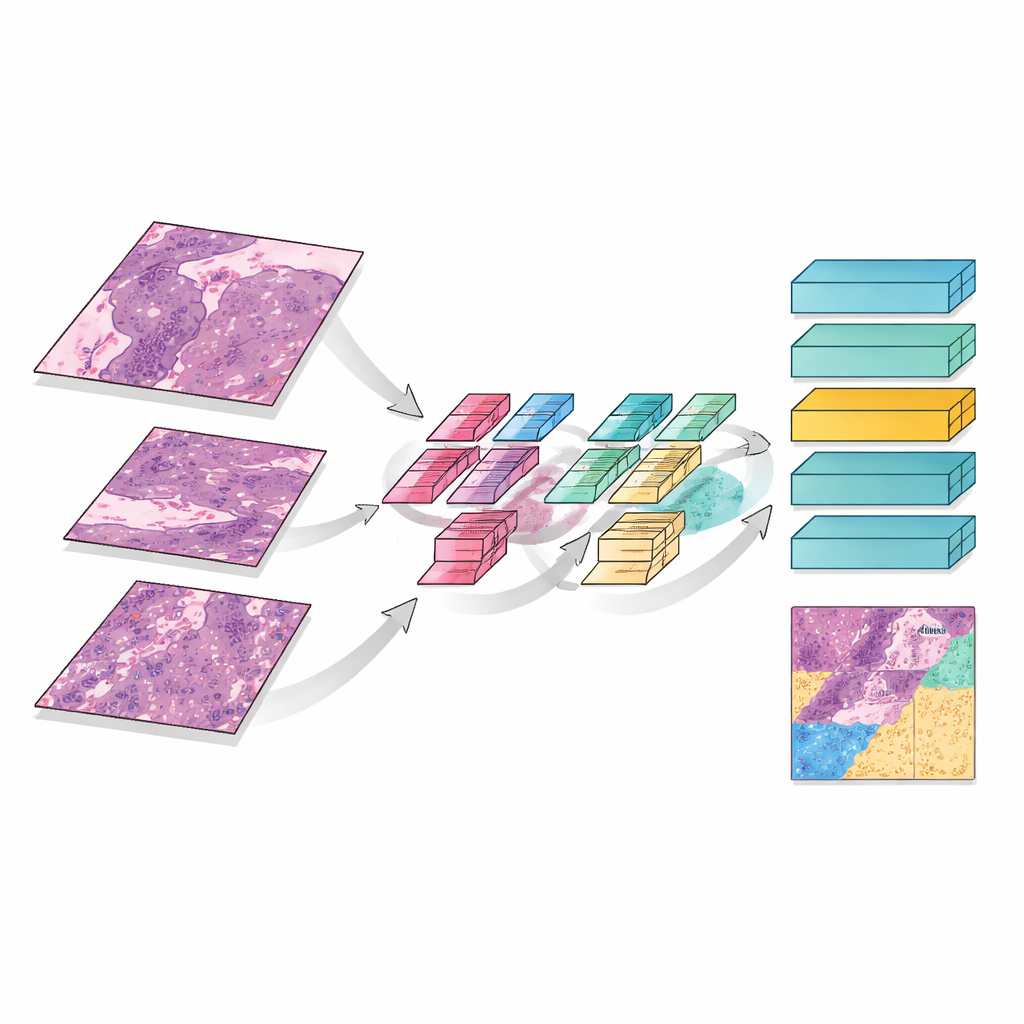
Hur väl systemet presterar
För att testa modellen använde teamet preparat från 23 patienter behandlade vid ett enda cancercenter. De delade upp data i tränings- och testgrupper, där expertpatologer noggrant markerade områden med viabel tumör, ärrliknande stroma och död vävnad enligt internationella riktlinjer. Jämfört med flera ledande djuplärningsmetoder uppnådde MMT-Net högst noggrannhet och klassificerade vävnadstyper korrekt i omkring 99 procent av testlapparna när den förtränats på patologibilder. De områden som lyftes fram av modellens interna attention-kartor överensstämde nära med de regioner mänskliga specialister fokuserar på, vilket tyder på att systemet ”tittar” på rätt strukturer snarare än att förlita sig på slumpmässiga ledtrådar.
Jämförelse med molekylära markörer
Utöver visuell jämförelse undersökte forskarna om MMT-Nets prediktioner stämmer överens med biologiska mått på tumöraktivitet. De granskade ytterligare preparat färgade för två vanliga laboratoriemarkörer: cytokeratiner, som markerar tumörceller av epitelialt ursprung, och Ki67, som markerar delande celler. Andelen regioner som modellen betecknade som viabel tumör visade en stark statistisk korrelation med båda markörerna, vilket innebär att där datorn såg aktiv tumör höll laboratoriefärgningarna med. Denna täta överensstämmelse stödjer idén att MMT-Net fångar verkliga aspekter av sjukdomens biologi, inte bara ytliga färgskillnader.
Vad detta kan innebära för patienter
Enkelt uttryckt visar denna studie att ett omsorgsfullt utformat AI-system kan uppskatta hur mycket lungtumör som återstår efter förbehandling nästan lika bra som expertpatologer, på ett sätt som är förklarligt och biologiskt förankrat. Arbetet är gjort på en relativt liten patientgrupp från ett enda center, och större studier över flera sjukhus behövs fortfarande, men tillvägagångssättet är flexibelt och kan anpassas till andra cancerformer och uppgifter. I framtiden kan verktyg som MMT-Net bidra till att standardisera hur behandlingssvar mäts, stödja mer tillförlitliga beslut om uppföljande behandlingar och föra precisionsmedicin närmare vardaglig klinisk praxis.
Citering: Yang, C., Liu, L., Xiao, W. et al. Estimating major pathological response in non-small cell lung cancer patients with post-neoadjuvant therapy using MMT-net. Sci Rep 16, 14144 (2026). https://doi.org/10.1038/s41598-026-44633-y
Nyckelord: lungcancer, digital patologi, artificiell intelligens, behandlingssvar, djuplärning