Clear Sky Science · nl
Schatting van major pathological response bij patiënten met niet-kleincellige longkanker na neoadjuvante therapie met MMT-net
Artsen helpen de behandeluitkomst te zien
Wanneer mensen met longkanker krachtige behandelingen vóór de operatie krijgen, moeten artsen weten hoe goed die therapieën in de tumor hebben gewerkt. Tegenwoordig berust die beoordeling op pathologen die enorme digitale microscoopbeelden zorgvuldig met het blote oog onderzoeken. Deze studie introduceert een nieuw hulpmiddel op basis van kunstmatige intelligentie, MMT-Net, dat snel en nauwkeurig kan inschatten welk deel van een longtumor door de behandeling is vernietigd, wat de zorg mogelijk sneller, consistenter en persoonlijker maakt.
Waarom meten wat overblijft ertoe doet
Bij patiënten met niet-kleincellige longkanker gebruiken artsen vaak geneesmiddelen en bestraling vóór de operatie om de tumor te verkleinen of te verzwakken. Na de operatie schatten pathologen de “major pathological response” door te bepalen welk fractie van het tumorbed nog levende kankercellen bevat. Als slechts een klein deel — ongeveer een tiende of minder — overblijft, hebben patiënten meestal een betere overleving en uitkomsten. Moderne digitale slides kunnen echter miljarden pixels bevatten en therapie laat een verwarrende mix achter van dode weefsels, littekenachtige gebieden en verspreide overlevende cellen. Het handmatig beoordelen van deze enorme beelden is traag, uitputtend en gevoelig voor variatie tussen experts.
Computers leren kankerslides lezen
De onderzoekers bouwden MMT-Net om pathologen bij deze veeleisende taak te ondersteunen. Het systeem analyseert hele slide-afbeeldingen van longtumoren die al behandeld zijn. In plaats van te vertrouwen op standaard computer vision-modellen die op alledaagse foto’s zijn getraind, laten ze het netwerk eerst de visuele “taal” van de pathologie zelf aanleren met duizenden niet-gelabelde weefselfragmenten. Deze zelfgestuurde leervoorziening helpt het model subtiele patronen te herkennen die specifiek zijn voor gekleurde microscoopbeelden, in plaats van katten, auto’s of landschappen.
Op hetzelfde moment dichtbij en veraf kijken
MMT-Net bootst ook na hoe menselijke experts in- en uitzoomen bij het lezen van een slide. Het systeem neemt kleine afbeeldingspatches op drie vergrotingen: laag vermogen om de algemene architectuur vast te leggen, middelgroot om schadepatronen te zien, en hoog vermogen om individuele cellen te inspecteren. Een gespecialiseerde attentiemechaniek voegt deze beelden vervolgens samen, waardoor het model zowel fijne details als brede context kan wegen. Een transformermodule — oorspronkelijk ontwikkeld voor taalvertaling — gebruikt deze samengevoegde kenmerken om elke patch in drie categorieën in te delen: resterende levende tumor, therapiegerelateerd littekenachtig stroma, of dood en gekeratiniseerd materiaal. Door over de gehele slide op te tellen, schat MMT-Net het aandeel levende tumorcellen, de sleutelgrootheid die artsen gebruiken om de respons te beoordelen.
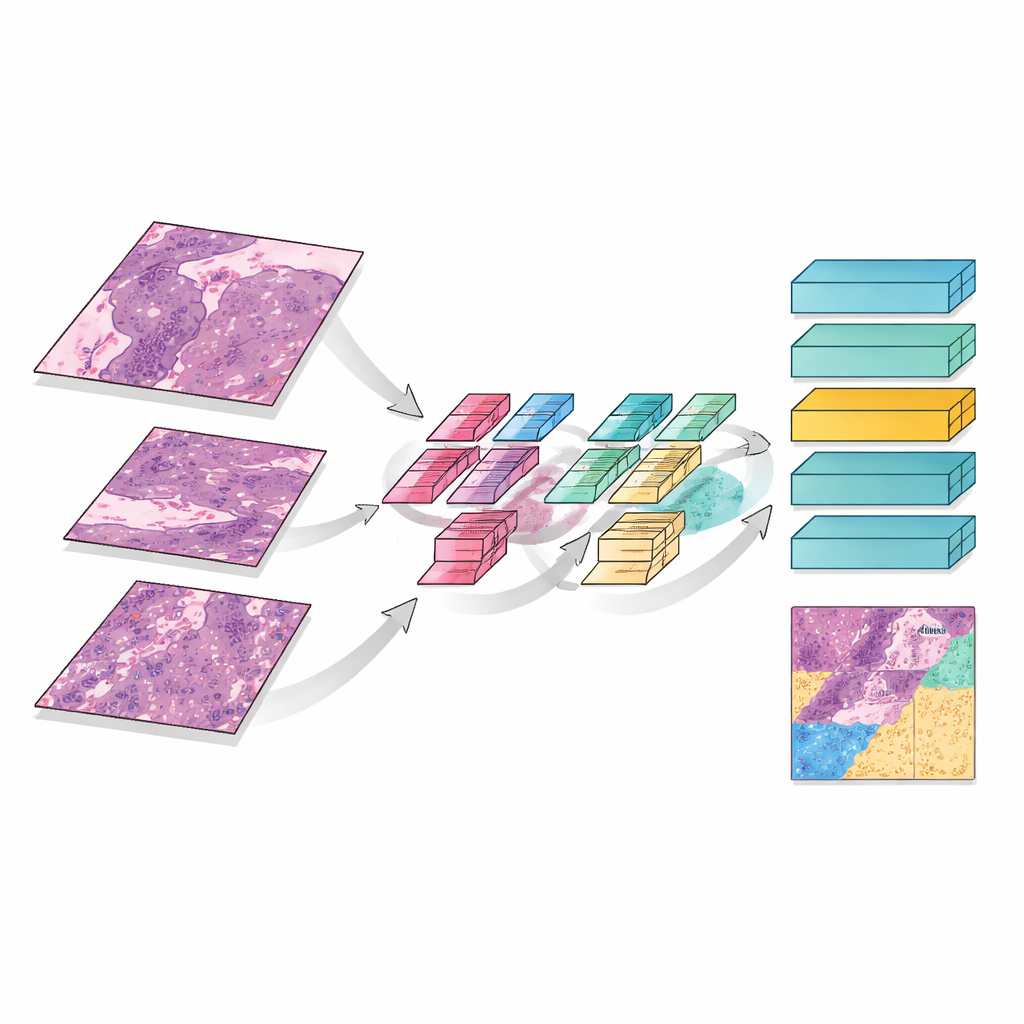
Hoe goed het systeem presteert
Om het model te testen gebruikte het team slides van 23 patiënten die behandeld waren in één kankercentrum. Ze verdeelden de gegevens in trainings- en testgroepen, waarbij expert-pathologen zorgvuldig gebieden van levensvatbare tumor, littekenachtig stroma en dood weefsel markeerden volgens internationale richtlijnen. Vergeleken met enkele toonaangevende deep learning-methoden behaalde MMT-Net de hoogste nauwkeurigheid en classificeerde het weefseltypen correct in ongeveer 99 procent van de testpatches wanneer het vooraf was getraind op pathologiebeelden. De gebieden die door de interne attentiekaarten van het model werden gemarkeerd, kwamen sterk overeen met de regio’s waarop menselijke specialisten zich richten, wat suggereert dat het systeem naar de juiste structuren “kijkt” en niet op toevallige aanwijzingen vertrouwt.
Vergelijking met moleculaire markers
Naast visuele vergelijking onderzochten de onderzoekers of de voorspellingen van MMT-Net overeenkomen met biologische maten van tumorgebruik. Ze bekeken extra slides die gekleurd waren voor twee veelgebruikte laboratoriummarkers: cytokeratines, die tumorcellen van epitheliale oorsprong oplichten, en Ki67, die delende cellen markeert. Het aandeel regio’s dat door het model als levensvatbare tumor werd aangemerkt, toonde een sterke statistische correlatie met beide markers, wat betekent dat waar de computer actieve tumor zag, de laboratoriummarkers dit bevestigden. Deze nauwe overeenkomst ondersteunt het idee dat MMT-Net echte aspecten van ziektebiologie vastlegt, en niet slechts oppervlakkige kleurverschillen.
Wat dit voor patiënten kan betekenen
Simpel gezegd toont deze studie aan dat een zorgvuldig ontworpen AI-systeem kan inschatten hoeveel longtumor overblijft na vooroperatieve behandeling bijna net zo goed als expert-pathologen, en op een manier die verklaarbaar en biologisch onderbouwd is. Hoewel het werk is uitgevoerd op een relatief kleine groep patiënten van één centrum en grotere multiziekenhuisstudies nog nodig zijn, is de aanpak flexibel en kan zij worden aangepast aan andere kankers en taken. In de toekomst kunnen tools zoals MMT-Net helpen standaardiseren hoe de respons op therapie wordt gemeten, betrouwbaardere beslissingen over vervolgbehandeling ondersteunen en precisiegeneeskunde dichter bij de dagelijkse klinische praktijk brengen.
Bronvermelding: Yang, C., Liu, L., Xiao, W. et al. Estimating major pathological response in non-small cell lung cancer patients with post-neoadjuvant therapy using MMT-net. Sci Rep 16, 14144 (2026). https://doi.org/10.1038/s41598-026-44633-y
Trefwoorden: longkanker, digitale pathologie, kunstmatige intelligentie, behandelingsrespons, deep learning