Clear Sky Science · fr
Estimation de la réponse pathologique majeure chez les patients atteints de cancer du poumon non à petites cellules après traitement néoadjuvant à l’aide de MMT-net
Aider les médecins à évaluer le succès du traitement
Lorsque des personnes atteintes d’un cancer du poumon reçoivent des traitements puissants avant la chirurgie, les médecins doivent savoir dans quelle mesure ces thérapies ont détruit la tumeur. Aujourd’hui, ce jugement repose sur des pathologistes qui examinent minutieusement d’immenses images numériques au microscope à l’œil nu. Cette étude présente un nouvel outil d’intelligence artificielle, nommé MMT-Net, qui peut estimer rapidement et précisément quelle part d’une tumeur pulmonaire a été détruite par le traitement, ce qui pourrait accélérer les soins, les rendre plus cohérents et plus personnalisés.
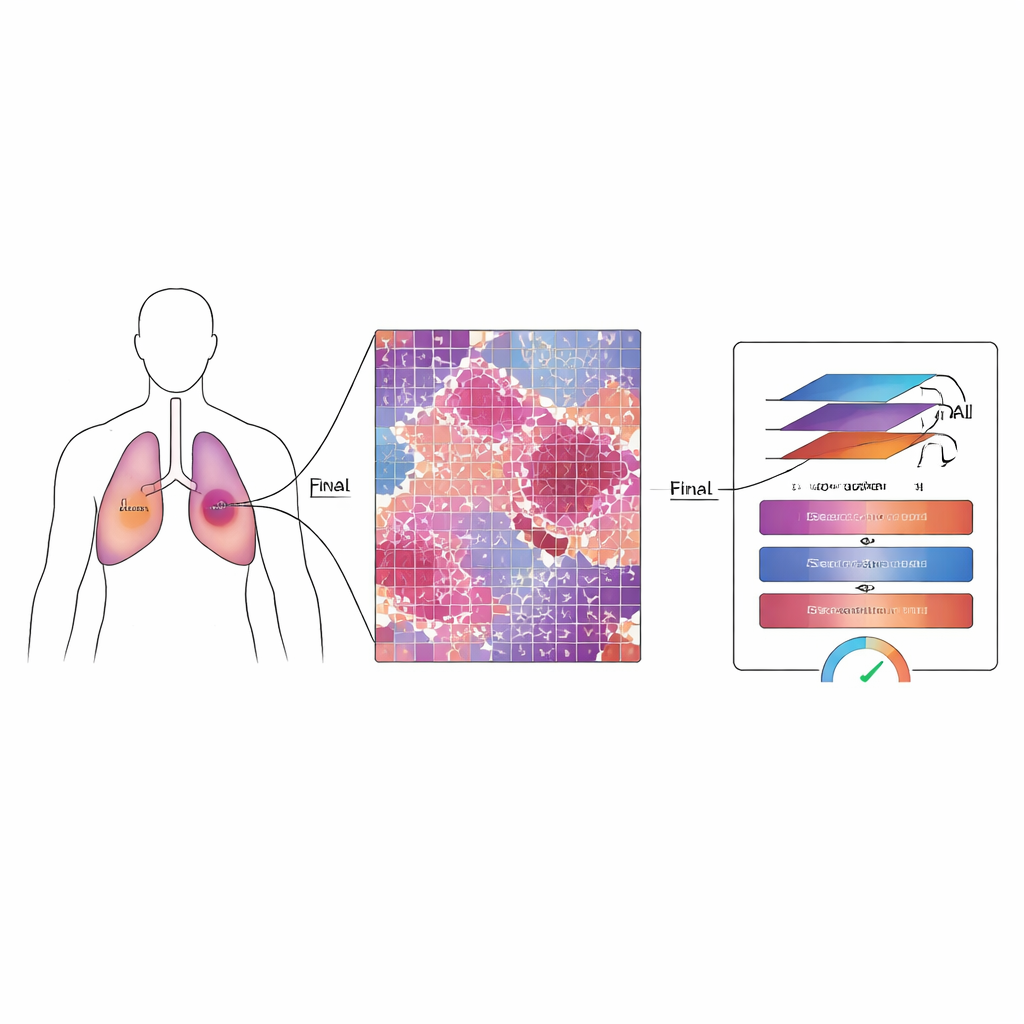
Pourquoi mesurer ce qui reste est important
Pour les patients atteints de cancer du poumon non à petites cellules, les médecins utilisent souvent des médicaments et la radiothérapie avant la chirurgie pour réduire ou affaiblir la tumeur. Après l’intervention, les pathologistes estiment la « réponse pathologique majeure » en vérifiant quelle fraction du lit tumoral contient encore des cellules cancéreuses vivantes. Si seule une petite quantité — environ un dixième ou moins — subsiste, les patients ont tendance à vivre plus longtemps et à mieux évoluer globalement. Cependant, les lames numériques modernes peuvent contenir des milliards de pixels, et la thérapeutique peut laisser un mélange trompeur de tissu nécrosé, de zones cicatricielles et de cellules survivantes éparses. L’examen manuel de ces images gigantesques est lent, épuisant et sujet à des variations entre experts.
Apprendre aux ordinateurs à lire les lames cancéreuses
Les chercheurs ont développé MMT-Net pour aider les pathologistes dans cette tâche exigeante. Le système analyse des lames entières de tumeurs pulmonaires déjà traitées. Plutôt que de s’appuyer sur des modèles de vision par ordinateur classiques entraînés sur des photos courantes, ils ont d’abord laissé le réseau s’auto-apprendre le « langage » visuel de la pathologie à partir de milliers de petits extraits de tissus non annotés. Cette étape d’apprentissage autodirigé aide le modèle à reconnaître des motifs subtils propres aux images colorées au microscope, plutôt qu’aux chats, voitures ou paysages.
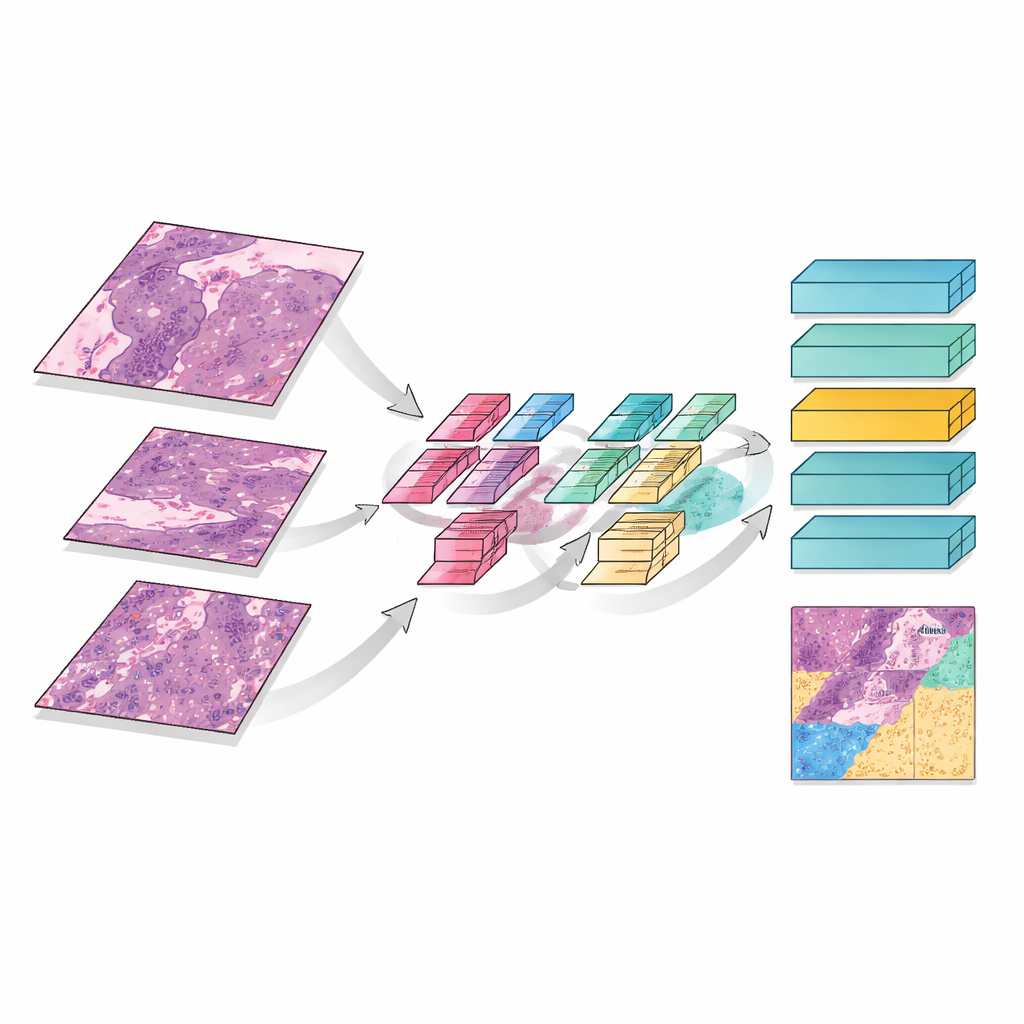
Regarder de près et de loin en même temps
MMT-Net imite également la façon dont les experts humains zooment et dézooment en lisant une lame. Le système extrait de petites fenêtres d’image à trois niveaux de grossissement : faible puissance pour capter l’architecture générale, puissance moyenne pour observer les motifs de lésion, et forte puissance pour inspecter les cellules individuelles. Un mécanisme d’attention spécialisé fusionne ensuite ces vues, permettant au modèle de pondérer ensemble les détails fins et le contexte global. Un module transformeur — initialement développé pour la traduction de langue — utilise ces caractéristiques fusionnées pour classer chaque patch en trois catégories : tumeur vivante résiduelle, tissu cicatriciel lié au traitement, ou matériau nécrotique/ kératinisé. En sommant sur l’ensemble de la lame, MMT-Net estime la fraction de cellules tumorales vivantes, la quantité clé utilisée par les médecins pour juger la réponse.
Performance du système
Pour évaluer le modèle, l’équipe a utilisé des lames provenant de 23 patients traités dans un seul centre de cancérologie. Ils ont séparé les données en ensembles d’entraînement et de test, des pathologistes experts ayant soigneusement marqué les régions de tumeur viable, le stroma cicatriciel et le tissu nécrosé selon des directives internationales. Comparé à plusieurs méthodes d’apprentissage profond de pointe, MMT-Net a obtenu la plus grande précision, classifiant correctement les types de tissus dans environ 99 % des patchs de test lorsqu’il était pré-entraîné sur des images de pathologie. Les zones mises en évidence par les cartes d’attention internes du modèle correspondaient étroitement aux régions sur lesquelles se concentrent les spécialistes humains, suggérant que le système « regarde » les bonnes structures plutôt que de s’appuyer sur des indices factices.
Vérification par des marqueurs moléculaires
Au-delà de la comparaison visuelle, les chercheurs ont vérifié si les prédictions de MMT-Net s’alignent avec des mesures biologiques de l’activité tumorale. Ils ont examiné des lames additionnelles colorées pour deux marqueurs de laboratoire courants : les cytokératines, qui mettent en évidence les cellules tumorales d’origine épithéliale, et Ki67, qui marque les cellules en division. La proportion de régions étiquetées comme tumeur viable par le modèle montrait une forte corrélation statistique avec ces deux marqueurs, ce qui signifie que là où l’ordinateur détectait une tumeur active, les colorations de laboratoire confirmaient. Cette concordance étroite soutient l’idée que MMT-Net capture des aspects réels de la biologie de la maladie, et non de simples différences superficielles de couleur.
Ce que cela pourrait signifier pour les patients
En termes simples, cette étude montre qu’un système d’IA soigneusement conçu peut estimer combien de tumeur pulmonaire subsiste après un traitement préopératoire presque aussi bien que des pathologistes experts, et d’une manière explicable et fondée biologiquement. Bien que le travail ait été réalisé sur un groupe relativement restreint de patients provenant d’un seul centre, et que des études plus larges multi-hospitalières soient encore nécessaires, l’approche est flexible et pourrait être adaptée à d’autres cancers et tâches. À l’avenir, des outils comme MMT-Net pourraient contribuer à standardiser la mesure de la réponse au traitement, soutenir des décisions de suivi plus fiables et rapprocher la médecine de précision de la pratique clinique quotidienne.
Citation: Yang, C., Liu, L., Xiao, W. et al. Estimating major pathological response in non-small cell lung cancer patients with post-neoadjuvant therapy using MMT-net. Sci Rep 16, 14144 (2026). https://doi.org/10.1038/s41598-026-44633-y
Mots-clés: cancer du poumon, pathologie numérique, intelligence artificielle, réponse au traitement, apprentissage profond