Clear Sky Science · pl
Szacowanie głównej odpowiedzi patologicznej u pacjentów z niedrobnokomórkowym rakiem płuca po terapii przedoperacyjnej za pomocą MMT-net
Pomoc lekarzom w ocenie skuteczności leczenia
Gdy osoby z rakiem płuca otrzymują silne terapie przed operacją, lekarze muszą ustalić, jak skuteczne były one wewnątrz guza. Obecnie ta ocena opiera się na patologach, którzy żmudnie przeglądają ogromne cyfrowe obrazy mikroskopowe wzrokowo. W tym badaniu przedstawiono nowe narzędzie sztucznej inteligencji, nazwane MMT-Net, które może szybko i precyzyjnie oszacować, jaka część guza płucnego została zniszczona przez terapię, co potencjalnie przyspiesza opiekę, zwiększa jej spójność i pozwala na większą personalizację.
Dlaczego ważne jest mierzenie, co pozostało
U pacjentów z niedrobnokomórkowym rakiem płuca lekarze często stosują leki i radioterapię przed zabiegiem, by zmniejszyć lub osłabić guz. Po operacji patolodzy oceniają „główną odpowiedź patologiczną”, sprawdzając, jaka część loża guza wciąż zawiera żywe komórki nowotworowe. Jeśli pozostaje tylko niewielka ilość — około jednej dziesiątej lub mniej — pacjenci mają tendencję do dłuższego przeżycia i lepszych wyników ogólnych. Jednak nowoczesne cyfrowe preparaty mogą zawierać miliardy pikseli, a terapia może pozostawić złożoną mieszankę martwej tkanki, obszarów przypominających bliznę i rozrzuconych żywych komórek. Ręczne przeglądanie tych ogromnych obrazów jest powolne, męczące i podatne na zmienność między ekspertami.
Nauczanie komputerów odczytywania preparatów nowotworowych
Badacze stworzyli MMT-Net, by wspierać patologów w tym wymagającym zadaniu. System analizuje całe skany preparatów guza płuca po terapii. Zamiast polegać na standardowych modelach wizji komputerowej trenowanych na codziennych zdjęciach, najpierw pozwolili sieci nauczyć się samodzielnie wizualnego „języka” patologii, wykorzystując tysiące nieoznakowanych fragmentów tkanki. Ten etap samodzielnego uczenia pomaga modelowi rozpoznawać subtelne wzory charakterystyczne dla barwionych obrazów mikroskopowych, a nie kotów, samochodów czy krajobrazów.
Patrzenie z bliska i z daleka jednocześnie
MMT-Net naśladuje także sposób, w jaki eksperci ludzie przybliżają i oddalają widok podczas przeglądania preparatu. System pobiera małe fragmenty obrazu w trzech powiększeniach: niskim, by uchwycić ogólną architekturę; średnim, by zobaczyć wzory uszkodzeń; i wysokim, by przyjrzeć się pojedynczym komórkom. Specjalizowany mechanizm uwagi łączy te widoki, pozwalając modelowi uwzględnić jednocześnie drobne detale i szeroki kontekst. Moduł transformera — pierwotnie opracowany do tłumaczeń językowych — wykorzystuje te zintegrowane cechy do zaklasyfikowania każdego fragmentu do trzech kategorii: pozostający żywy guz, bliznopodobne tkanki łącznej związane z leczeniem lub martwa i zrogowaciała materia. Sumując wyniki dla całego preparatu, MMT-Net szacuje udział żywych komórek nowotworowych, kluczową wielkość stosowaną przez lekarzy do oceny odpowiedzi.
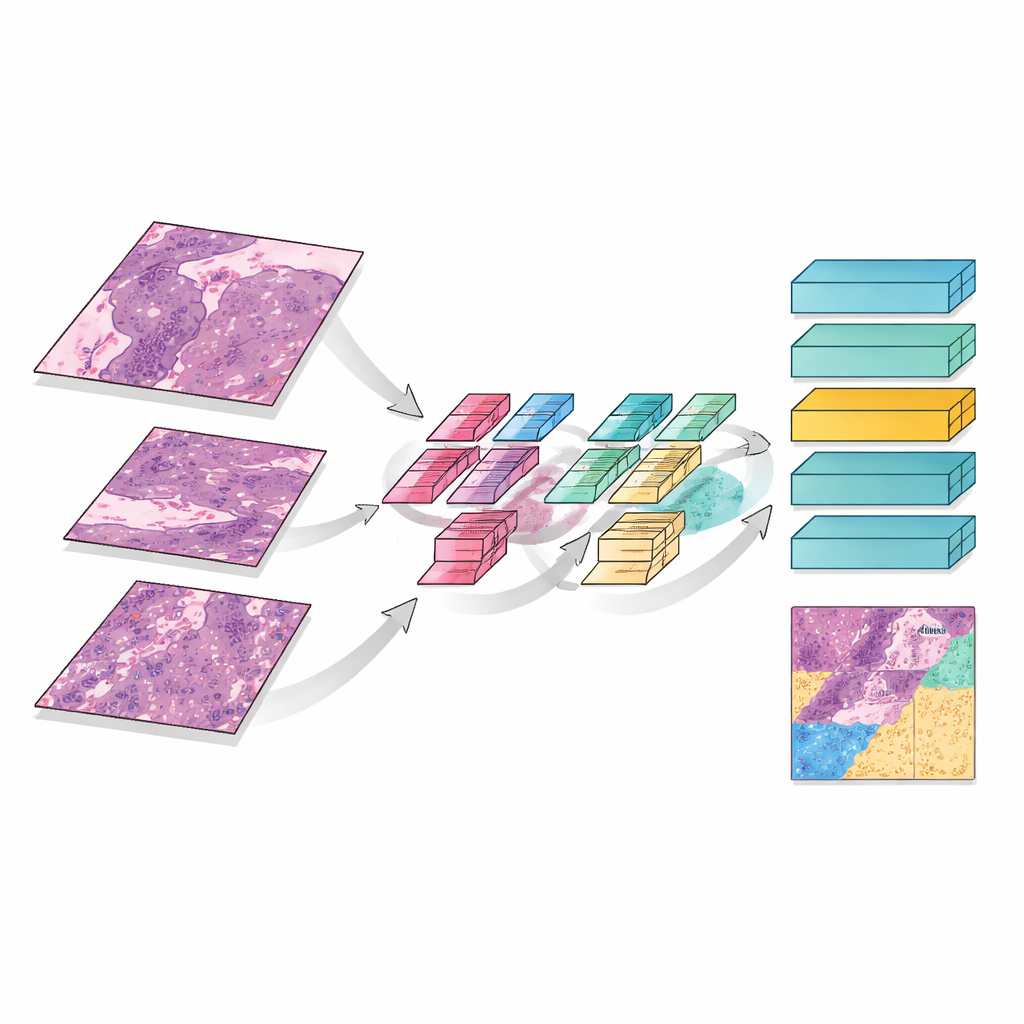
Jak dobrze działa system
Aby przetestować model, zespół wykorzystał preparaty od 23 pacjentów leczonych w jednym ośrodku onkologicznym. Dane podzielono na grupy treningowe i testowe, a doświadczeni patolodzy dokładnie oznaczyli obszary żywotnego guza, bliznopodobnego zrębu i martwej tkanki zgodnie z międzynarodowymi wytycznymi. W porównaniu z kilkoma czołowymi metodami uczenia głębokiego MMT-Net osiągnął najwyższą dokładność, prawidłowo klasyfikując typy tkanek w około 99 procentach testowych fragmentów, gdy był wstępnie wytrenowany na obrazach patologicznych. Obszary wyróżnione przez wewnętrzne mapy uwagi modelu ściśle pokrywały się z regionami, na które skupiają się ludzie‑specjaliści, co sugeruje, że system „patrzy” na właściwe struktury, zamiast polegać na przypadkowych wskazówkach.
Porównanie z markerami molekularnymi
Ponad porównaniem wizualnym badacze sprawdzili, czy przewidywania MMT-Net zgadzają się z biologicznymi miarami aktywności guza. Zbadali dodatkowe preparaty barwione pod kątem dwóch powszechnych markerów laboratoryjnych: cytokeratyn, które uwidaczniają komórki nowotworowe pochodzenia nabłonkowego, oraz Ki67, który oznacza komórki dzielące się. Udział regionów oznaczonych przez model jako żywy guz wykazywał silną korelację statystyczną z oboma markerami, co oznacza, że tam, gdzie komputer widział aktywny guz, barwienia laboratoryjne to potwierdzały. To bliskie dopasowanie wspiera tezę, że MMT-Net uchwycił rzeczywiste aspekty biologii choroby, a nie tylko powierzchowne różnice w kolorze.
Co to może znaczyć dla pacjentów
Mówiąc wprost, badanie pokazuje, że starannie zaprojektowany system AI może oszacować, ile guza płuca pozostaje po leczeniu przedoperacyjnym, niemal tak dobrze jak doświadczeni patolodzy, w sposób wytłumaczalny i osadzony biologicznie. Choć prace przeprowadzono na stosunkowo niewielkiej grupie pacjentów z jednego ośrodka i potrzebne są większe, wieloośrodkowe badania, podejście to jest elastyczne i mogłoby zostać dostosowane do innych nowotworów i zadań. W przyszłości narzędzia takie jak MMT-Net mogą pomóc ujednolicić sposób mierzenia odpowiedzi na terapię, wspierać bardziej wiarygodne decyzje dotyczące dalszego leczenia i przybliżyć medycynę precyzyjną do codziennej praktyki klinicznej.
Cytowanie: Yang, C., Liu, L., Xiao, W. et al. Estimating major pathological response in non-small cell lung cancer patients with post-neoadjuvant therapy using MMT-net. Sci Rep 16, 14144 (2026). https://doi.org/10.1038/s41598-026-44633-y
Słowa kluczowe: rak płuca, patologia cyfrowa, sztuczna inteligencja, odpowiedź na leczenie, uczenie głębokie