Clear Sky Science · es
Estimación de la respuesta patológica mayor en pacientes con cáncer de pulmón no microcítico tras terapia neoadyuvante usando MMT-net
Ayudando a los médicos a ver el éxito del tratamiento
Cuando las personas con cáncer de pulmón reciben terapias potentes antes de la cirugía, los médicos necesitan saber qué tan bien funcionaron esos tratamientos dentro del tumor. Hoy en día, ese juicio se basa en patólogos que examinan a fondo enormes imágenes digitales de microscopio a simple vista. Este estudio presenta una nueva herramienta de inteligencia artificial, llamada MMT-Net, que puede estimar rápida y con precisión cuánto del tumor pulmonar ha sido destruido por el tratamiento, lo que potencialmente puede hacer la atención más rápida, coherente y personalizada.
Por qué importa medir lo que queda
Para los pacientes con cáncer de pulmón no microcítico, los médicos a menudo usan fármacos y radiación antes de la cirugía para reducir o debilitar el tumor. Tras la intervención, los patólogos estiman la “respuesta patológica mayor” comprobando qué fracción del lecho tumoral aún contiene células cancerosas vivas. Si solo queda una pequeña cantidad —aproximadamente una décima parte o menos—, los pacientes suelen vivir más y tener mejores resultados. Sin embargo, las diapositivas digitales modernas pueden contener miles de millones de píxeles, y la terapia puede dejar una mezcla confusa de tejido muerto, zonas similares a cicatriz y células supervivientes dispersas. Revisar manualmente estas enormes imágenes es lento, agotador y propenso a variaciones entre expertos.
Enseñar a los ordenadores a leer placas de cáncer
Los investigadores construyeron MMT-Net para ayudar a los patólogos en esta tarea exigente. El sistema analiza imágenes de la placa completa de tumores pulmonares que ya han recibido tratamiento. En lugar de confiar en modelos estándar de visión por ordenador entrenados con fotos cotidianas, primero permiten que la red aprenda por sí misma el “lenguaje” visual de la patología usando miles de fragmentos de tejido no etiquetados. Este paso de aprendizaje autodirigido ayuda al modelo a reconocer patrones sutiles específicos de imágenes teñidas de microscopio, en lugar de gatos, coches o paisajes.
Mirar de cerca y de lejos al mismo tiempo
MMT-Net también imita cómo los expertos humanos aumentan y reducen el zoom mientras leen una placa. El sistema toma pequeños fragmentos de imagen en tres aumentos: baja potencia para capturar la arquitectura general, media para ver patrones de daño y alta para inspeccionar células individuales. Un mecanismo de atención especializado fusiona estas vistas, permitiendo que el modelo pese los detalles finos y el contexto amplio conjuntamente. Un módulo transformer —desarrollado originalmente para traducción de lenguaje— usa estas características fusionadas para clasificar cada fragmento en tres categorías: tumor vivo restante, tejido cicatricial relacionado con el tratamiento, o material muerto y queratinizado. Al sumar sobre toda la diapositiva, MMT-Net estima la fracción de células tumorales vivas, la cantidad clave que los médicos usan para juzgar la respuesta.
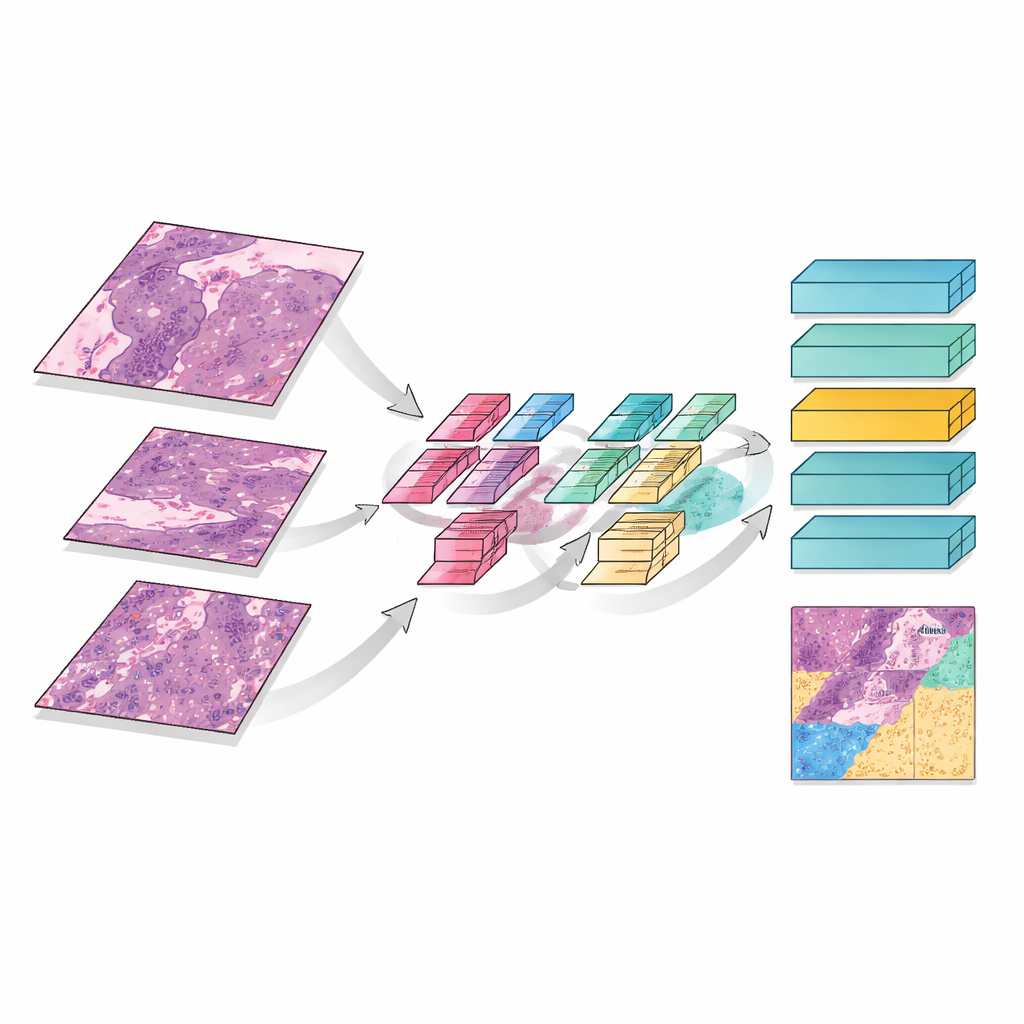
Qué tan bien funciona el sistema
Para evaluar el modelo, el equipo usó diapositivas de 23 pacientes tratados en un único centro oncológico. Dividieron los datos en grupos de entrenamiento y prueba, con patólogos expertos marcando cuidadosamente regiones de tumor viable, estroma similar a cicatriz y tejido muerto según guías internacionales. En comparación con varios métodos líderes de aprendizaje profundo, MMT-Net alcanzó la mayor precisión, clasificando correctamente los tipos de tejido en aproximadamente el 99 por ciento de los fragmentos de prueba cuando se preentrenó con imágenes de patología. Las áreas destacadas por los mapas de atención internos del modelo coincidieron estrechamente con las regiones en las que se enfocan los especialistas humanos, lo que sugiere que el sistema está “mirando” las estructuras correctas en lugar de basarse en señales espurias.
Comprobación con marcadores moleculares
Más allá de la comparación visual, los investigadores preguntaron si las predicciones de MMT-Net se alinean con medidas biológicas de la actividad tumoral. Examinaron diapositivas adicionales teñidas para dos marcadores de laboratorio comunes: citoqueratinas, que resaltan células tumorales de origen epitelial, y Ki67, que marca células en división. La proporción de regiones etiquetadas como tumor viable por el modelo mostró una fuerte correlación estadística con ambos marcadores, lo que significa que donde el ordenador veía tumor activo, las tinciones de laboratorio coincidían. Esta estrecha concordancia respalda la idea de que MMT-Net está capturando aspectos reales de la biología de la enfermedad, no solo diferencias superficiales de color.
Qué podría significar esto para los pacientes
En términos simples, este estudio muestra que un sistema de IA cuidadosamente diseñado puede estimar cuánto tumor pulmonar queda después del tratamiento preoperatorio casi tan bien como los patólogos expertos, y de una forma que es explicable y con base biológica. Aunque el trabajo se realizó en un grupo relativamente pequeño de pacientes de un único centro y aún se necesitan estudios más amplios en varios hospitales, el enfoque es flexible y podría adaptarse a otros cánceres y tareas. En el futuro, herramientas como MMT-Net podrían ayudar a estandarizar cómo se mide la respuesta al tratamiento, respaldar decisiones más fiables sobre el tratamiento de seguimiento y acercar la medicina de precisión a la práctica clínica cotidiana.
Cita: Yang, C., Liu, L., Xiao, W. et al. Estimating major pathological response in non-small cell lung cancer patients with post-neoadjuvant therapy using MMT-net. Sci Rep 16, 14144 (2026). https://doi.org/10.1038/s41598-026-44633-y
Palabras clave: cáncer de pulmón, patología digital, inteligencia artificial, respuesta al tratamiento, aprendizaje profundo