Clear Sky Science · de
Schätzung des major pathological response bei Patienten mit nicht‑kleinzelligem Lungenkrebs nach neoadjuvanter Therapie mittels MMT‑Net
Ärzten helfen, den Behandlungserfolg zu erkennen
Wenn Menschen mit Lungenkrebs vor einer Operation intensive Therapien erhalten, müssen Ärztinnen und Ärzte wissen, wie gut diese Behandlungen im Tumor gewirkt haben. Heute beruht diese Einschätzung auf Pathologinnen und Pathologen, die riesige digitale Mikroskopbilder mühsam mit dem Auge untersuchen. Diese Studie stellt ein neues Werkzeug der künstlichen Intelligenz vor, genannt MMT‑Net, das schnell und präzise abschätzen kann, wie viel eines Lungentumors durch die Behandlung zerstört wurde. Das könnte die Versorgung beschleunigen, konsistenter machen und individueller gestalten.
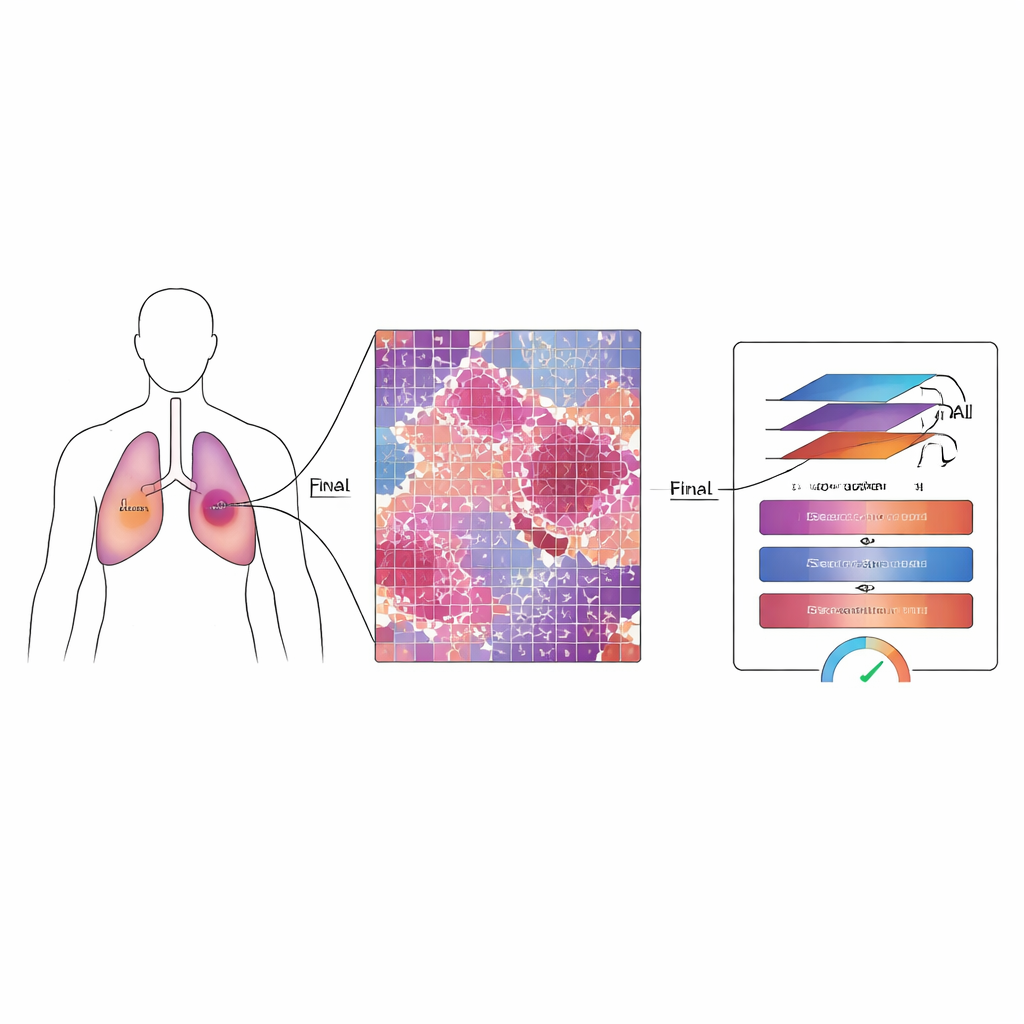
Warum es wichtig ist, das Verbleibende zu messen
Bei Patientinnen und Patienten mit nicht‑kleinzelligem Lungenkrebs werden häufig vor der Operation Medikamente und Strahlung eingesetzt, um den Tumor zu verkleinern oder zu schwächen. Nach der Operation schätzen Pathologinnen und Pathologen die „major pathological response“ ein, indem sie prüfen, welcher Anteil des Tumorbettes noch lebende Krebszellen enthält. Bleibt nur eine geringe Menge – etwa ein Zehntel oder weniger – übrig, haben Patientinnen und Patienten tendenziell eine längere Überlebenszeit und bessere Gesamtprognosen. Moderne digitale Präparate können jedoch Milliarden von Pixeln enthalten, und die Therapie hinterlässt oft ein verwirrendes Gemisch aus abgestorbenem Gewebe, narbenähnlichen Bereichen und verstreut überlebenden Zellen. Das manuelle Durchsehen dieser enormen Bilder ist langsam, ermüdend und anfällig für Unterschiede zwischen Expertinnen und Experten.
Computern beibringen, Krebspräparate zu lesen
Die Forschenden entwickelten MMT‑Net, um Pathologinnen und Pathologen bei dieser anspruchsvollen Aufgabe zu unterstützen. Das System analysiert Ganzscheibenbilder von bereits behandelten Lungentumoren. Anstatt auf Standard‑Computer‑Vision‑Modelle zu setzen, die mit Alltagsfotos trainiert wurden, lässt das Team das Netzwerk zunächst die visuelle „Sprache“ der Pathologie selbst erlernen, indem es tausende unlabeled Gewebe‑Schnipsel verwendet. Dieser selbstgesteuerte Lernschritt hilft dem Modell, subtile Muster zu erkennen, die spezifisch für gefärbte Mikroskopbilder sind – nicht für Katzen, Autos oder Landschaften.
Gleichzeitig nah und fern betrachten
MMT‑Net ahmt außerdem nach, wie menschliche Expertinnen und Experten beim Lesen einer Präparatscheibe hinein- und herauszoomen. Das System verarbeitet kleine Bildausschnitte in drei Vergrößerungsstufen: niedrige Vergrößerung, um die Gesamtarchitektur zu erfassen, mittlere, um Schadensmuster zu sehen, und hohe, um einzelne Zellen zu inspizieren. Ein spezieller Attention‑Mechanismus verschmilzt diese Betrachtungsweisen, sodass das Modell feine Details und großen Kontext gemeinsam gewichten kann. Ein Transformer‑Modul – ursprünglich für Sprachübersetzung entwickelt – verwendet diese fusionierten Merkmale, um jeden Ausschnitt in drei Kategorien einzuteilen: verbleibender lebender Tumor, therapiebedingtes narbenähnliches Stroma oder abgestorbenes/keratinisiertes Material. Indem es über die gesamte Scheibe aufsummiert, schätzt MMT‑Net den Anteil lebender Tumorzellen, die entscheidende Größe, mit der Ärztinnen und Ärzte das Ansprechen beurteilen.
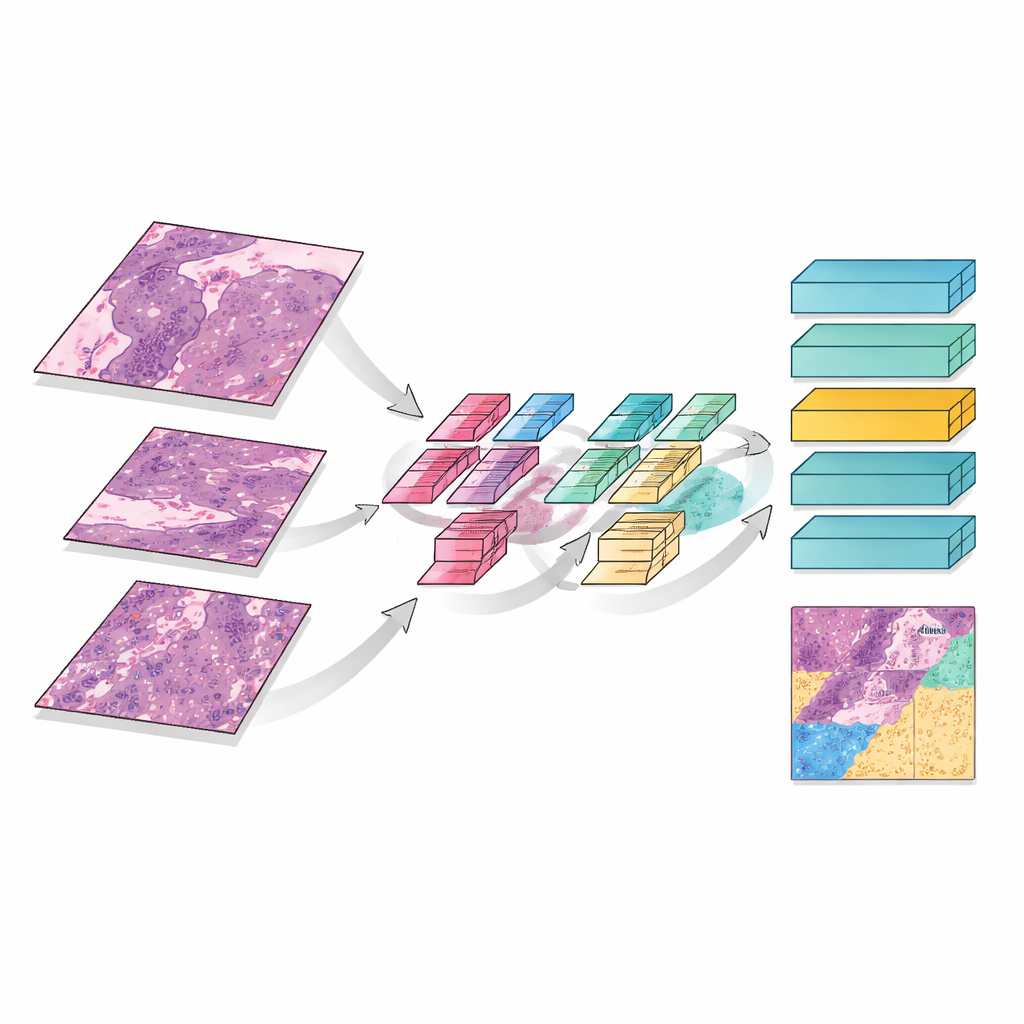
Wie gut das System arbeitet
Um das Modell zu testen, nutzte das Team Präparate von 23 Patientinnen und Patienten, die an einem einzelnen Krebszentrum behandelt worden waren. Die Daten wurden in Trainings‑ und Testgruppen aufgeteilt; Expertinnen und Experten markierten sorgfältig Bereiche mit vitalem Tumor, narbenähnlichem Stroma und totem Gewebe gemäß internationalen Richtlinien. Im Vergleich zu mehreren führenden Deep‑Learning‑Methoden erreichte MMT‑Net die höchste Genauigkeit und klassifizierte Gewebetypen in etwa 99 Prozent der Testausschnitte korrekt, wenn das Modell vorab auf Pathologie‑Bildern vortrainiert worden war. Die vom Modell hervorgehobenen Bereiche in seinen internen Attention‑Karten stimmten eng mit den Regionen überein, auf die menschliche Spezialistinnen und Spezialisten achten – ein Hinweis darauf, dass das System die richtigen Strukturen betrachtet und sich nicht auf zufällige Hinweise stützt.
Abgleich mit molekularen Markern
Über den visuellen Vergleich hinaus prüften die Forschenden, ob die Vorhersagen von MMT‑Net mit biologischen Maßen der Tumoraktivität übereinstimmen. Sie untersuchten zusätzliche Präparate, die für zwei gängige Labor‑Marker gefärbt waren: Cytokeratine, die Tumorzellen epithelialen Ursprungs hervorheben, und Ki67, das sich teilende Zellen markiert. Der Anteil der vom Modell als vitaler Tumor klassifizierten Regionen zeigte eine starke statistische Korrelation mit beiden Markern, was bedeutet, dass dort, wo der Computer aktiven Tumor sah, die Laborfärbungen dies bestätigten. Diese enge Übereinstimmung stützt die Idee, dass MMT‑Net reale biologische Aspekte der Erkrankung erfasst und nicht nur oberflächliche Farbunterschiede.
Was das für Patientinnen und Patienten bedeuten könnte
Einfach ausgedrückt zeigt diese Studie, dass ein sorgfältig entwickeltes KI‑System abschätzen kann, wie viel Lungentumor nach einer präoperativen Behandlung verbleibt – nahezu so gut wie Expertinnen und Experten der Pathologie – und zwar auf eine erklärbare und biologisch fundierte Weise. Obwohl die Arbeit an einer vergleichsweise kleinen Patientengruppe aus einem einzelnen Zentrum durchgeführt wurde und größere multizentrische Studien noch nötig sind, ist der Ansatz flexibel und könnte auf andere Krebsarten und Aufgaben adaptiert werden. Zukünftig könnten Werkzeuge wie MMT‑Net dabei helfen, die Messung des Therapieansprechens zu standardisieren, verlässlichere Entscheidungen über Folgebehandlungen zu unterstützen und die präzisionsmedizinische Praxis näher an den klinischen Alltag zu bringen.
Zitation: Yang, C., Liu, L., Xiao, W. et al. Estimating major pathological response in non-small cell lung cancer patients with post-neoadjuvant therapy using MMT-net. Sci Rep 16, 14144 (2026). https://doi.org/10.1038/s41598-026-44633-y
Schlüsselwörter: Lungenkrebs, digitale Pathologie, künstliche Intelligenz, Therapieansprechen, Deep Learning