Clear Sky Science · he
הערכת תגובה פתולוגית משמעותית בחולי סרטן ריאות לא־תאוני לאחר טיפול נאו־אדג'ובנטי באמצעות MMT-Net
סיוע לרופאים לראות את הצלחת הטיפול
כאשר מטופלים עם סרטן ריאות מקבלים טיפולים רבי עוצמה לפני ניתוח, הרופאים צריכים לדעת עד כמה הטיפולים פגעו בגידול. כיום שיפוט זה מתבסס על פתולוגים הבוחנים בזהירות תמונות מיקרוסקופ דיגיטליות עצומות בעין. מחקר זה מציג כלי חדש של בינה מלאכותית, בשם MMT‑Net, שיכול להעריך במהירות ובדייקנות עד כמה חלק מהגידול הריאתי נהרס על ידי הטיפול, עם פוטנציאל להאיץ את הטיפול, להפוך אותו לעקבי יותר ולהתאים אותו אישית.
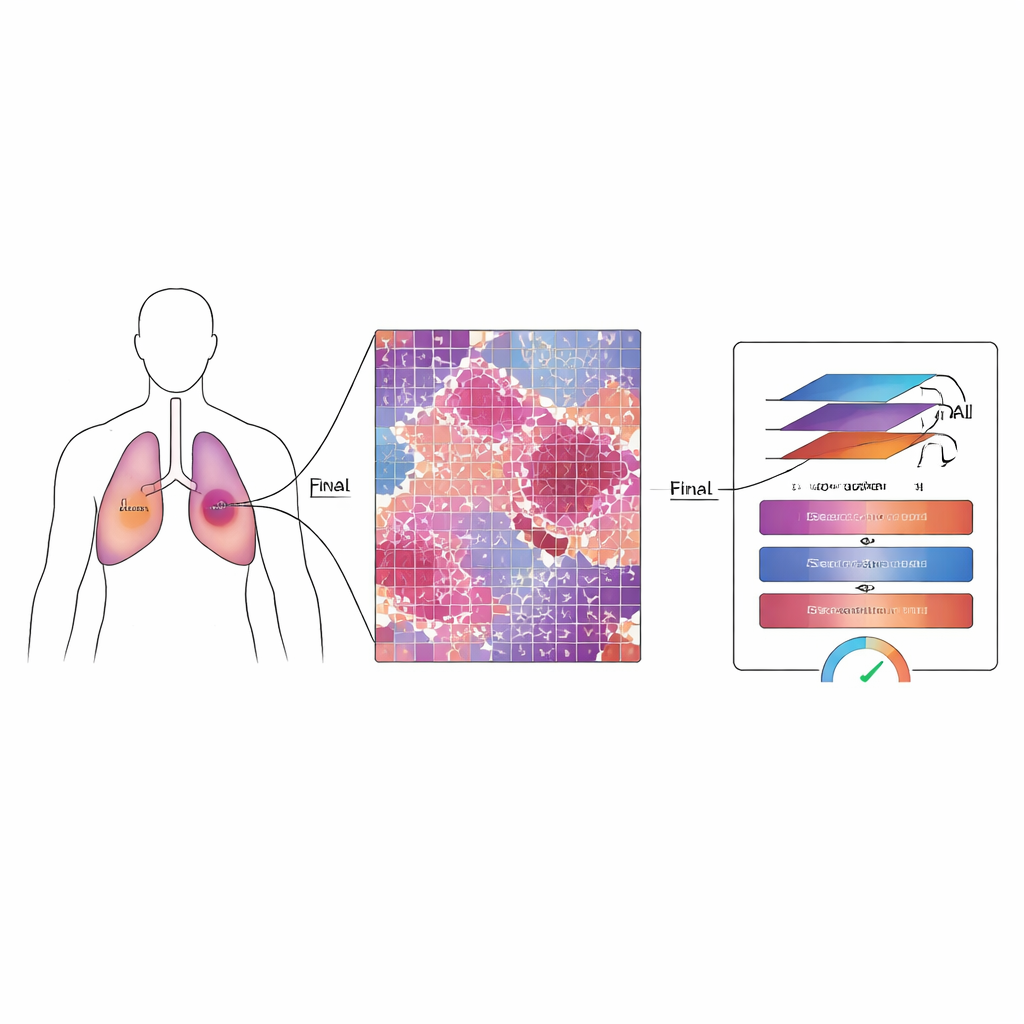
למה חשוב למדוד מה נשאר
במטופלים עם סרטן ריאות לא‑תאוני, רופאים לעתים משתמשים בתרופות ובקרינה לפני הניתוח כדי להקטין או להחליש את הגידול. לאחר ניתוח, פתולוגים מעריכים את ה"תגובה הפתולוגית העיקרית" על‑ידי בדיקת החלק מהמיטת הגידול שעוד מכיל תאים סרטניים חיים. אם נותר רק חלק קטן — בערך עשירית או פחות — המטופלים נוטים לשרוד זמן רב יותר ולהשיג תוצאות טובות יותר בסך הכל. עם זאת, פרוסות דיגיטליות מודרניות יכולות להכיל מיליארדי פיקסלים, והטיפול עלול להשאיר תערובת מבלבלת של רקמה מתה, אזורים צלקתיים ותאים ששרדו מפוזרים. בדיקה ידנית של תמונות עצומות אלה איטית, מתישה ורגישה לשונות בין מומחים.
ללמד מחשבים לקרוא פרוסות סרטניות
החוקרים בנו את MMT‑Net כדי לסייע לפתולוגים במשימה התובענית הזו. המערכת מנתחת תמונות של פרוסות שלמות של גידולים ריאתיים שטופלו כבר. במקום להסתמך על מודלים סטנדרטיים של ראיית מחשב שאומנו על תמונות יום‑יום, הם אפשרו לרשת ללמוד בעצמה את "שפת" הוויזואליה הפתולוגית באמצעות אלפי חתיכות רקמה שאינן מתויגות. שלב למידה עצמי זה מסייע לדגם לזהות דפוסים עדינים המיוחדים לתמונות מיקרוסקופיות מוכללות, במקום לחפש חתולים, מכוניות או נופים.
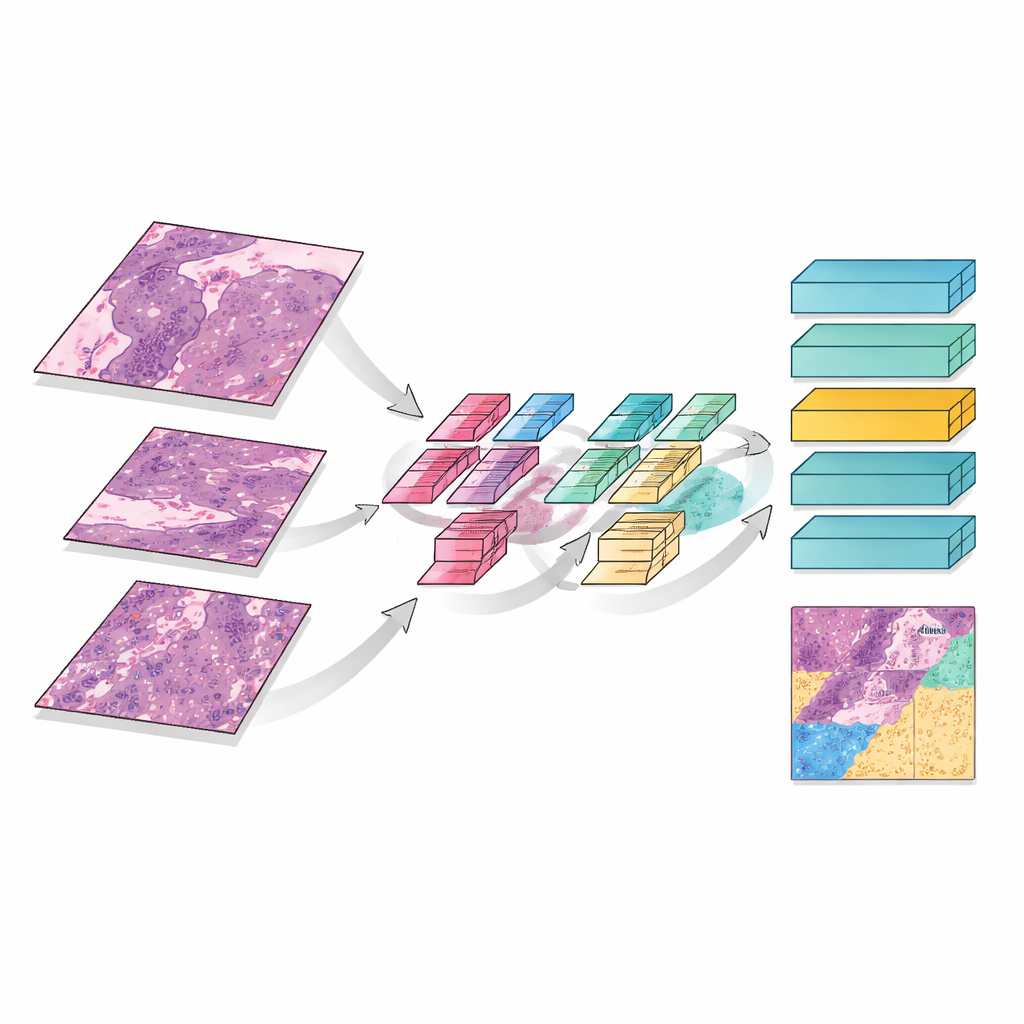
להסתכל קרוב ורחוק בו‑זמנית
MMT‑Net מדמה גם את האופן שבו מומחים בני אדם מגדילים ומקטינים בזמן קריאת פרוסה. המערכת לוקחת חתיכות תמונה קטנות בשלוש הגדלות: כוח נמוך לתפיסת מבנה כללי, בינוני כדי לראות דפוסי נזק, וכוח גבוה כדי לבחון תאים בודדים. מנגנון תשומת לב מיוחד מאחד אזורי תצפית אלה, ומאפשר לדגם לשקלל יחד פרטים זעירים והקשר רחב. מודול טרנספורמר — שפותח במקור לתרגום שפה — משתמש בתכונות המאוחדות כדי למיין כל חתיכה לשלוש קטגוריות: גידול חי ששרד, רקמת צלקת הקשורה לטיפול, או חומר מת ומיקרוטורי. על‑ידי סכימת כל החתיכות בכל הפרוסה, MMT‑Net מעריך את החלק של תאי גידול חיים, הכמות המכרעת שהרופאים משתמשים בה להערכת התגובה.
עד כמה המערכת מדויקת
לבדיקת המודל השתמשה הצוות בפרוסות מ‑23 מטופלים שטופלו במרכז סרטן בודד. הם חילקו את הנתונים לקבוצות אימון ובדיקה, כאשר פתולוגים מומחים סומנו בקפידה אזורים של גידול חי, רקמת מזנכימה דמויית צלקת ורקמה מתה לפי הנחיות בינלאומיות. בהשוואה למספר שיטות למידה עמוקה מובילות, MMT‑Net השיג את הדיוק הגבוה ביותר, וסיווג נכון של סוגי רקמה בכ‑99 אחוזים מהחתיכות בבדיקות כאשר תוכנן מוקדם על תמונות פתולוגיות. האזורים שהודגמו במפות התשומת לב הפנימיות של המודל התאימו במידה רבה לאזורים שבם התמקדו המומחים האנושיים, מה שמשמעותו שהמערכת "מסתכלת" על המבנים הנכונים במקום להסתמך על רמזים מקריים.
בדיקה מול סמנים מולקולאריים
מעבר להשוואה ויזואלית, החוקרים שאלו האם תחזיות MMT‑Net תואמות מדדים ביולוגיים לפעילות הגידול. הם בחנו פרוסות נוספות צבועות לשני סמנים מעבדתיים נפוצים: ציטוקרטינים, שמדגישים תאי גידול ממקור אפיתליאלי, ו‑Ki67, שמסמן תאים בתהליך חלוקה. השיעור של האזורים שסווגו על‑ידי המודל כגידול חי הראה מתאם סטטיסטי חזק עם שני הסמנים, כלומר היכן שהמחשב זיהה גידול פעיל, הצבעות המעבדה אישרו זאת. התאמה צמודה זו תומכת ברעיון ש‑MMT‑Net לוכד היבטים ביולוגיים ממשיים של המחלה, לא רק הבדלי צבע שטחיים.
מה זה עשוי לומר למטופלים
במלים פשוטות, מחקר זה מראה שמערכת AI שעוצבה בקפידה יכולה להעריך כמה גידול ריאתי נותר לאחר טיפול לפני ניתוח כמעט ברמת מומחיות של פתולוגים, ובאופן שניתן להסבירו ובעל יסוד ביולוגי. בעוד העבודה בוצעה על קבוצת מטופלים יחסית קטנה ממרכז יחיד ועדיין דרושים מחקרים רחבים בריבוי‑בתי‑חולים, הגישה גמישה וניתנת להתאמה לסוגי סרטן ומשימות אחרות. בעתיד, כלים כמו MMT‑Net עשויים לסייע להנחיל סטנדרט למדידת תגובה לטיפול, לתמוך בקבלת החלטות מהימנה יותר לגבי טיפול המשך, ולהקרב את הרפואה המדויקת לפרקטיקה הקלינית השוטפת.
ציטוט: Yang, C., Liu, L., Xiao, W. et al. Estimating major pathological response in non-small cell lung cancer patients with post-neoadjuvant therapy using MMT-net. Sci Rep 16, 14144 (2026). https://doi.org/10.1038/s41598-026-44633-y
מילות מפתח: סרטן ריאות, פתולוגיה דיגיטלית, בינה מלאכותית, תגובה לטיפול, למידה עמוקה