Clear Sky Science · sv
En deep‑SVM‑hybridramverk med förbättrad EEG‑feature‑engineering och SHAP‑baserad förklarbarhet för klassificering av Alzheimers
Varför hjärnvågstester kan upptäcka demens tidigare
Demens, inklusive Alzheimers sjukdom och frontotemporal demens, ökar globalt, samtidigt som dagens diagnostiska verktyg ofta är dyra, invasiva eller svåra att upprepa regelbundet. Denna studie undersöker om enkla hjärnvågsinspelningar, tagna med en elektroencefalografi (EEG)‑mössa, kan hjälpa läkare att skilja mellan olika demenstyper och normal åldrande. Forskarna fokuserar också på att göra datorns beslut begripliga för kliniker, så att systemet inte bara är noggrant utan också transparent och trovärdigt.
Lyssna på hjärnan utan operation
EEG mäter mycket små elektriska signaler från skalpen när grupper av hjärnceller avfyrar tillsammans. Dessa signaler förändras när demens utvecklas: snabbare rytmer tenderar att försvagas, långsammare rytmer blir starkare och kommunikationen mellan hjärnregioner kan försämras. Till skillnad från hjärnavbildning eller lumbalpunktion är EEG icke‑invasivt, relativt billigt och kan upprepas så ofta som behövs. Det gör det till en attraktiv kandidat för storskalig screening och rutinuppföljning, förutsatt att vi kan avkoda de komplexa, brusiga mönstren i vågorna på ett tillförlitligt sätt.
Blanda mänsklig insikt med maskininlärning
Teamet utformade ett hybriddatorsystem som kombinerar två typer av information från varje 4‑sekunders EEG‑segment. Först konstruerade de "handgjorda" features som neurovetare redan vet är kopplade till demens, såsom hur starka olika frekvensband är (långsamma delta och theta, snabbare alfa och beta), hur oförutsägbar spektrat är och hur väl vänster och höger hjärnhalva är synkroniserade i alfa‑bandet. För det andra tränade de ett kompakt endimensionellt konvolutionellt neuralt nätverk för att automatiskt lära sig användbara tidsmässiga mönster direkt från de rensade signalerna. Dessa två feature‑strömmar standardiseras, sammanslås till en enda representation och komprimeras sedan till ett mindre komponentset för att undvika redundans.
Noga hantering av begränsade patientdata
Huvuddatamängden bestod av vila‑EEG från 88 vuxna—personer med Alzheimers sjukdom, personer med frontotemporal demens och kognitivt normala frivilliga—insamlade under konsekventa inspelningsförhållanden. Eftersom antalet frivilliga är måttligt tog forskarna särskild omsorg för att undvika att överskatta prestanda. De delade upp data per person, inte per individuellt EEG‑segment, så en deltagares hjärnvågor förekom aldrig både i träning och test. Inom varje träningssätt balanserade de klasserna med en kontrollerad oversampling‑metod, normaliserade features och ställde in modellparametrar såsom hur många huvudkomponenter som skulle behållas och hur starkt slutklassificeraren skulle regulariseras. Denna nästlade utvärderingsdesign minskar kraftigt risken för "läckage" och överoptimistiska resultat.
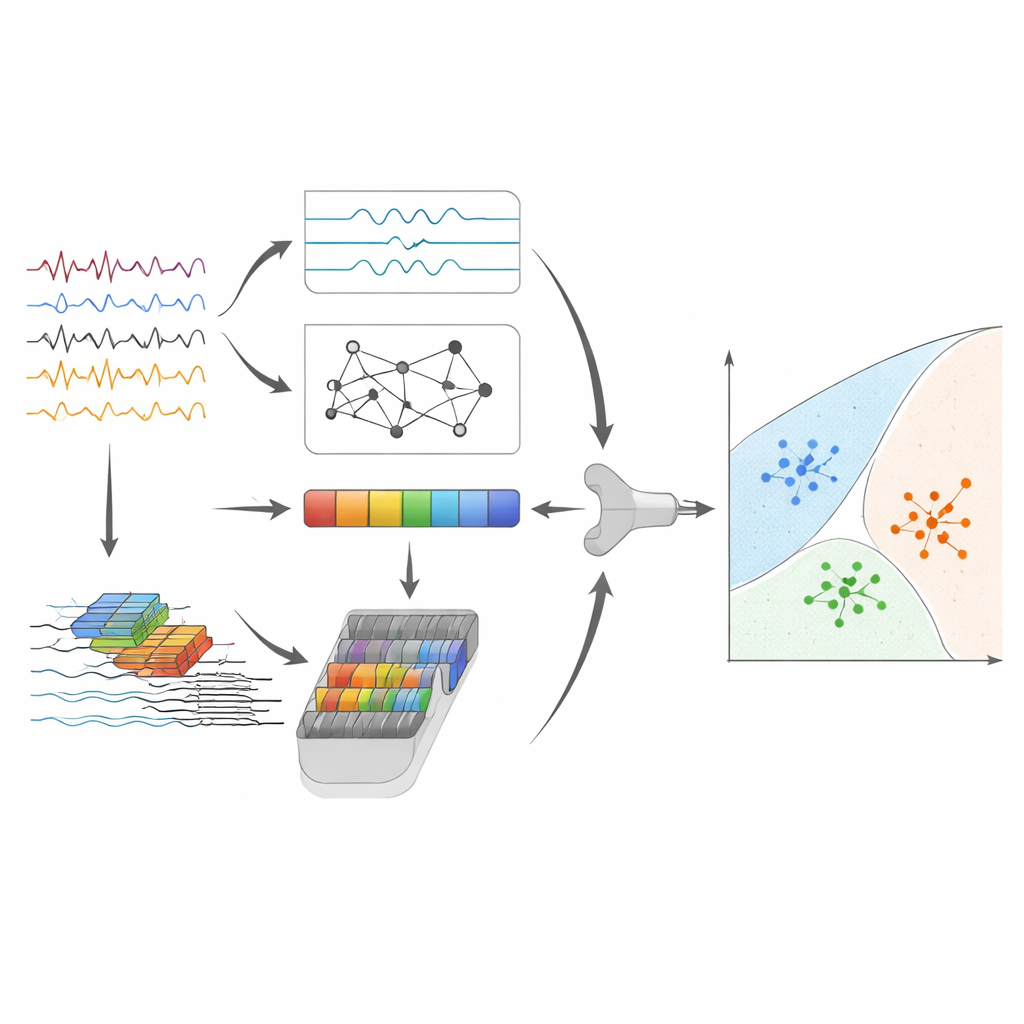
Hög noggrannhet och insikter i vad modellen ser
Efter feature‑fusion och kompression används i sista steget en supportvektormaskin, en klassisk algoritm som drar separerande gränser mellan punktgrupper i feature‑rymden. På huvuddatamängden särskilde denna hybridpipeline korrekt Alzheimers sjukdom, frontotemporal demens och normalt åldrande i ungefär 95 % av EEG‑segmenten, med lika stark prestanda över de tre grupperna. För att pröva hur väl metoden kan hålla i nya situationer tillämpade författarna den också, utan större omdesign, på hjärnvågor från samma personer inspelade med öppna ögon och på en helt oberoende datamängd inspelad med annan utrustning och andra demografiska förhållanden. Medan prestandan naturligtvis sjönk visade systemet ändå meningsfull diskriminering, vilket tyder på att det fångar sjukdomsrelaterade mönster snarare än egenheter i enskilda studier.
Öppna svart lådan för kliniker
Utöver noggrannhet är ett centralt mål med arbetet förklarbarhet: läkare behöver se varför en algoritm lutar åt en viss diagnos. Forskarna använde en metod kallad SHAP för att uppskatta hur mycket varje feature "pushar" modellen mot eller bort från en given klass. Genom att gruppera dessa bidrag i enkla enheter—som specifika frekvensband och hjärnregioner—producerade de sammanfattningar som liknar traditionella EEG‑rapporter. Mönster som ökade sannolikheten för Alzheimers eller frontotemporal demens inkluderade starkare långsam theta‑aktivitet över frontala områden, svagare alfa‑rytmer i bakre regioner och minskad alfa‑bandskoordination mellan hemisfärerna, vilket stämmer med årtionden av kliniska EEG‑observationer.
Vad detta betyder för patienter och kliniker
I praktiska termer visar studien att ett omsorgsfullt utformat EEG‑baserat system kan hjälpa till att särskilja två stora demenstyper från varandra och från normalt åldrande med hög tillförlitlighet, samtidigt som det förklarar sin slutsats i välkända fysiologiska termer. Om det valideras på större, multicenter‑kohorter skulle sådana verktyg kunna stödja tidigare och mer precis diagnostik med prisvärd utrustning, och kunna integreras i klinikvänliga instrumentpaneler som visar riskuppskattningar och de hjärnvågsfeatures som driver dem. Istället för att ersätta kliniker är tillvägagångssättet avsett att fungera som ett andra par ögon—framlyftande subtila förändringar i hjärnaktivitet som kan signalera när vidare utredning eller tätare uppföljning är motiverad.
Citering: Akbar, F., Alkhrijah, Y., Usman, S.M. et al. A deep-SVM hybrid framework with enhanced EEG feature engineering and SHAP-based explainability for Alzheimer’s classification. Sci Rep 16, 13001 (2026). https://doi.org/10.1038/s41598-026-43431-w
Nyckelord: EEG demensdiagnostik, Alzheimers sjukdom, frontotemporal demens, förklarlig AI, hjärnvågor