Clear Sky Science · pl
Hybydowe ramy deep-SVM z ulepszoną inżynierią cech EEG i wyjaśnialnością opartą na SHAP dla klasyfikacji choroby Alzheimera
Dlaczego testy fal mózgowych mogą wykrywać demencję wcześniej
Demencja, w tym choroba Alzheimera i otępienie czołowo-skroniowe, narasta na całym świecie, podczas gdy dostępne dziś narzędzia diagnostyczne są często kosztowne, inwazyjne lub trudne do regularnego powtarzania. W tym badaniu sprawdzono, czy proste zapisy fal mózgowych wykonane elektroencefalografią (EEG) mogą pomóc lekarzom rozróżnić różne typy demencji oraz prawidłowe starzenie się. Badacze skupili się również na uczynieniu decyzji komputera zrozumiałymi dla klinicystów, tak aby system był nie tylko trafny, lecz także przejrzysty i godny zaufania.
Słuchanie mózgu bez operacji
EEG mierzy drobne sygnały elektryczne na skórze głowy, powstające gdy grupy komórek mózgowych aktywują się jednocześnie. Sygnały te zmieniają się wraz z postępem demencji: szybsze rytmy zwykle słabną, wolniejsze rytmy wzmacniają się, a komunikacja między obszarami mózgu może ulegać pogorszeniu. W przeciwieństwie do obrazowania mózgu czy nakłuć lędźwiowych, EEG jest nieinwazyjne, względnie tanie i można je powtarzać tak często, jak potrzeba. To czyni je atrakcyjną kandydaturą do badań przesiewowych oraz rutynowej obserwacji, pod warunkiem że potrafimy niezawodnie odczytać złożone, zaszumione wzorce ukryte w falach.
Łączenie wiedzy ludzkiej z uczeniem maszynowym
Zespół zaprojektował hybrydowy system komputerowy, który łączy dwa rodzaje informacji z każdego 4‑sekundowego segmentu EEG. Po pierwsze, opracowano „ręcznie konstruowane” cechy znane neurobiologom jako powiązane z demencją, takie jak siła poszczególnych pasm częstotliwości (wolne delta i theta, szybsze alfa i beta), nieprzewidywalność widma oraz synchronizacja lewych i prawych obszarów mózgu w paśmie alfa. Po drugie, wytrenowano kompaktową jednowymiarową sieć konwolucyjną, która automatycznie uczy się przydatnych wzorców czasowych bezpośrednio z oczyszczonych sygnałów. Te dwa strumienie cech są standaryzowane, scalane w jedną reprezentację, a następnie kompresowane do mniejszego zestawu składników, by uniknąć redundancji.
Rozważne korzystanie z ograniczonych danych pacjentów
Główny zbiór danych składał się z EEG spoczynkowego 88 dorosłych — osób z chorobą Alzheimera, osób z otępieniem czołowo-skroniowym oraz ochotników o prawidłowej funkcji poznawczej — zebranych w spójnych warunkach rejestracji. Ponieważ liczba uczestników jest umiarkowana, badacze zastosowali szczególne środki, by nie przecenić wyników. Podzielili dane według osób, a nie poszczególnych segmentów EEG, tak by nagrania tej samej osoby nigdy nie występowały jednocześnie w zbiorach treningowym i testowym. W każdej części treningowej zrównoważono klasy za pomocą kontrolowanej metody oversamplingu, znormalizowano cechy i dostrajano parametry modelu, takie jak liczba zachowanych składowych głównych oraz siła regularyzacji finalnego klasyfikatora. Tak zaprojektowana zagnieżdżona ewaluacja istotnie zmniejsza ryzyko „przecieku” danych i nadmiernie optymistycznych wyników.
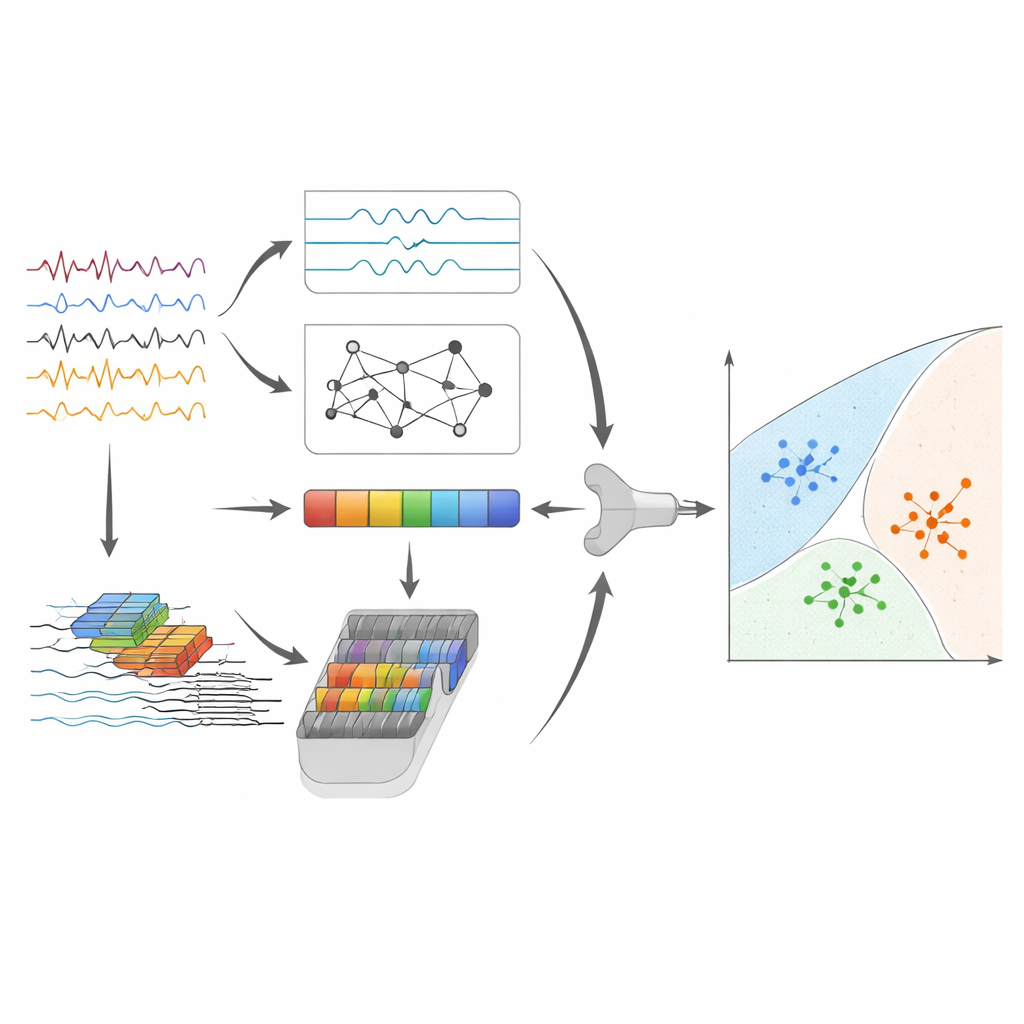
Wysoka trafność i wgląd w to, co widzi model
Po fuzji cech i kompresji, końcowy etap wykorzystuje maszynę wektorów nośnych (SVM), klasyczny algorytm rysujący granice separujące grupy punktów w przestrzeni cech. Na głównym zbiorze danych ten hybrydowy pipeline poprawnie rozróżniał chorobę Alzheimera, otępienie czołowo-skroniowe i prawidłowe starzenie w około 95% segmentów EEG, przy równomiernie dobrej wydajności dla wszystkich trzech grup. Aby sprawdzić, jak podejście zachowa się w nowych sytuacjach, autorzy zastosowali je bez większych zmian do zapisów z otwartymi oczami tych samych osób oraz do całkowicie niezależnego zbioru danych zarejestrowanego innym sprzętem i w innych warunkach demograficznych. Choć skuteczność naturalnie spadła, system nadal wykazał znaczącą zdolność dyskryminacji, co sugeruje, że wychwytuje wzorce związane z chorobą, a nie cechy jednego badania.
Otwieranie czarnej skrzynki dla klinicystów
Ponad trafnością, centralnym celem pracy jest wyjaśnialność: lekarze muszą rozumieć, dlaczego algorytm skłania się ku konkretnej diagnozie. Badacze zastosowali metodę SHAP, by oszacować, jak bardzo każda cecha „popycha” model w stronę lub z dala od danej klasy. Grupując te wkłady w proste jednostki — takie jak konkretne pasma częstotliwości i obszary mózgu — otrzymali podsumowania przypominające tradycyjne raporty EEG. Wzorce zwiększające prawdopodobieństwo decyzji o Alzheimerze lub otępieniu czołowo-skroniowym obejmowały silniejszą aktywność wolnego theta w obszarach czołowych, słabsze rytmy alfa w rejonach tylnych oraz zmniejszoną koordynację w paśmie alfa między półkulami, co zgadza się z wieloletnimi klinicznymi obserwacjami EEG.
Co to oznacza dla pacjentów i placówek
W praktycznym ujęciu badanie pokazuje, że starannie zaprojektowany system oparty na EEG może z wysoką niezawodnością rozdzielać dwie główne postacie demencji między sobą i od zdrowego starzenia, jednocześnie wyjaśniając swoje rozumowanie w znanych, fizjologicznych kategoriach. Jeśli narzędzia te zostaną zweryfikowane na większych, wieloośrodkowych kohortach, mogłyby wspierać wcześniejszą, precyzyjniejszą diagnostykę przy użyciu taniego sprzętu i integrować się z przyjaznymi dla klinik panelami pokazującymi estymaty ryzyka oraz cechy fal mózgowych je warunkujące. Podejście nie ma zastępować klinicystów, lecz działać jako dodatkowa para oczu — uwypuklając subtelne zmiany w aktywności mózgu, które mogą wskazywać na konieczność dalszych badań lub bliższego monitorowania.
Cytowanie: Akbar, F., Alkhrijah, Y., Usman, S.M. et al. A deep-SVM hybrid framework with enhanced EEG feature engineering and SHAP-based explainability for Alzheimer’s classification. Sci Rep 16, 13001 (2026). https://doi.org/10.1038/s41598-026-43431-w
Słowa kluczowe: diagnostyka demencji z EEG, choroba Alzheimera, otępienie czołowo-skroniowe, wyjaśnialna sztuczna inteligencja, fale mózgowe