Clear Sky Science · es
Un marco híbrido deep‑SVM con ingeniería de características EEG mejorada y explicabilidad basada en SHAP para la clasificación del Alzheimer
Por qué las pruebas de ondas cerebrales podrían detectar la demencia antes
La demencia, incluida la enfermedad de Alzheimer y la demencia frontotemporal, está aumentando en todo el mundo, pero las herramientas diagnósticas actuales suelen ser costosas, invasivas o difíciles de repetir con regularidad. Este estudio explora si registros simples de ondas cerebrales, tomados con un electroencefalograma (EEG), pueden ayudar a los médicos a distinguir entre distintos tipos de demencia y el envejecimiento saludable. Los investigadores también se centran en hacer comprensibles las decisiones del ordenador para los clínicos, de modo que no solo sean precisas, sino también transparentes y confiables.
Escuchar el cerebro sin cirugía
El EEG mide diminutas señales eléctricas desde el cuero cabelludo cuando grupos de células cerebrales disparan de forma sincronizada. Estas señales cambian a medida que la demencia progresa: los ritmos más rápidos tienden a debilitarse, los ritmos más lentos se fortalecen y la comunicación entre regiones cerebrales puede deteriorarse. A diferencia de las pruebas por imagen o las punciones lumbares, el EEG es no invasivo, relativamente barato y puede repetirse tantas veces como sea necesario. Eso lo convierte en un candidato atractivo para cribados a gran escala y seguimientos rutinarios, siempre que podamos decodificar de forma fiable los patrones complejos y ruidosos escondidos en las ondas.
Mezclando la intuición humana con el aprendizaje automático
El equipo diseñó un sistema híbrido que combina dos tipos de información de cada segmento EEG de 4 segundos. Primero, generaron características «manualmente diseñadas» que los neurocientíficos ya saben que están vinculadas a la demencia, como la potencia de distintas bandas de frecuencia (delta y theta lentas, alfa y beta más rápidas), la imprevisibilidad del espectro y cómo de sincronizadas permanecen las regiones izquierda y derecha del cerebro en la banda alfa. Segundo, entrenaron una red neuronal convolucional unidimensional compacta para aprender automáticamente patrones temporales útiles directamente de las señales depuradas. Estas dos corrientes de características se estandarizan, se fusionan en una única representación y luego se comprimen en un conjunto menor de componentes para evitar redundancias.
Uso cuidadoso de datos limitados de pacientes
El conjunto de datos principal consistió en EEG en estado de reposo de 88 adultos—personas con enfermedad de Alzheimer, personas con demencia frontotemporal y voluntarios cognitivamente normales—recogidos bajo condiciones de registro consistentes. Dado que el número de voluntarios es moderado, los investigadores pusieron especial cuidado en evitar sobreestimar el rendimiento. Dividieron los datos por persona, no por segmentos EEG individuales, de modo que las ondas de un mismo participante nunca aparecieran en ambos, entrenamiento y prueba. Dentro de cada partición de entrenamiento, equilibraron las clases usando un método de sobremuestreo controlado, normalizaron las características y ajustaron parámetros del modelo como cuántos componentes principales conservar y qué fuerza de regularización aplicar al clasificador final. Este diseño de evaluación anidada reduce marcadamente el riesgo de “filtración” y de resultados excesivamente optimistas.
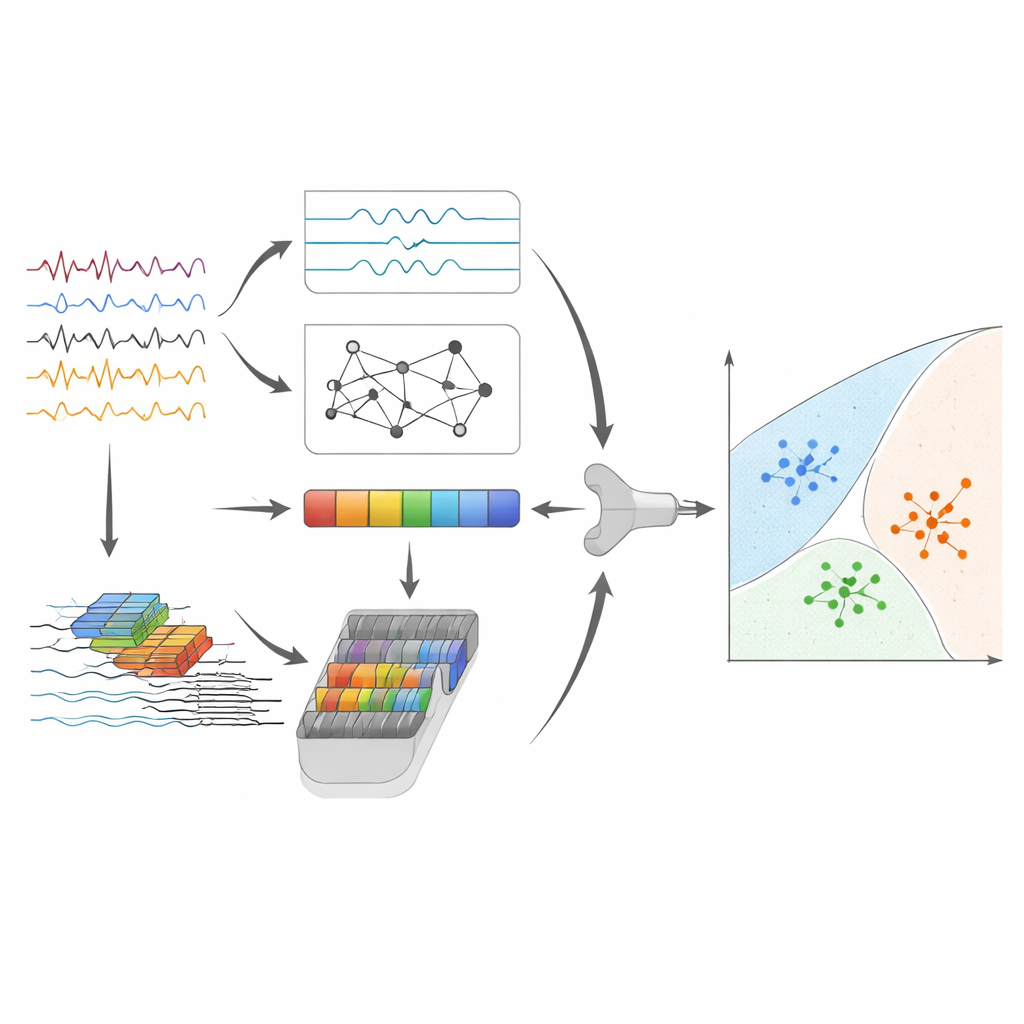
Alta precisión y visión sobre lo que el modelo detecta
Tras la fusión y compresión de características, el paso final utiliza una máquina de vectores de soporte, un algoritmo clásico que traza límites separadores entre grupos de puntos en el espacio de características. En el conjunto de datos principal, esta canalización híbrida distinguió correctamente entre la enfermedad de Alzheimer, la demencia frontotemporal y el envejecimiento normal en aproximadamente el 95% de los segmentos EEG, con un rendimiento igualmente sólido entre los tres grupos. Para evaluar la capacidad de generalización a situaciones nuevas, los autores también aplicaron el método, sin rediseños mayores, a ondas cerebrales de las mismas personas registradas con los ojos abiertos y a un conjunto de datos completamente independiente, grabado con distinto equipo y demografía. Aunque el rendimiento bajó de forma natural, el sistema siguió mostrando discriminación significativa, lo que sugiere que captura patrones relacionados con la enfermedad en lugar de peculiaridades de un único estudio.
Abrir la caja negra para los clínicos
Más allá de la precisión, un objetivo central del trabajo es la explicabilidad: los médicos necesitan ver por qué un algoritmo se inclina hacia un diagnóstico concreto. Los investigadores emplearon un método llamado SHAP para estimar cuánto «empuja» cada característica al modelo hacia o en contra de una clase determinada. Agrupando estas contribuciones en unidades sencillas—como bandas de frecuencia específicas y regiones cerebrales—produjeron resúmenes que se asemejan a los informes EEG tradicionales. Los patrones que favorecían las decisiones de Alzheimer o demencia frontotemporal incluían actividad theta lenta más intensa en áreas frontales, ritmos alfa debilitados en regiones posteriores y reducción de la coordinación en la banda alfa entre ambos hemisferios, hallazgos coherentes con décadas de observaciones clínicas en EEG.
Qué significa esto para pacientes y clínicas
En términos prácticos, este estudio muestra que un sistema basado en EEG cuidadosamente diseñado puede ayudar a separar con alta fiabilidad dos tipos principales de demencia entre sí y del envejecimiento sano, al tiempo que explica su razonamiento en términos fisiológicos familiares. Si se valida en cohortes más grandes y multicéntricas, tales herramientas podrían facilitar diagnósticos más tempranos y precisos con equipamiento asequible, y podrían integrarse en paneles clínicos que muestren estimaciones de riesgo y las características de las ondas cerebrales que las sustentan. En lugar de reemplazar a los clínicos, el enfoque pretende actuar como un segundo par de ojos—resaltando cambios sutiles en la actividad cerebral que pueden indicar la necesidad de investigaciones adicionales o un seguimiento más estrecho.
Cita: Akbar, F., Alkhrijah, Y., Usman, S.M. et al. A deep-SVM hybrid framework with enhanced EEG feature engineering and SHAP-based explainability for Alzheimer’s classification. Sci Rep 16, 13001 (2026). https://doi.org/10.1038/s41598-026-43431-w
Palabras clave: diagnóstico de demencia por EEG, enfermedad de Alzheimer, demencia frontotemporal, IA explicable, ondas cerebrales