Clear Sky Science · de
Ein Deep‑SVM‑Hybridrahmen mit verbesserter EEG‑Merkmalsentwicklung und SHAP‑basierter Erklärbarkeit zur Alzheimer‑Klassifikation
Warum Hirnwellentests Demenz früher erkennen könnten
Die Häufigkeit von Demenz, einschließlich Alzheimer‑Krankheit und frontotemporaler Demenz, steigt weltweit an, während die heutigen Diagnoseverfahren oft teuer, invasiv oder schwer regelmäßig zu wiederholen sind. Diese Studie untersucht, ob einfache Hirnwellenaufzeichnungen, die mit einer Elektroenzephalogramm‑(EEG‑)Kappe gewonnen werden, Ärzten helfen können, verschiedene Demenzformen von gesundem Altern zu unterscheiden. Die Forschenden legen dabei besonderen Wert darauf, die Entscheidungen der Computer für Kliniker verständlich zu machen, sodass das System nicht nur genau, sondern auch transparent und vertrauenswürdig ist.
Dem Gehirn zuhören ohne Operation
EEG misst winzige elektrische Signale von der Kopfhaut, die entstehen, wenn Gruppen von Nervenzellen gemeinsam feuern. Diese Signale verändern sich, wenn Demenz fortschreitet: schnellere Rhythmen tendieren dazu abzuschwächen, langsamere Rhythmen verstärken sich, und die Kommunikation zwischen Hirnregionen kann gestört werden. Im Gegensatz zu bildgebenden Verfahren oder Liquorpunktionen ist EEG nicht invasiv, relativ kostengünstig und wiederholbar so oft wie nötig. Das macht es zu einem attraktiven Kandidaten für großflächiges Screening und routinemäßige Nachsorge, vorausgesetzt, wir können die komplexen, rauschbehafteten Muster in den Wellen zuverlässig entschlüsseln.
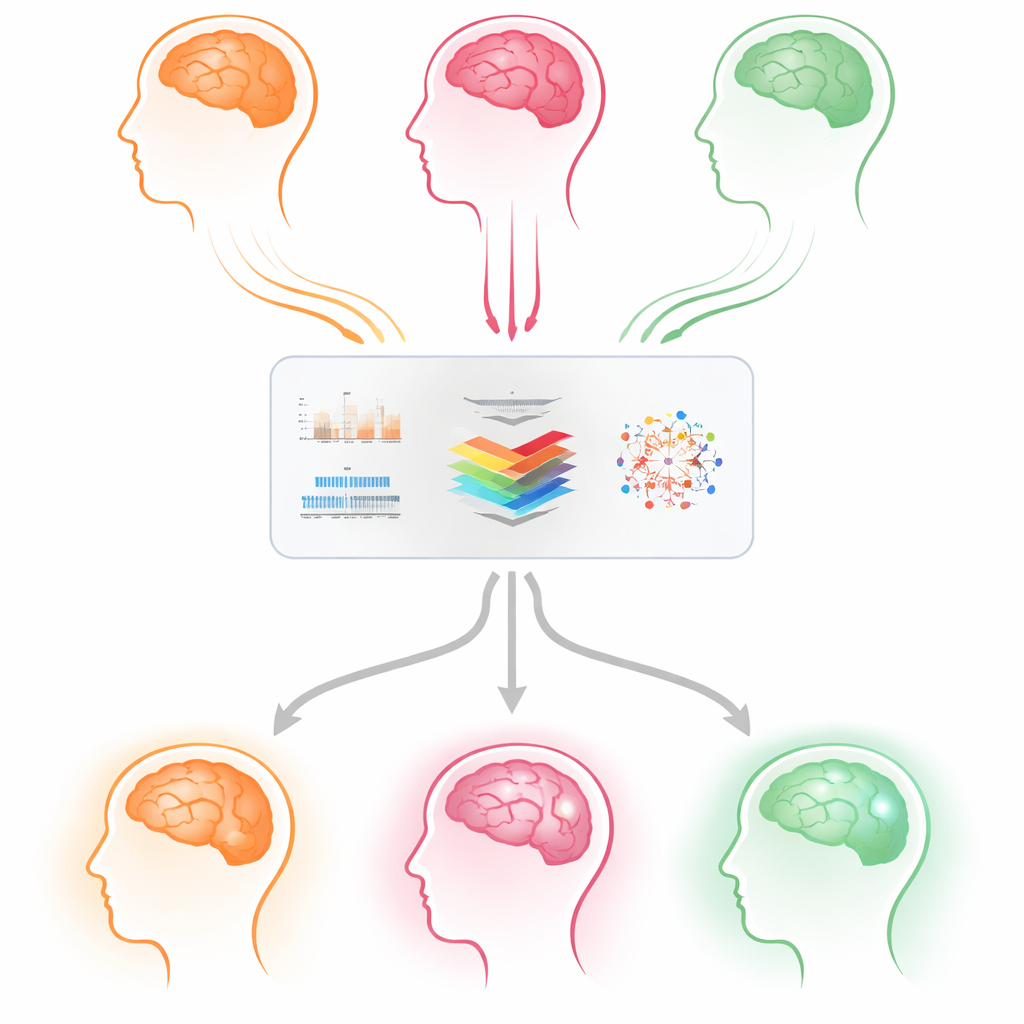
Menschliches Wissen mit maschinellem Lernen verbinden
Das Team entwarf ein hybrides System, das zwei Arten von Informationen aus jedem 4‑Sekunden‑EEG‑Segment kombiniert. Erstens extrahierten sie «handgefertigte» Merkmale, die Neurowissenschaftler bereits mit Demenz in Verbindung bringen, etwa die Stärke verschiedener Frequenzbänder (langsame Delta‑ und Theta‑Bänder, schnellere Alpha‑ und Beta‑Bänder), die Unvorhersehbarkeit des Spektrums und die Synchronität zwischen linker und rechter Hirnhälfte im Alpha‑Band. Zweitens trainierten sie ein kompaktes eindimensionales Faltungsnetzwerk, das automatisch nützliche zeitliche Muster direkt aus den bereinigten Signalen lernt. Diese beiden Merkmalsströme werden standardisiert, zu einer einzigen Repräsentation zusammengeführt und anschließend in eine kleinere Menge Komponenten komprimiert, um Redundanzen zu vermeiden.
Bewusster Umgang mit begrenzten Patientendaten
Der Hauptdatensatz bestand aus Ruhe‑EEG von 88 Erwachsenen – Personen mit Alzheimer‑Krankheit, Personen mit frontotemporaler Demenz und kognitiv normalen Freiwilligen – die unter einheitlichen Aufzeichnungsbedingungen erhoben wurden. Da die Stichprobengröße moderat ist, achteten die Forschenden besonders darauf, die Leistungsbewertung nicht zu überschätzen. Sie teilten die Daten nach Personen, nicht nach einzelnen EEG‑Segmenten, sodass die Signale einer Person niemals gleichzeitig im Training und im Test auftauchten. Innerhalb jeder Trainingsaufteilung balancierten sie die Klassen mittels kontrollierter Oversampling‑Methoden, normierten die Merkmale und optimierten Modellparameter wie die Zahl der zu behaltenden Hauptkomponenten und die Stärke der Regularisierung des finalen Klassifikators. Dieses verschachtelte Evaluationsdesign reduziert das Risiko von «Leakage» und übermäßig optimistischen Ergebnissen erheblich.
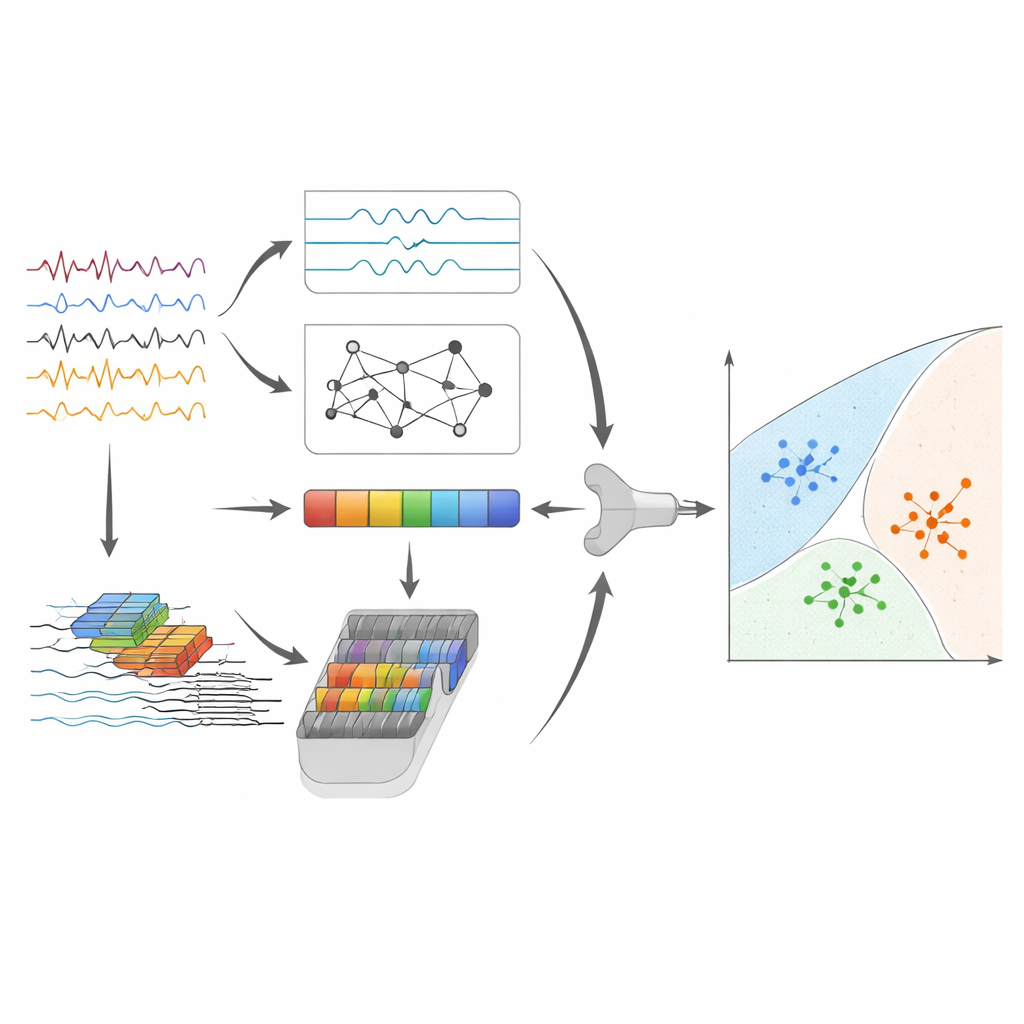
Hohe Genauigkeit und Einblicke in die Modellwahrnehmung
Nach Merkmalsfusion und Kompression folgt der letzte Schritt: ein Support‑Vector‑Machine‑Klassifikator, ein bewährter Algorithmus, der trennende Grenzen zwischen Punktgruppen im Merkmalsraum zieht. Im Hauptdatensatz unterschied diese hybride Pipeline Alzheimer‑Krankheit, frontotemporale Demenz und normales Altern korrekt für etwa 95 % der EEG‑Segmente, mit gleich starker Leistung über alle drei Gruppen. Um die Allgemeingültigkeit zu prüfen, wendeten die Autoren das System ohne wesentliche Umgestaltung auch auf Augen‑offen‑Aufnahmen derselben Personen sowie auf einen vollständig unabhängigen Datensatz an, der mit anderer Ausrüstung und anderen demografischen Merkmalen aufgenommen wurde. Zwar fiel die Leistung erwartungsgemäß etwas ab, doch zeigte das System weiterhin sinnvolle Diskriminationsfähigkeit und deutet darauf hin, dass es krankheitsrelevante Muster und nicht bloße Studienspezifika erfasst.
Die Blackbox für Kliniker öffnen
Über die Genauigkeit hinaus ist Erklärbarkeit ein zentrales Ziel der Arbeit: Ärzte müssen verstehen, warum ein Algorithmus zu einer bestimmten Diagnose tendiert. Die Forschenden nutzten die Methode SHAP, um abzuschätzen, wie stark jedes Merkmal das Modell in Richtung einer Klasse «drückt» oder davon «weggedrückt». Indem sie diese Beiträge in einfache Einheiten gruppierten – etwa spezifische Frequenzbänder und Hirnregionen – erzeugten sie Zusammenfassungen, die traditionellen EEG‑Befunden ähneln. Muster, die Entscheidungen zugunsten von Alzheimer oder frontotemporaler Demenz stärkten, umfassten verstärkte langsame Theta‑Aktivität über frontalen Bereichen, abgeschwächte Alpha‑Rhythmen in posterioren Regionen und reduzierte Alpha‑Band‑Koordination zwischen den Hemisphären, was mit jahrzehntelangen klinischen EEG‑Beobachtungen übereinstimmt.
Was das für Patienten und Kliniken bedeutet
Praktisch zeigt die Studie, dass ein sorgfältig gestaltetes EEG‑basiertes System helfen kann, zwei wichtige Demenzformen voneinander und vom gesunden Altern mit hoher Zuverlässigkeit zu trennen, und dabei seine Entscheidungsgrundlage in vertrauten physiologischen Begriffen erklärt. Wenn solche Werkzeuge in größeren, multizentrischen Kohorten validiert werden, könnten sie frühere und präzisere Diagnosen mit erschwinglicher Ausrüstung unterstützen und in klinikfreundliche Dashboards integriert werden, die Risikoschätzungen und die zugrunde liegenden Hirnwellenmerkmale anzeigen. Ziel ist nicht, Kliniker zu ersetzen, sondern als zweite Beobachterin bzw. zweites Beobachter zu dienen – subtile Veränderungen in der Hirnaktivität hervorzuheben, die auf eine weitergehende Abklärung oder engere Nachverfolgung hinweisen sollten.
Zitation: Akbar, F., Alkhrijah, Y., Usman, S.M. et al. A deep-SVM hybrid framework with enhanced EEG feature engineering and SHAP-based explainability for Alzheimer’s classification. Sci Rep 16, 13001 (2026). https://doi.org/10.1038/s41598-026-43431-w
Schlüsselwörter: EEG Demenzdiagnose, Alzheimer‑Krankheit, frontotemporale Demenz, erklärbare KI, Hirnwellen