Clear Sky Science · nl
Een deep‑SVM hybride kader met verbeterde EEG‑feature engineering en SHAP‑gebaseerde verklaarbaarheid voor de classificatie van Alzheimer
Waarom hersengolftests dementie eerder zouden kunnen opsporen
Dementie, waaronder de ziekte van Alzheimer en frontotemporale dementie, neemt wereldwijd toe, terwijl de huidige diagnostische middelen vaak duur, invasief of moeilijk regelmatig te herhalen zijn. Deze studie onderzoekt of eenvoudige hersengolfopnamen, gemaakt met een elektro-encefalogram (EEG)-cap, artsen kunnen helpen om verschillende vormen van dementie te onderscheiden van gezond ouder worden. De onderzoekers richten zich daarnaast op het begrijpelijk maken van de beslissingen van de computer voor clinici, zodat het systeem niet alleen nauwkeurig maar ook transparant en betrouwbaar is.
Luisteren naar de hersenen zonder operatie
EEG meet kleine elektrische signalen op de hoofdhuid wanneer groepen hersencellen tegelijk vuren. Deze signalen veranderen naarmate dementie vordert: snellere ritmes verzwakken vaak, tragere ritmes nemen toe en de communicatie tussen hersengebieden kan verslechteren. In tegenstelling tot hersenscans of lumbaalpuncties is EEG niet-invasief, relatief goedkoop en kan het zo vaak herhaald worden als nodig. Dat maakt het een aantrekkelijke kandidaat voor grootschalige screening en routinematige opvolging, mits we de complexe, lawaaierige patronen in de golven betrouwbaar kunnen ontcijferen.
Het samensmeden van menselijke inzichten en machine learning
Het team ontwierp een hybride computersysteem dat twee soorten informatie combineert uit elk 4 seconden durend EEG‑segment. Ten eerste maakten ze ‘handgemaakte’ kenmerken die neurowetenschappers al kennen als gerelateerd aan dementie, zoals de sterkte van verschillende frequentiebanden (trage delta en theta, snellere alfa en bèta), hoe onvoorspelbaar het spectrum is, en hoe goed linker- en rechterhersengebieden synchroon blijven in de alfaband. Ten tweede trainden ze een compacte eendimensionale convolutionele neurale netwerk (1D‑CNN) om automatisch nuttige temporele patronen direct uit de schoongemaakte signalen te leren. Deze twee feature‑stromen worden gestandaardiseerd, samengevoegd tot één representatie en vervolgens gecomprimeerd tot een kleinere set componenten om redundantie te vermijden.
Zorgvuldig omgaan met beperkte patiëntgegevens
De hoofdgegevensset bestond uit rust‑EEG van 88 volwassenen — mensen met de ziekte van Alzheimer, mensen met frontotemporale dementie en cognitief normale vrijwilligers — verzameld onder consistente opnameomstandigheden. Omdat het aantal vrijwilligers bescheiden is, namen de onderzoekers extra voorzorgsmaatregelen om te voorkomen dat de prestaties te optimistisch worden ingeschat. Ze splitsten de data per persoon, niet per individueel EEG‑segment, zodat de golven van een deelnemer nooit zowel in de training als in de test voorkwamen. Binnen elke trainingssplit balanceerden ze de klassen met een gecontroleerde oversamplingmethode, normaliseerden de kenmerken en stelden ze modelinstellingen af, zoals het aantal te behouden hoofdcomponenten en de sterkte van regularisatie van de uiteindelijke classifier. Dit geneste evaluatieontwerp verkleint sterk het risico op ‘lekkage’ en te optimistische resultaten.
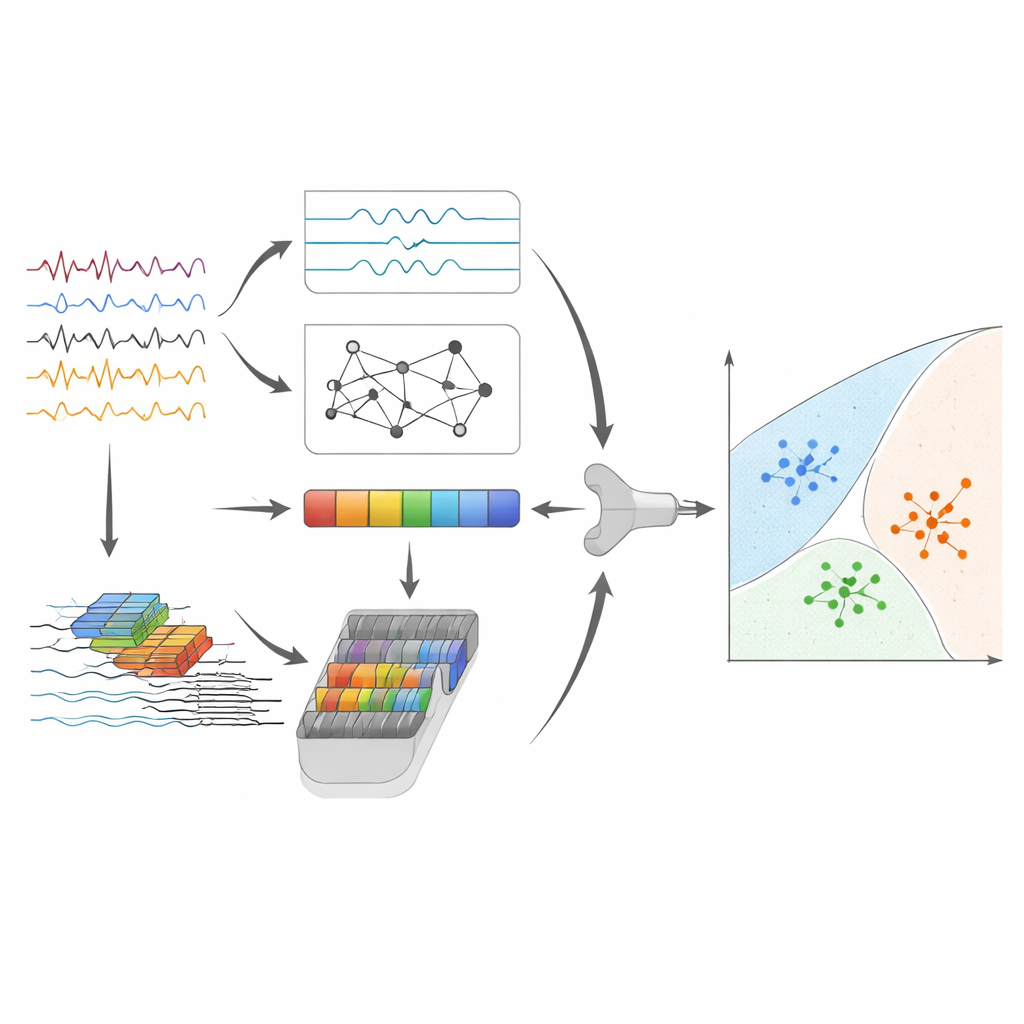
Hoge nauwkeurigheid en inzichten in wat het model ziet
Na featurefusie en compressie gebruikt de laatste stap een support vector machine, een klassiek algoritme dat scheidende grenzen trekt tussen groepen punten in de feature‑ruimte. Op de hoofdgegevensset onderscheidde deze hybride pijplijn correct de ziekte van Alzheimer, frontotemporale dementie en normaal ouder worden in ongeveer 95% van de EEG‑segmenten, met gelijk sterke prestaties over de drie groepen. Om te testen hoe goed de aanpak in nieuwe omstandigheden standhoudt, pasten de auteurs het, zonder ingrijpende herontwerp, ook toe op hersengolven van dezelfde personen opgenomen met open ogen en op een volledig onafhankelijke dataset die met andere apparatuur en andere demografieën was opgenomen. Hoewel de prestaties natuurlijk iets daalden, liet het systeem nog steeds betekenisvolle discriminatie zien, wat suggereert dat het ziektespecifieke patronen opvangt in plaats van eigenaardigheden van één enkele studie.
De zwarte doos openen voor clinici
Naast nauwkeurigheid is verklaarbaarheid een centraal doel van het werk: artsen moeten kunnen zien waarom een algoritme naar een bepaalde diagnose neigt. De onderzoekers gebruikten een methode genaamd SHAP om te schatten hoeveel elke feature het model naar of van een bepaalde klasse ‘duwt’. Door deze bijdragen te groeperen in eenvoudige units — zoals specifieke frequentiebanden en hersenregio’s — produceerden ze samenvattingen die lijken op traditionele EEG‑rapporten. Patronen die de beslissingen voor Alzheimer of frontotemporale dementie versterkten omvatten sterkere trage theta‑activiteit over frontale gebieden, zwakkere alfa‑ritmes in posterieure regio’s en verminderde alfa‑band coördinatie tussen de twee hemisferen, wat overeenkomt met decennia aan klinische EEG‑bevindingen.
Wat dit betekent voor patiënten en klinieken
In praktische termen toont deze studie aan dat een zorgvuldig ontworpen EEG‑gebaseerd systeem kan helpen om twee belangrijke dementietypen van elkaar en van gezond ouder worden te onderscheiden met hoge betrouwbaarheid, terwijl het ook zijn redenering uitlegt in vertrouwde fysiologische termen. Als het gevalideerd wordt op grotere, multicentrische cohorten, zouden dergelijke hulpmiddelen eerdere en preciezere diagnoses met betaalbare apparatuur kunnen ondersteunen en geïntegreerd kunnen worden in kliniek‑vriendelijke dashboards die risicoschattingen en de onderliggende hersengolfkenmerken tonen. In plaats van artsen te vervangen, is de aanpak bedoeld als een extra paar ogen — het benadrukken van subtiele veranderingen in hersenactiviteit die kunnen aangeven wanneer verder onderzoek of intensievere opvolging nodig is.
Bronvermelding: Akbar, F., Alkhrijah, Y., Usman, S.M. et al. A deep-SVM hybrid framework with enhanced EEG feature engineering and SHAP-based explainability for Alzheimer’s classification. Sci Rep 16, 13001 (2026). https://doi.org/10.1038/s41598-026-43431-w
Trefwoorden: EEG dementiediagnose, Ziekte van Alzheimer, frontotemporale dementie, verklaarbare AI, hersengolven