Clear Sky Science · pt
Uma estrutura híbrida deep‑SVM com engenharia de características EEG aprimorada e explicabilidade baseada em SHAP para classificação do Alzheimer
Por que testes de ondas cerebrais podem detectar demência mais cedo
A demência, incluindo a doença de Alzheimer e a demência frontotemporal, está aumentando em todo o mundo, contudo as ferramentas de diagnóstico atuais costumam ser caras, invasivas ou difíceis de repetir com regularidade. Este estudo investiga se registros simples de ondas cerebrais, obtidos com um capacete de eletroencefalograma (EEG), podem ajudar médicos a distinguir entre diferentes tipos de demência e o envelhecimento saudável. Os pesquisadores também se concentraram em tornar as decisões do computador compreensíveis para clínicos, de modo que não sejam apenas precisas, mas também transparentes e confiáveis.
Ouvir o cérebro sem cirurgia
O EEG mede sinais elétricos minúsculos no couro cabeludo quando grupos de células cerebrais disparam em conjunto. Esses sinais mudam à medida que a demência progride: ritmos mais rápidos tendem a enfraquecer, ritmos mais lentos se tornam mais fortes, e a comunicação entre regiões cerebrais pode se degradar. Ao contrário de exames de imagem ou punções lombares, o EEG é não invasivo, relativamente barato e pode ser repetido quantas vezes necessário. Isso o torna um candidato atraente para triagem em larga escala e acompanhamento rotineiro, desde que consigamos decodificar de forma confiável os padrões complexos e ruidosos escondidos nas ondas.
Misturando insight humano com aprendizado de máquina
A equipe projetou um sistema híbrido que combina dois tipos de informação de cada segmento EEG de 4 segundos. Primeiro, foram extraídas características “manuais” que neurocientistas já sabem estar relacionadas à demência, como a intensidade de diferentes bandas de frequência (lentas delta e teta, mais rápidas alfa e beta), quão imprevisível é o espectro e quão bem as regiões cerebrais esquerda e direita se mantêm sincronizadas na banda alfa. Em segundo lugar, treinaram uma rede neural convolucional unidimensional compacta para aprender automaticamente padrões temporais úteis diretamente a partir dos sinais limpos. Esses dois fluxos de características são padronizados, fundidos em uma representação única e então comprimidos em um conjunto menor de componentes para evitar redundância.
Uso cuidadoso de dados limitados de pacientes
O conjunto de dados principal consistiu em EEG de repouso de 88 adultos — pessoas com doença de Alzheimer, com demência frontotemporal e voluntários cognitivamente normais — coletados sob condições de gravação consistentes. Como o número de voluntários é modesto, os pesquisadores tomaram cuidados especiais para evitar superestimar o desempenho. Eles dividiram os dados por pessoa, não por segmentos individuais de EEG, para que as ondas cerebrais de um mesmo participante nunca aparecessem tanto no treinamento quanto no teste. Dentro de cada divisão de treinamento, equilibraram as classes usando um método controlado de sobremuestreamento, normalizaram as características e ajustaram parâmetros do modelo, como quantos componentes principais manter e quão forte regularizar o classificador final. Esse desenho de avaliação aninhada reduz fortemente o risco de “vazamento” e de resultados excessivamente otimistas.
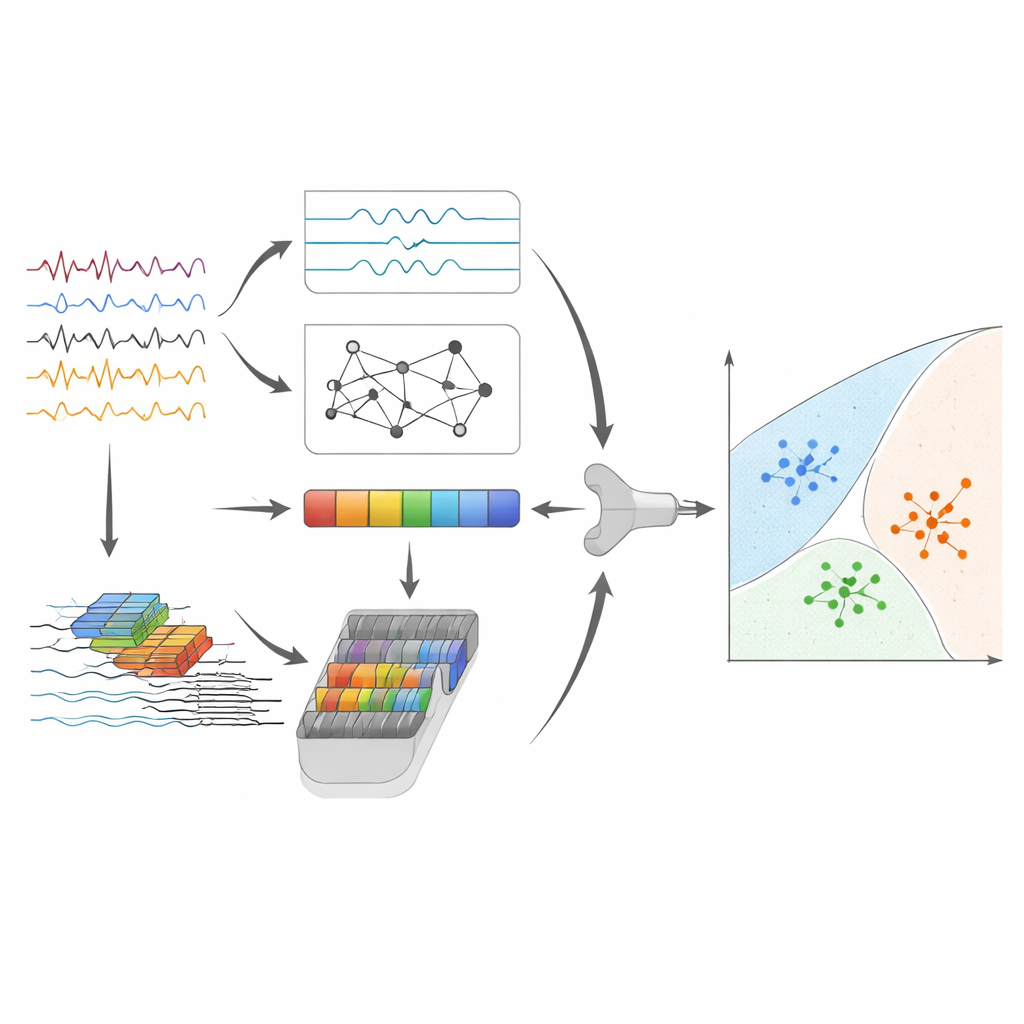
Alta acurácia e percepções sobre o que o modelo enxerga
Após a fusão e compressão das características, a etapa final usa uma máquina de vetores de suporte, um algoritmo clássico que traça fronteiras separadoras entre grupos de pontos no espaço de características. No conjunto de dados principal, esse pipeline híbrido distinguiu corretamente entre doença de Alzheimer, demência frontotemporal e envelhecimento normal em cerca de 95% dos segmentos de EEG, com desempenho igualmente forte entre os três grupos. Para avaliar quão bem o método poderia se manter em novas situações, os autores também o aplicaram, sem grande redesenho, a ondas cerebrais das mesmas pessoas registradas de olhos abertos, e a um conjunto de dados completamente independente coletado com equipamentos e demografia diferentes. Embora o desempenho tenha naturalmente caído, o sistema ainda apresentou discriminação significativa, sugerindo que está capturando padrões relacionados à doença em vez de peculiaridades de um único estudo.
Abrindo a caixa‑preta para os clínicos
Além da acurácia, um objetivo central do trabalho é a explicabilidade: os médicos precisam ver por que um algoritmo tende a um diagnóstico específico. Os pesquisadores usaram um método chamado SHAP para estimar o quanto cada característica “empurra” o modelo em direção ou contra uma determinada classe. Ao agrupar essas contribuições em unidades simples — como bandas de frequência específicas e regiões cerebrais — eles produziram resumos que se assemelham a relatórios tradicionais de EEG. Padrões que favoreceram decisões de Alzheimer ou demência frontotemporal incluíram maior atividade lenta em teta sobre áreas frontais, ritmos alfa mais fracos em regiões posteriores e redução da coordenação na banda alfa entre os dois hemisférios, o que corresponde a décadas de achados clínicos em EEG.
O que isso significa para pacientes e clínicas
Em termos práticos, este estudo mostra que um sistema baseado em EEG cuidadosamente projetado pode ajudar a separar dois grandes tipos de demência entre si e do envelhecimento saudável com alta confiabilidade, ao mesmo tempo em que explica seu raciocínio em termos fisiológicos familiares. Se validado em coortes maiores e multicêntricas, tais ferramentas poderiam apoiar diagnósticos mais precoces e precisos usando equipamentos acessíveis, e ser integradas em painéis amigáveis à clínica que mostram estimativas de risco e as características de ondas cerebrais que as impulsionam. Em vez de substituir os clínicos, a abordagem pretende atuar como um segundo par de olhos — destacando alterações sutis na atividade cerebral que podem sinalizar quando é necessária investigação adicional ou acompanhamento mais próximo.
Citação: Akbar, F., Alkhrijah, Y., Usman, S.M. et al. A deep-SVM hybrid framework with enhanced EEG feature engineering and SHAP-based explainability for Alzheimer’s classification. Sci Rep 16, 13001 (2026). https://doi.org/10.1038/s41598-026-43431-w
Palavras-chave: diagnóstico de demência por EEG, doença de Alzheimer, demência frontotemporal, IA explicável, ondas cerebrais