Clear Sky Science · fr
Un cadre hybride deep‑SVM avec ingénierie améliorée des caractéristiques EEG et explicabilité basée sur SHAP pour la classification de la maladie d’Alzheimer
Pourquoi les tests des ondes cérébrales pourraient repérer la démence plus tôt
La démence, y compris la maladie d’Alzheimer et la démence frontotemporale, augmente dans le monde entier, alors que les outils diagnostiques actuels sont souvent coûteux, invasifs ou difficiles à répéter régulièrement. Cette étude explore si de simples enregistrements d’ondes cérébrales, réalisés avec un casque électroencéphalographique (EEG), peuvent aider les médecins à distinguer différents types de démence et le vieillissement cognitif normal. Les chercheurs accordent également une attention particulière à rendre les décisions de l’ordinateur compréhensibles pour les cliniciens, de sorte qu’elles soient non seulement précises, mais aussi transparentes et dignes de confiance.
Écouter le cerveau sans chirurgie
L’EEG mesure de faibles signaux électriques depuis le cuir chevelu lorsque des groupes de cellules cérébrales s’activent simultanément. Ces signaux évoluent au fur et à mesure de la progression de la démence : les rythmes rapides tendent à s’affaiblir, les rythmes lents deviennent plus marqués, et la communication entre régions cérébrales peut se dégrader. Contrairement aux imageries cérébrales ou aux ponctions lombaires, l’EEG est non invasif, relativement peu coûteux et peut être répété aussi souvent que nécessaire. Cela en fait un candidat intéressant pour le dépistage à grande échelle et le suivi de routine, à condition que l’on sache décoder de manière fiable les motifs complexes et bruités cachés dans les ondes.
Mêler l’expertise humaine et l’apprentissage automatique
L’équipe a conçu un système hybride qui combine deux types d’informations extraites de chaque segment EEG de 4 secondes. Premièrement, ils ont construit des caractéristiques « faites à la main » que les neuroscientifiques savent déjà liées à la démence, comme l’intensité des différentes bandes de fréquence (lentes delta et thêta, plus rapides alpha et bêta), l’imprévisibilité du spectre, et la synchronisation entre hémisphères dans la bande alpha. Deuxièmement, ils ont entraîné un réseau de neurones convolutionnel compact unidimensionnel pour apprendre automatiquement des motifs temporels utiles directement à partir des signaux nettoyés. Ces deux flux de caractéristiques sont standardisés, fusionnés en une représentation unique, puis comprimés en un petit ensemble de composantes pour éviter la redondance.
Une utilisation prudente de données patients limitées
Le jeu de données principal comprenait des EEG de repos de 88 adultes — des personnes atteintes de la maladie d’Alzheimer, des personnes atteintes de démence frontotemporale et des volontaires cognitivement normaux — collectés dans des conditions d’enregistrement cohérentes. Parce que le nombre de volontaires est modeste, les chercheurs ont pris des précautions particulières pour éviter de surestimer les performances. Ils ont séparé les données par personne, et non par segment EEG, de sorte que les ondes d’un même participant n’apparaissent jamais à la fois dans l’entraînement et le test. Dans chaque division d’entraînement, ils ont équilibré les classes à l’aide d’une méthode d’oversampling contrôlée, normalisé les caractéristiques et ajusté les paramètres du modèle, comme le nombre de composantes principales à conserver et la force de régularisation du classifieur final. Ce protocole d’évaluation emboîté réduit fortement le risque de « fuite » d’informations et de résultats trop optimistes.
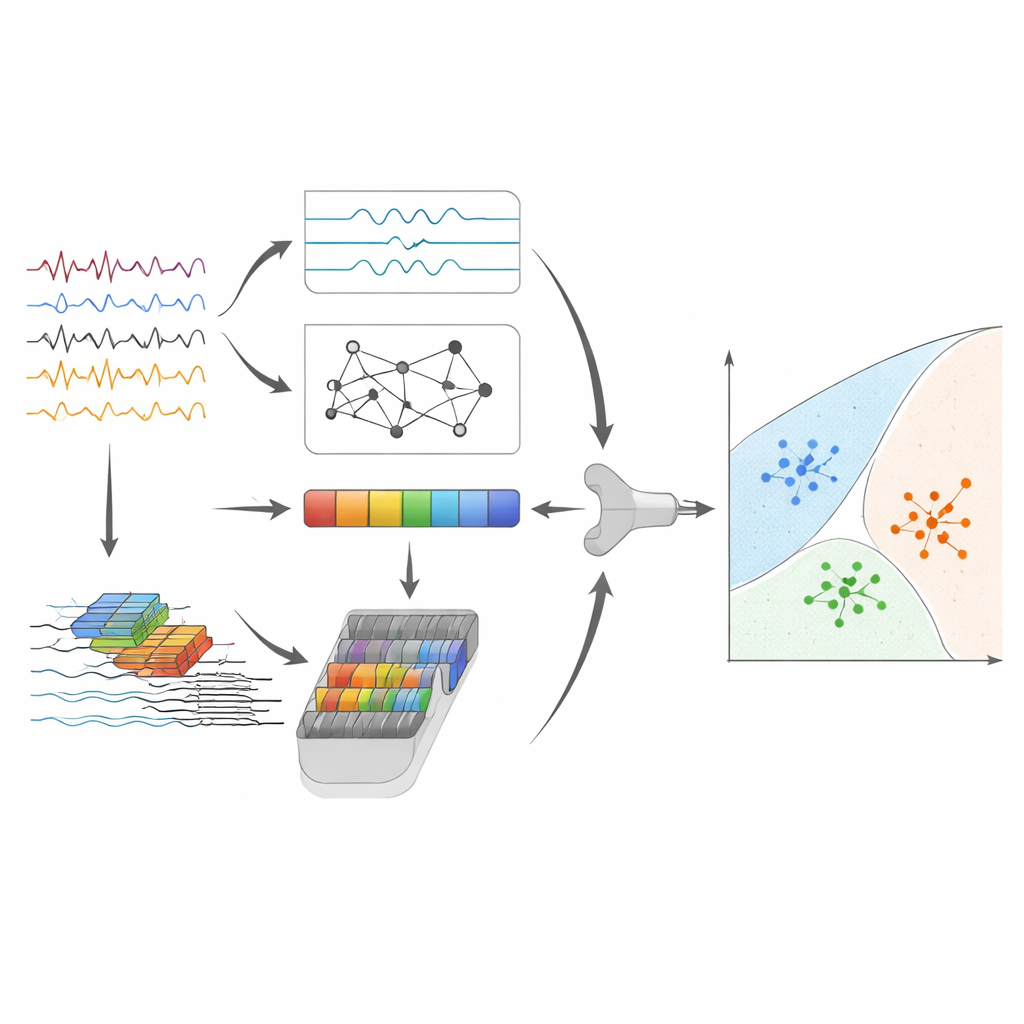
Haute précision et compréhension de ce que voit le modèle
Après fusion et compression des caractéristiques, l’étape finale utilise une machine à vecteurs de support (SVM), un algorithme classique qui trace des frontières séparatrices entre groupes de points dans l’espace des caractéristiques. Sur le jeu de données principal, ce pipeline hybride a correctement distingué la maladie d’Alzheimer, la démence frontotemporale et le vieillissement normal pour environ 95 % des segments EEG, avec des performances également solides entre les trois groupes. Pour évaluer la robustesse de l’approche, les auteurs l’ont aussi appliquée, sans refonte majeure, aux ondes cérébrales des mêmes sujets enregistrées les yeux ouverts, et à un jeu de données totalement indépendant enregistré avec du matériel et une démographie différents. Bien que les performances aient naturellement diminué, le système a conservé une discrimination significative, suggérant qu’il capte des motifs liés à la maladie plutôt que des particularités d’une seule étude.
Ouvrir la boîte noire pour les cliniciens
Au‑delà de la précision, un objectif central du travail est l’explicabilité : les médecins doivent voir pourquoi un algorithme penche vers un diagnostic particulier. Les chercheurs ont utilisé une méthode appelée SHAP pour estimer dans quelle mesure chaque caractéristique « pousse » le modèle vers ou à l’écart d’une classe donnée. En regroupant ces contributions en unités simples — telles que des bandes de fréquence spécifiques et des régions cérébrales — ils ont produit des synthèses qui ressemblent à des comptes rendus EEG traditionnels. Les motifs favorisant les décisions en faveur d’Alzheimer ou de démence frontotemporale incluaient une activité thêta lente renforcée dans les régions frontales, des rythmes alpha affaiblis dans les régions postérieures et une coordination réduite en bande alpha entre les deux hémisphères, ce qui concorde avec des décennies d’observations cliniques EEG.
Ce que cela signifie pour les patients et les cliniques
Concrètement, cette étude montre qu’un système EEG bien conçu peut aider à séparer avec fiabilité deux grands types de démence l’un de l’autre et du vieillissement sain, tout en expliquant son raisonnement en termes physiologiques familiers. Si ces résultats sont validés sur des cohortes plus larges et multicentriques, de tels outils pourraient soutenir un diagnostic plus précoce et plus précis avec du matériel abordable, et être intégrés dans des tableaux de bord adaptés aux cliniques affichant estimations de risque et caractéristiques d’ondes cérébrales explicatives. Plutôt que de remplacer les cliniciens, l’approche vise à agir comme une seconde paire d’yeux — mettant en évidence des changements subtils de l’activité cérébrale qui peuvent signaler la nécessité d’investigations complémentaires ou d’un suivi rapproché.
Citation: Akbar, F., Alkhrijah, Y., Usman, S.M. et al. A deep-SVM hybrid framework with enhanced EEG feature engineering and SHAP-based explainability for Alzheimer’s classification. Sci Rep 16, 13001 (2026). https://doi.org/10.1038/s41598-026-43431-w
Mots-clés: diagnostic démence EEG, maladie d’Alzheimer, démence frontotemporale, IA explicable, rythmes cérébraux