Clear Sky Science · it
Un framework ibrido deep-SVM con ingegneria delle caratteristiche EEG potenziata e spiegabilità basata su SHAP per la classificazione dell’Alzheimer
Perché i test delle onde cerebrali potrebbero individuare la demenza prima
La demenza, inclusa la malattia di Alzheimer e la demenza frontotemporale, è in aumento a livello globale, eppure gli strumenti diagnostici attuali sono spesso costosi, invasivi o difficili da ripetere regolarmente. Questo studio esplora se semplici registrazioni delle onde cerebrali, effettuate con un elettroencefalogramma (EEG) a cuffia, possano aiutare i medici a distinguere tra diversi tipi di demenza e l’invecchiamento sano. I ricercatori si concentrano inoltre sul rendere le decisioni del computer comprensibili ai clinici, in modo che non siano solo accurate, ma anche trasparenti e affidabili.
Ascoltare il cervello senza chirurgia
L’EEG misura minuscoli segnali elettrici dal cuoio capelluto mentre gruppi di cellule cerebrali si attivano insieme. Questi segnali cambiano con la progressione della demenza: i ritmi più veloci tendono a indebolirsi, quelli più lenti diventano più forti e la comunicazione tra le regioni cerebrali può deteriorarsi. Diversamente da esami di imaging o punture lombari, l’EEG è non invasivo, relativamente economico e può essere ripetuto tutte le volte necessarie. Questo lo rende un candidato interessante per screening su larga scala e follow-up di routine, a patto che si riescano a decodificare in modo affidabile i pattern complessi e rumorosi nascosti nelle onde.
Fondere l’intuizione umana con il machine learning
Il team ha progettato un sistema ibrido che combina due tipi di informazioni per ciascun segmento EEG di 4 secondi. Innanzitutto, hanno costruito caratteristiche “artigianali” note ai neuroscienziati come legate alla demenza, ad esempio l’energia nelle diverse bande di frequenza (delta e theta lente, alpha e beta più veloci), l’imprevedibilità dello spettro e quanto bene le regioni cerebrali sinistra e destra restano sincronizzate nella banda alpha. In secondo luogo, hanno addestrato una rete neurale convoluzionale compatta monodimensionale per apprendere automaticamente pattern temporali utili direttamente dai segnali puliti. Questi due flussi di caratteristiche vengono standardizzati, fusi in una rappresentazione unica e poi compressi in un numero ridotto di componenti per evitare ridondanze.
Usare con cura dati paziente limitati
Il dataset principale consisteva in EEG a riposo di 88 adulti—persone con malattia di Alzheimer, con demenza frontotemporale e volontari cognitivamente normali—raccolti in condizioni di registrazione coerenti. Poiché il numero di partecipanti è contenuto, i ricercatori hanno adottato misure speciali per evitare di sovrastimare le prestazioni. Hanno diviso i dati per persona, non per singoli segmenti EEG, così le onde di uno stesso partecipante non comparivano né nel training né nel test contemporaneamente. All’interno di ogni split di training hanno bilanciato le classi usando un metodo di oversampling controllato, normalizzato le caratteristiche e ottimizzato parametri del modello come il numero di componenti principali da mantenere e la forza di regolarizzazione del classificatore finale. Questo disegno di valutazione annidato riduce notevolmente il rischio di “leakage” e risultati eccessivamente ottimistici.
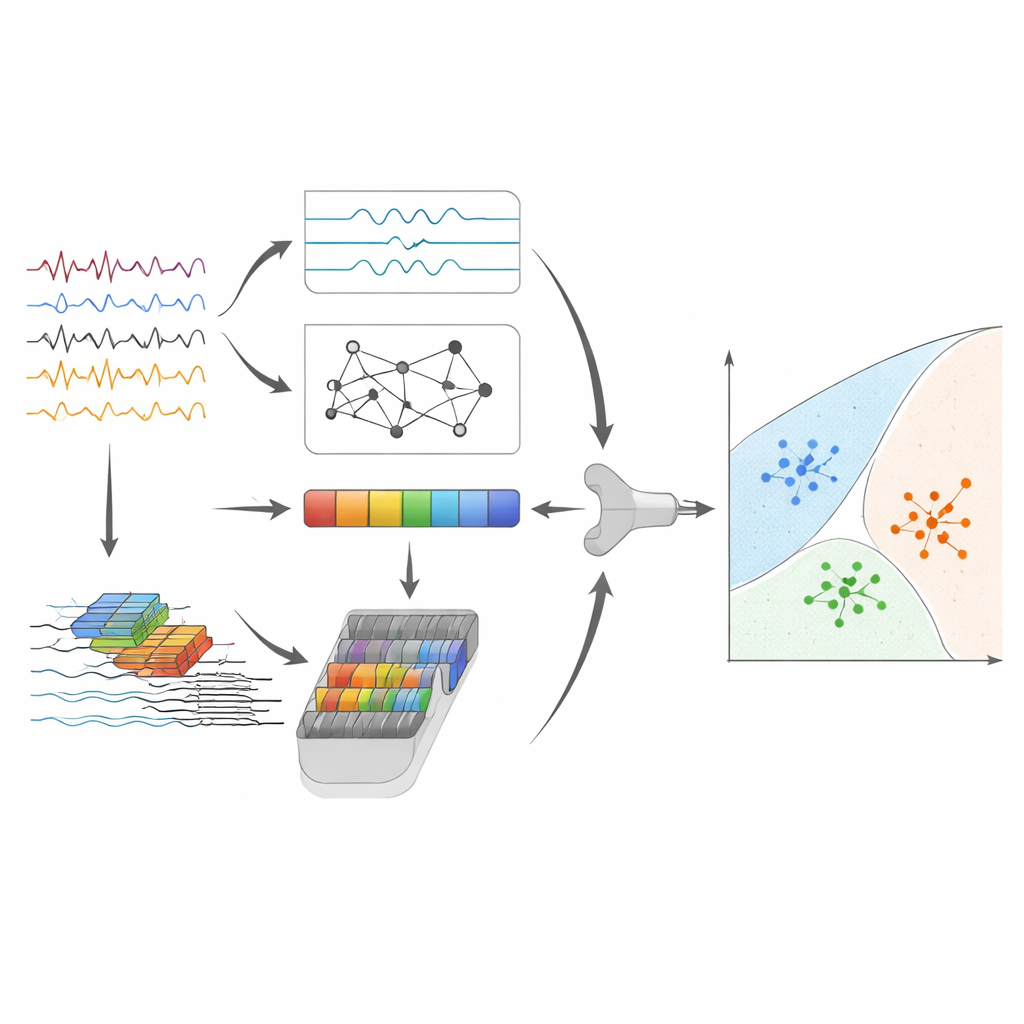
Alta accuratezza e intuizioni su ciò che il modello vede
Dopo la fusione e la compressione delle caratteristiche, il passo finale utilizza una support vector machine, un algoritmo classico che traccia confini separatori tra gruppi di punti nello spazio delle caratteristiche. Sul dataset principale, questa pipeline ibrida ha distinto correttamente tra malattia di Alzheimer, demenza frontotemporale e invecchiamento normale per circa il 95% dei segmenti EEG, con prestazioni altrettanto solide nelle tre classi. Per verificare la robustezza dell’approccio in nuovi contesti, gli autori lo hanno applicato, senza grandi modifiche, a registrazioni con gli occhi aperti delle stesse persone e a un dataset completamente indipendente registrato con apparecchiature e demografie diverse. Pur con un calo naturale di performance, il sistema ha mantenuto una discriminazione significativa, suggerendo che cattura pattern legati alla malattia piuttosto che peculiarità di un singolo studio.
Aprire la scatola nera per i clinici
Oltre all’accuratezza, un obiettivo centrale del lavoro è la spiegabilità: i medici devono poter vedere perché un algoritmo propende per una diagnosi specifica. I ricercatori hanno usato un metodo chiamato SHAP per stimare quanto ciascuna caratteristica “spinga” il modello verso o lontano da una certa classe. Raggruppando questi contributi in unità semplici—come bande di frequenza specifiche e regioni cerebrali—hanno prodotto riassunti che ricordano i referti EEG tradizionali. I pattern che favorivano le decisioni per Alzheimer o demenza frontotemporale includevano attività theta lenta più marcata nelle aree frontali, ritmi alpha più deboli nelle regioni posteriori e ridotta coordinazione nella banda alpha tra i due emisferi, riscontrazioni coerenti con decenni di osservazioni cliniche EEG.
Cosa significa per pazienti e cliniche
In termini pratici, questo studio dimostra che un sistema basato sull’EEG progettato con cura può aiutare a separare due grandi tipi di demenza l’uno dall’altro e dall’invecchiamento sano con alta affidabilità, spiegando al contempo il proprio ragionamento in termini fisiologici familiari. Se validati su coorti più ampie e multicentriche, tali strumenti potrebbero supportare diagnosi più precoci e più precise usando apparecchiature economiche, e potrebbero essere integrati in cruscotti clinici che mostrano stime di rischio e le caratteristiche delle onde cerebrali che le guidano. Piuttosto che sostituire i clinici, l’approccio è pensato per fungere da secondo paio di occhi—evidenziando cambiamenti sottili nell’attività cerebrale che possono segnalare la necessità di ulteriori indagini o di un follow-up più ravvicinato.
Citazione: Akbar, F., Alkhrijah, Y., Usman, S.M. et al. A deep-SVM hybrid framework with enhanced EEG feature engineering and SHAP-based explainability for Alzheimer’s classification. Sci Rep 16, 13001 (2026). https://doi.org/10.1038/s41598-026-43431-w
Parole chiave: diagnosi demenza EEG, malattia di Alzheimer, demenza frontotemporale, IA interpretabile, onde cerebrali