Clear Sky Science · sv
Mikrotubuli i axonen är bundna till GDP men antar ett stabilt GTP‑likt expanderat tillstånd
Hur cellens motorvägar formar hjärnans kopplingar
Inuti varje nervcell löper ett nätverk av mikroskopiska rör som fungerar som motorvägar och transporterar signaler och förnödenheter över långa avstånd. För att hjärnan ska fungera, särskilt när nervceller bildar långa axoner, måste dessa motorvägar vara både robusta och finjusterade. Denna studie tittar på dessa rör inne i levande‑lika mänskliga neuroner med nästan atomär detalj och visar att axonala ”vägar” använder en oväntad strategi för att förbli stabila—en strategi som kan hjälpa till att förklara hur neuroner utvecklas, hur trafiken längs axoner regleras och varför vissa hjärnläkemedel fungerar som de gör.
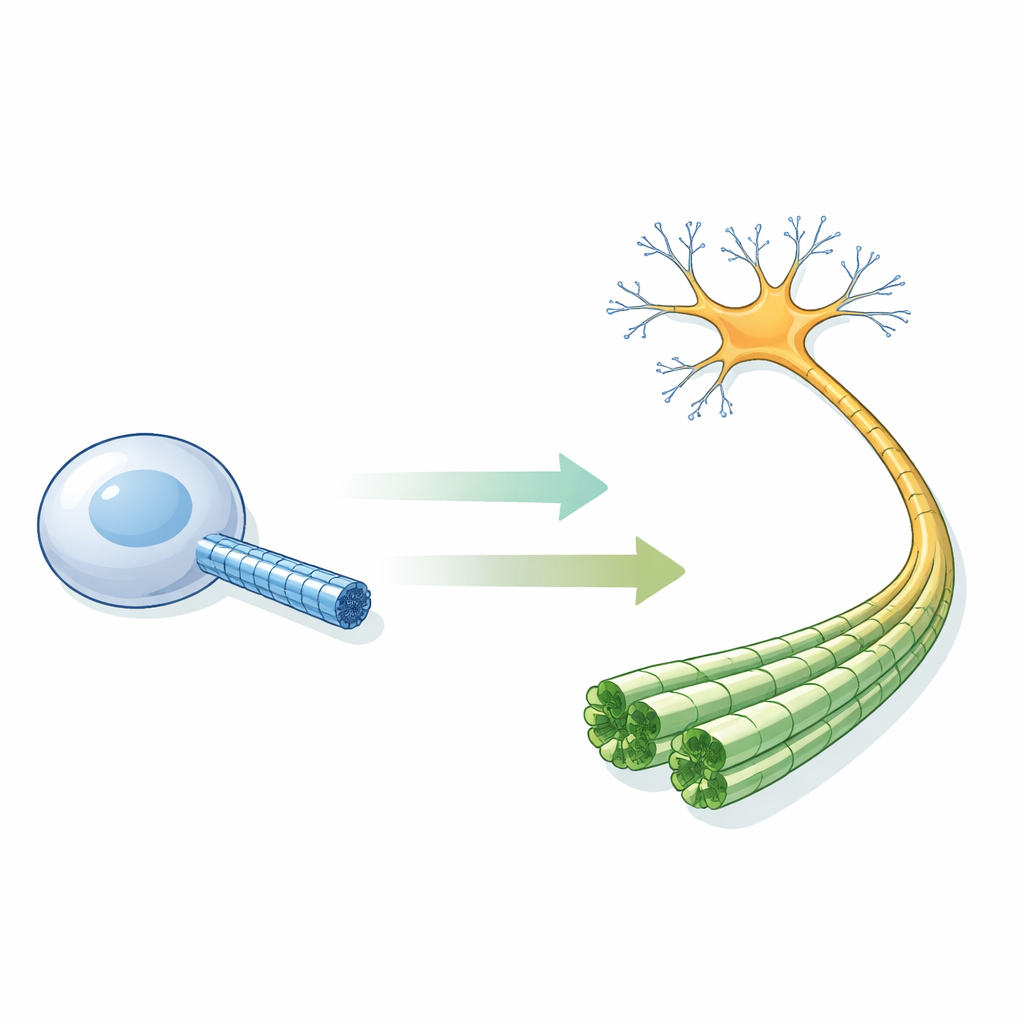
Små rör som håller neuronerna vid liv
Mikrotubuli är ihåliga cylindrar uppbyggda av repeterande proteinblock och finns i nästan alla våra celler. I neuroner är de särskilt viktiga: bundna till täta, parallella fackverk ger de axonerna deras form och fungerar som spår för motorproteiner som transporterar last mellan cellkroppen och avlägsna synapser. Provrörsexperiment har länge föreslagit en enkel regel: när byggstenarna bär en GTP‑molekyl antar rörväggen en ”expanderad” form och är stabil; efter att GTP brutits ned till GDP komprimeras väggen och röret blir skört och benäget att falla isär. Men ingen hade tidigare sett, med atomupplösning, hur dessa mikrotubuli ser ut inne i en verklig mänsklig neuron.
Att se axonala motorvägar atom för atom
Författarna odlade humana neuroner från inducerade pluripotenta stamceller och stimulerade dem att bilda sfäriska kluster som förlängde långa axoner över specialdesignade galler för elektronmikroskopi. Med toppmodern kryo‑elektronmikroskopi och tomografi registrerade de tusentals bilder av mikrotubuli inom intakta axoner frusna i ett nära‑naturligt tillstånd. Genom att datorbaserat medelvärdesbilda många vyer uppnådde de en rekonstruktion på 2,7 ångström—tillräckligt fin för att urskilja de två närbesläktade tubulinproteinerna, lokalisera de bundna nukleotiderna och till och med lösa ordnade vattenmolekyler och metalljoner. De kunde därför bestämma inte bara hur långt ifrån varandra byggstenarna sitter längs varje protofilament, utan också exakt i vilket kemiskt tillstånd dessa block befann sig.
En stabil gitterstruktur som bryter mot de vanliga reglerna
Den högupplösta strukturen gav en överraskning. I axonala mikrotubuli höll den utbytbara platsen i β‑tubulin tydligt GDP, vilket visar att GTP hade hydrolyserats som förväntat. Ändå var avståndet mellan tubulinparen längs röret expanderat, vilket matchade det som tidigare setts endast i GTP‑lika, stabila gitter bildade in vitro. Detaljerade jämförelser med kända strukturer avslöjade ett hybridtillstånd: regioner av proteinet som känner av närvaron av γ‑fosfat uppträdde som klassiska GDP‑mikrotubuli, medan element längre bort—särskilt en rörlig segment kallat T5‑loopen vid skarven mellan intilliggande dimerer—antog den expanderade, GTP‑lika arrangemanget. En kedja av aromatiska aminosyror verkar förmedla rörelser från denna loop till närliggande kontakter och låser det axonala gitteret i en utsträckt, stabil konfiguration trots dess GDP‑kemi.
Byten av tillstånd när neuroner mognar
För att ta reda på om denna ovanliga geometri var ett särskilt drag hos mogna axoner mätte teamet gitteravstånd i andra sammanhang med hjälp av kryo‑elektrontomografi och effekt‑spektumanalys. I odifferentierade stamceller visade mikrotubuli mer kompakt avstånd, som nära matchade GDP‑mikrotubuli assemblerade i provrör. Däremot uppvisade mikrotubuli inom axoner i differentierade neuroner expanderat avstånd, liknande den axonala atomstrukturen och de in vitro‑gitter som stabiliserats av icke‑hydrolyserbara GTP‑mimiker eller läkemedlet Taxol. Denna övergång från kompakt till expanderad geometri verkar alltså vara en del av neuronernas differentieringsprogram och sammanfaller med behovet av att stabilisera långa axonala utskott och organisera dem i täta buntar.
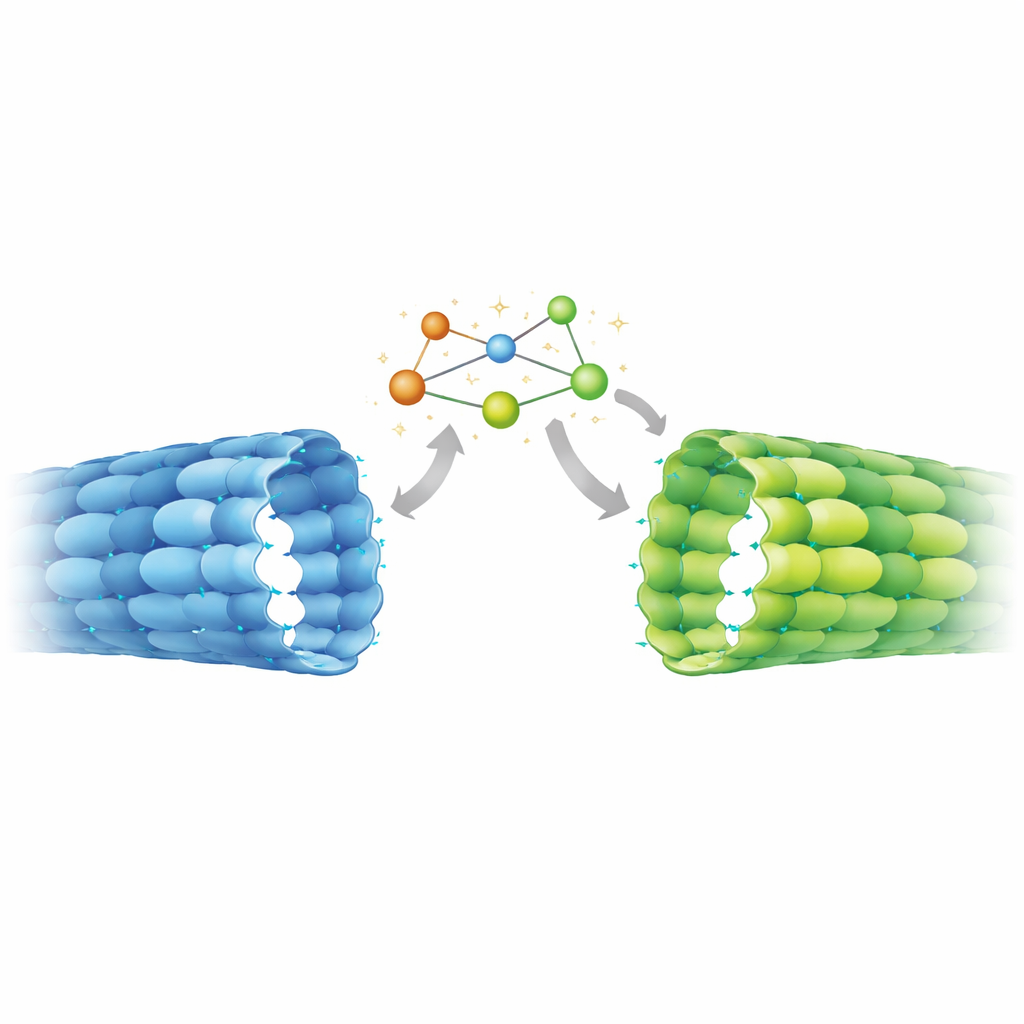
Konsekvenser för hjärnfunktion och terapi
Detta arbete visar att axonala mikrotubuli kemiskt befinner sig i ett GDP‑tillstånd men strukturellt i en GTP‑lik expanderad form, stabiliserad av en intern mekanisk växel. Det betyder att motorer, regulatoriska proteiner och enzymer som dekorerar mikrotubuli i neuroner interagerar med en gitttertyp som många standardlaboratoriepreparat inte troget återskapar. Eftersom dessa effektorer själva kan föredra expanderat eller kompakt avstånd—och vissa kemiska modifieringar av tubulin gynnar expanderade gitter—kan det upptäckta tillståndet sannolikt vara inblandat i en återkopplingsslinga som finjusterar transport av last och mikrotubulilivslängd under hjärnans utveckling. Resultaten antyder också att läkemedel som Taxol, som är kända för att expandera gitteret, kan främja axontillväxt delvis genom att föra mikrotubuli mot samma stabila konformation som naturligt uppträder när neuroner kopplas samman.
Citering: Zehr, E.A., Sun, S., Sarbanes, S.L. et al. Microtubules in the axon are GDP bound but adopt a stable GTP-like expanded state. Nat Struct Mol Biol 33, 631–640 (2026). https://doi.org/10.1038/s41594-026-01787-7
Nyckelord: mikrotubuli, axon, neuronal differentiering, kryo‑elektronmikroskopi, cytoskelett