Clear Sky Science · fr
Les microtubules dans l’axone sont liés au GDP mais adoptent un état étendu stable de type GTP
Comment les autoroutes cellulaires façonnent le câblage cérébral
À l’intérieur de chaque cellule nerveuse circule un réseau de tubes microscopiques qui fonctionnent comme des autoroutes, transportant signaux et fournitures sur de longues distances. Pour que le cerveau fonctionne, notamment lorsque les neurones allongent leurs axones, ces voies doivent être à la fois robustes et finement réglées. Cette étude examine ces tubes au sein de neurones humains proches du vivant avec un détail quasi‑atomique et montre que les « chaussées » axonales utilisent une stratégie inattendue pour rester stables — une stratégie qui pourrait aider à expliquer comment les neurones se développent, comment le trafic le long des axones est contrôlé, et pourquoi certains médicaments cérébraux agissent comme ils le font.
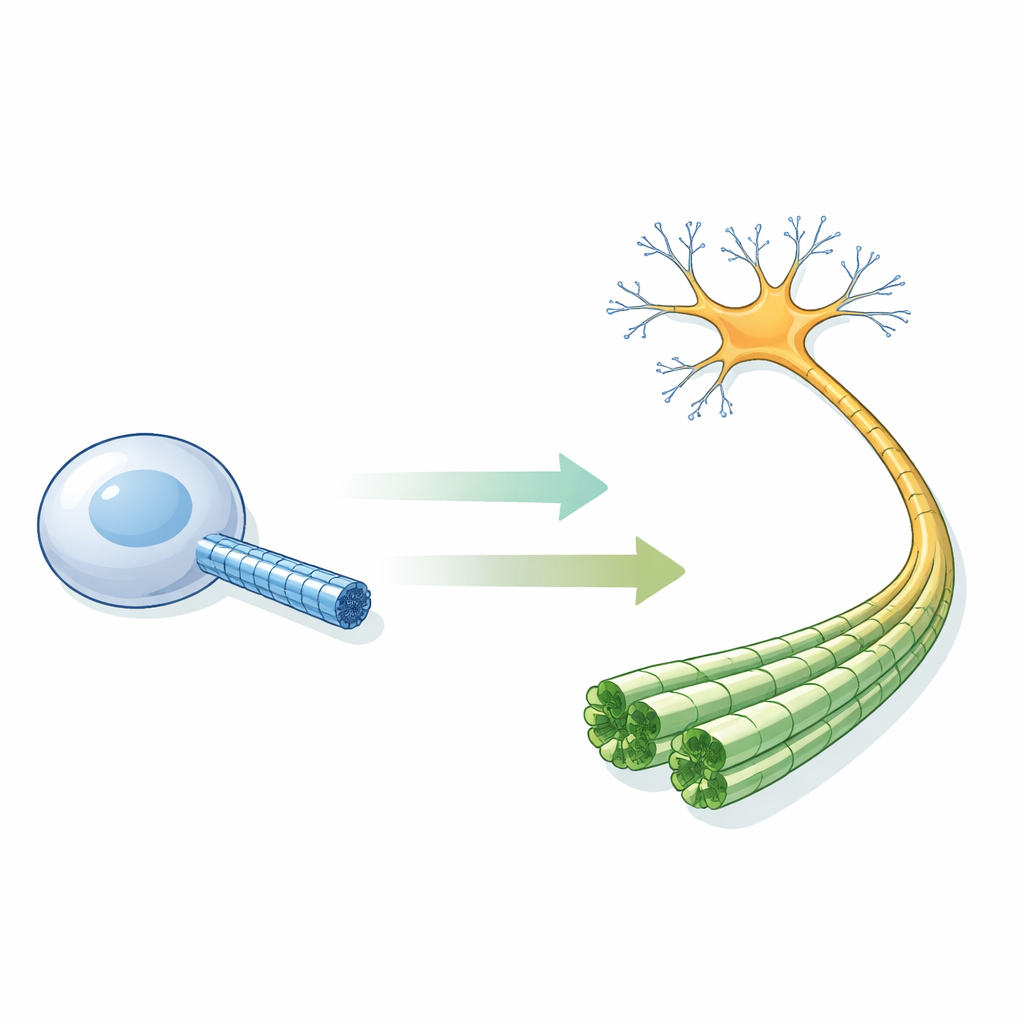
Petits tubes qui maintiennent les neurones
Les microtubules sont des cylindres creux constitués de blocs protéiques répétés et présents dans presque toutes nos cellules. Dans les neurones ils sont particulièrement cruciaux : regroupés en faisceaux parallèles serrés, ils donnent leur forme aux axones et servent de rails pour les protéines motrices qui acheminent la cargaison entre le corps cellulaire et les synapses éloignées. Des expériences en éprouvette ont longtemps suggéré une règle simple : lorsque les sous‑unités portent une molécule de GTP, la paroi du tube adopte une conformation « étendue » et est stable ; après hydrolyse du GTP en GDP, la paroi se compacte et le tube devient fragile et susceptible de se désassembler. Mais personne n’avait encore observé, à résolution atomique, à quoi ressemblent ces microtubules à l’intérieur d’un vrai neurone humain.
Voir les autoroutes axonales atome par atome
Les auteurs ont fait croître des neurones humains à partir de cellules souches pluripotentes induites et les ont encouragés à former des amas sphériques qui étendaient de longs axones à travers des grilles spéciales pour microscope électronique. En utilisant la cryo‑microscopie électronique et la tomographie de pointe, ils ont enregistré des milliers d’images de microtubules au sein d’axones intacts figés dans un état proche du naturel. En moyennant informatiquement de nombreuses vues, ils ont obtenu une reconstruction à 2,7 angströms — suffisamment fine pour distinguer les deux tubulines apparentées, localiser les nucléotides liés, et même résoudre des molécules d’eau ordonnées et des ions métalliques. Ils ont ainsi pu déterminer non seulement l’espacement entre les blocs le long de chaque protofilament, mais aussi l’état chimique exact de ces blocs.
Une maille stable qui défie les règles habituelles
La structure à haute résolution a livré une surprise. Dans les microtubules axonaux, le site échangeable de la β‑tubuline portait clairement du GDP, indiquant que le GTP avait été hydrolysé comme prévu. Pourtant, l’espacement entre les paires de tubuline le long du tube était étendu, correspondant à ce qui avait auparavant été observé uniquement dans des mailles stables de type GTP fabriquées in vitro. Une comparaison détaillée avec des structures connues a révélé un état hybride : des régions de la protéine qui détectent la présence du γ‑phosphate se comportaient comme dans des microtubules classiques liés au GDP, tandis que des éléments plus éloignés — en particulier un segment mobile appelé boucle T5 à la jonction entre dimères voisins — adoptaient la conformation étendue de type GTP. Une chaîne d’acides aminés aromatiques semble transmettre les mouvements de cette boucle aux contacts voisins, verrouillant la maille axonale dans une configuration étirée et stable malgré sa chimie en GDP.
Changer d’état au fur et à mesure de la maturation neuronale
Pour savoir si cette géométrie inhabituelle était une caractéristique spécifique des axones matures, l’équipe a mesuré l’espacement de la maille dans d’autres contextes en utilisant la tomographie cryo‑électronique et l’analyse du spectre de puissance. Dans les cellules souches indifférenciées, les microtubules présentaient un espacement plus compact, correspondant étroitement aux microtubules liés au GDP assemblés en éprouvette. En revanche, les microtubules au sein des axones de neurones différenciés affichaient un espacement étendu, similaire à la structure atomique observée dans l’axone et aux mailles in vitro stabilisées par des analogues non hydrolysables du GTP ou par le médicament Taxol. Cette transition d’une géométrie compacte à une géométrie étendue semble donc faire partie du programme de différenciation neuronale, coïncidant avec le besoin de stabiliser de longs prolongements axonaux et de les réorganiser en faisceaux denses.
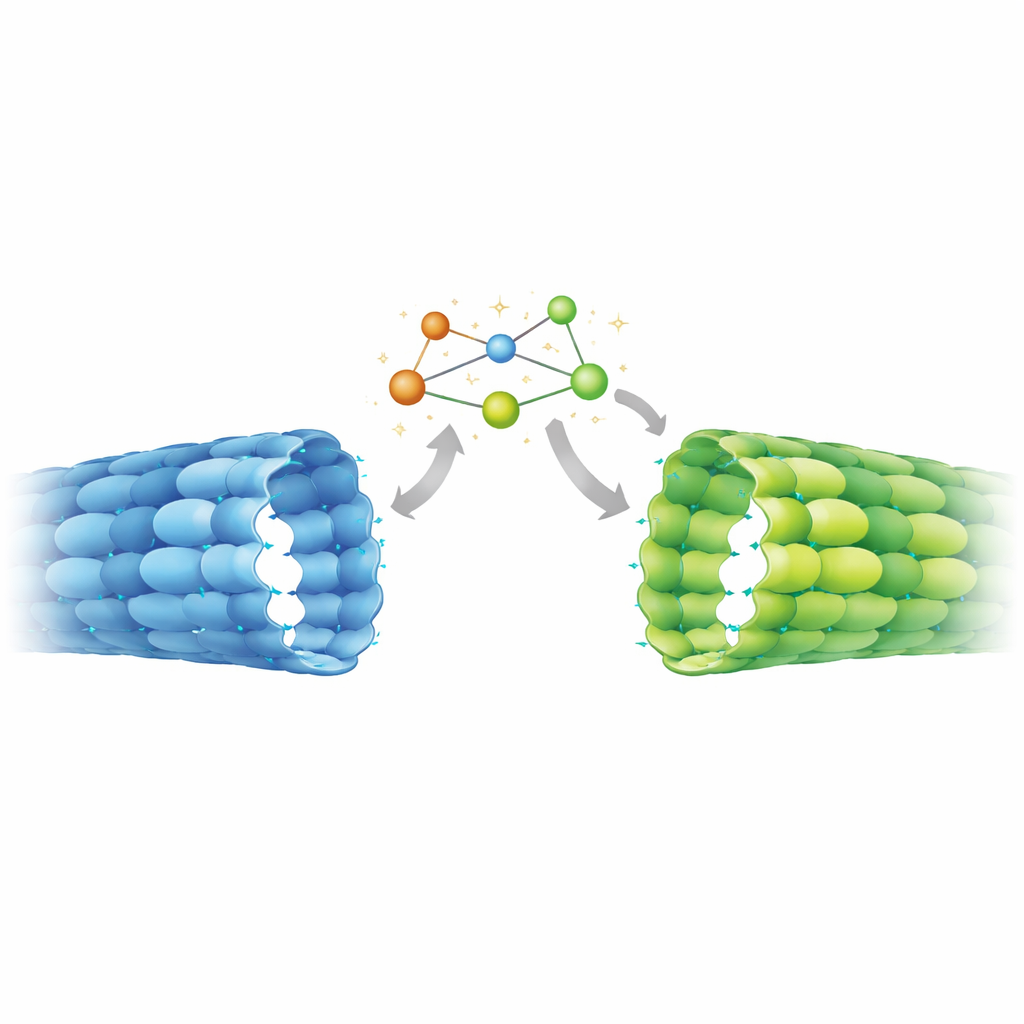
Implications pour la fonction cérébrale et la thérapie
Ce travail montre que les microtubules axonaux sont chimiquement à l’état GDP mais structurellement dans une forme étendue de type GTP, stabilisée par un commutateur mécanique interne. Cela signifie que les moteurs, protéines régulatrices et enzymes qui se lient aux microtubules dans les neurones interagissent avec un type de maille qui n’est pas fidèlement reproduit par de nombreuses préparations de laboratoire standard. Parce que ces effecteurs peuvent eux‑mêmes favoriser un espacement étendu ou compact — et que certaines modifications chimiques de la tubuline préfèrent des mailles étendues —, l’état découvert s’inscrit probablement dans une boucle de rétroaction qui ajuste le transport de cargaison et la longévité des microtubules pendant le développement cérébral. Les résultats suggèrent aussi que des médicaments comme le Taxol, connus pour élargir la maille, peuvent favoriser la croissance axonale en poussant les microtubules vers la même conformation stable qui apparaît naturellement au cours du câblage neuronal.
Citation: Zehr, E.A., Sun, S., Sarbanes, S.L. et al. Microtubules in the axon are GDP bound but adopt a stable GTP-like expanded state. Nat Struct Mol Biol 33, 631–640 (2026). https://doi.org/10.1038/s41594-026-01787-7
Mots-clés: microtubules, axone, différenciation neuronale, cryo‑microscopie électronique, cytosquelette