Clear Sky Science · de
Mikrotubuli im Axon sind GDP‑gebunden, nehmen aber einen stabilen, GTP‑ähnlich expandierten Zustand an
Wie Zell‑Autobahnen die Verschaltung des Gehirns formen
Im Inneren jeder Nervenzelle verläuft ein Netz winziger Röhren, die wie Autobahnen funktionieren und Signale und Versorgung über lange Strecken transportieren. Damit das Gehirn funktioniert, insbesondere wenn Nervenzellen lange Axone ausbilden, müssen diese Autobahnen sowohl stabil als auch fein abgestimmt sein. Diese Studie gewährt einen Blick auf diese Röhren in lebensecht wirkenden menschlichen Neuronen in nahezu atomarer Detailauflösung und zeigt, dass axonale "Straßen" eine unerwartete Strategie zur Stabilisierung nutzen — eine, die erklären helfen könnte, wie Neuronen sich entwickeln, wie der Verkehr entlang von Axonen gesteuert wird und warum bestimmte Wirkstoffe im Gehirn so wirken, wie sie es tun.
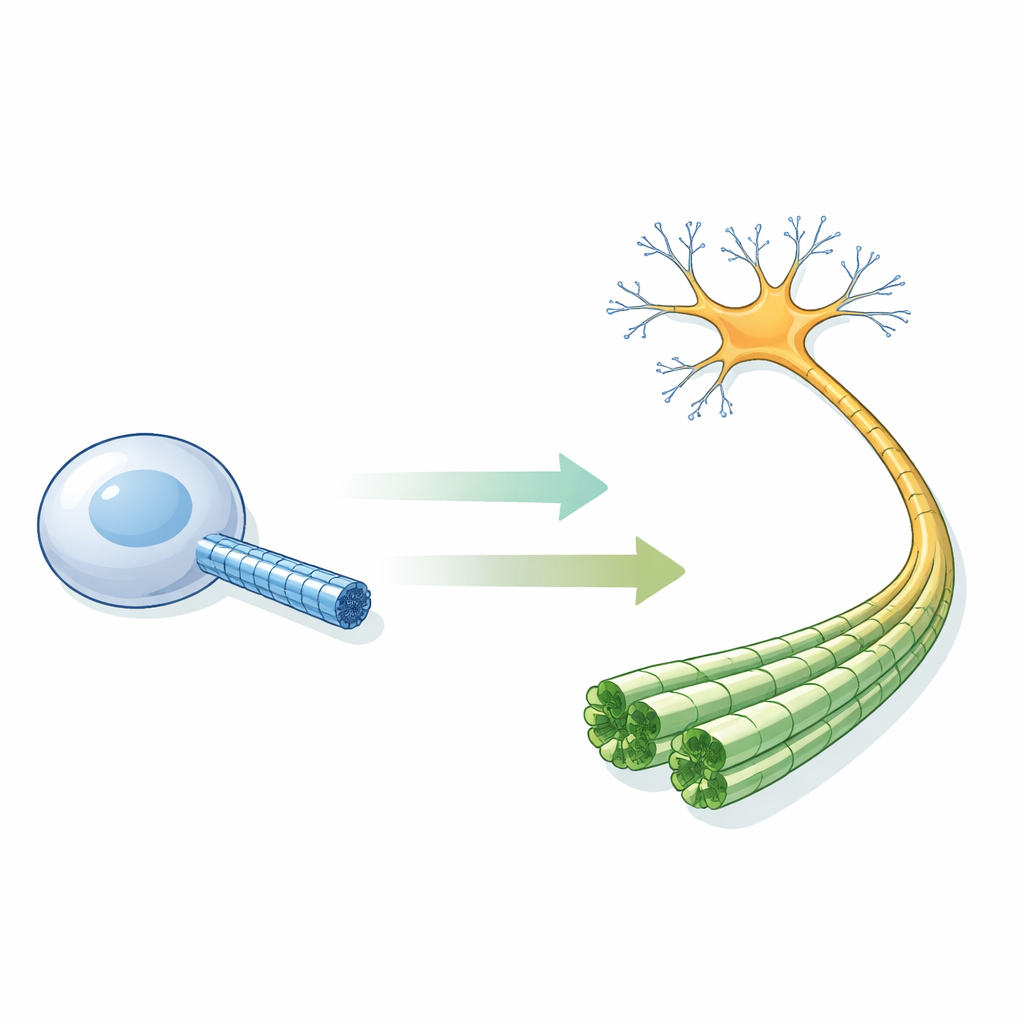
Winzige Röhren, die Neuronen am Laufen halten
Mikrotubuli sind hohle Zylinder aus sich wiederholenden Proteinbausteinen und kommen in nahezu allen Zellen vor. In Neuronen sind sie besonders wichtig: eng gebündelt in parallelen Arrays verleihen sie Axonen ihre Form und dienen als Schienen für Motorproteine, die Fracht zwischen Zellkörper und entfernten Synapsen transportieren. Reagenzglas‑Experimente legten lange eine einfache Regel nahe: tragen die Bausteine GTP, nimmt die Rohrwand eine „expandierte“ Form an und ist stabil; nach der Hydrolyse von GTP zu GDP kompaktieren die Bausteine, das Rohr wird brüchig und neigt dazu, sich aufzulösen. Aber noch nie hatte man im atomaren Detail gesehen, wie diese Mikrotubuli innerhalb einer echten menschlichen Nervenzelle aussehen.
Axonale Autobahnen Atom für Atom sehen
Die Autoren züchteten menschliche Neuronen aus induzierten pluripotenten Stammzellen und regten sie an, kugelförmige Cluster zu bilden, die lange Axone über spezielle Raster für das Elektronenmikroskop ausstreckten. Mit modernster Kryo‑Elektronenmikroskopie und Tomographie dokumentierten sie Tausende von Aufnahmen von Mikrotubuli in intakten, in einem naturnahen Zustand eingefrorenen Axonen. Durch die computergestützte Mittelung vieler Ansichten erzielten sie eine Rekonstruktion mit 2,7 Å Auflösung — fein genug, um die beiden verwandten Tubulin‑Proteine zu unterscheiden, die gebundenen Nukleotide zu identifizieren und sogar geordnete Wassermoleküle und Metallionen aufzulösen. So konnten sie nicht nur messen, wie weit die Bausteine entlang jedes Protofilaments voneinander entfernt sitzen, sondern auch genau bestimmen, in welchem chemischen Zustand diese Bausteine vorlagen.
Ein stabiles Gitter, das die üblichen Regeln bricht
Die hochaufgelöste Struktur lieferte eine Überraschung. In axonalen Mikrotubuli hielt die austauschbare Stelle in β‑Tubulin eindeutig GDP, was anzeigt, dass GTP wie erwartet hydrolysiert worden war. Dennoch war der Abstand zwischen Tubulinpaaren entlang des Rohres expandiert und entsprach dem, was zuvor nur in GTP‑ähnlichen, stabilen Gittern in vitro beobachtet worden war. Detaillierte Vergleiche mit bekannten Strukturen enthüllten einen Hybridzustand: Bereiche des Proteins, die das Vorhandensein der γ‑Phosphatgruppe wahrnehmen, verhielten sich wie klassische GDP‑Mikrotubuli, während weiter entfernte Elemente — insbesondere ein bewegliches Segment, die T5‑Schleife an der Grenze zwischen benachbarten Dimeren — die expandierte, GTP‑ähnliche Anordnung einnahmen. Eine Kette aromatischer Aminosäuren scheint Bewegungen von dieser Schleife zu benachbarten Kontaktstellen weiterzuleiten und das axonale Gitter mechanisch in einer gestreckten, stabilen Konfiguration zu verriegeln, trotz seiner GDP‑Chemie.
Zustandswechsel während der neuronalen Reifung
Um herauszufinden, ob diese ungewöhnliche Geometrie ein Merkmal reifer Axone ist, maßen die Forschenden die Gitterabstände in anderen Kontexten mittels Kryo‑Elektronentomographie und Leistungsspektrumsanalyse. In undifferenzierten Stammzellen zeigten Mikrotubuli kompaktere Abstände, die stark mit in vitro zusammengesetzten GDP‑Mikrotubuli übereinstimmten. Im Gegensatz dazu wiesen Mikrotubuli innerhalb der Axone differenzierter Neuronen expandierte Abstände auf, ähnlich der axonalen Atomstruktur und den in vitro‑Gittern, die durch nicht‑hydrolysierbare GTP‑Analoga oder das Medikament Taxol stabilisiert wurden. Dieser Wechsel von kompakter zu expandierter Geometrie scheint daher Teil des Programms der neuronalen Differenzierung zu sein, zeitlich abgestimmt auf die Notwendigkeit, lange axonale Prozesse zu stabilisieren und in dichte Bündel umzustrukturieren.
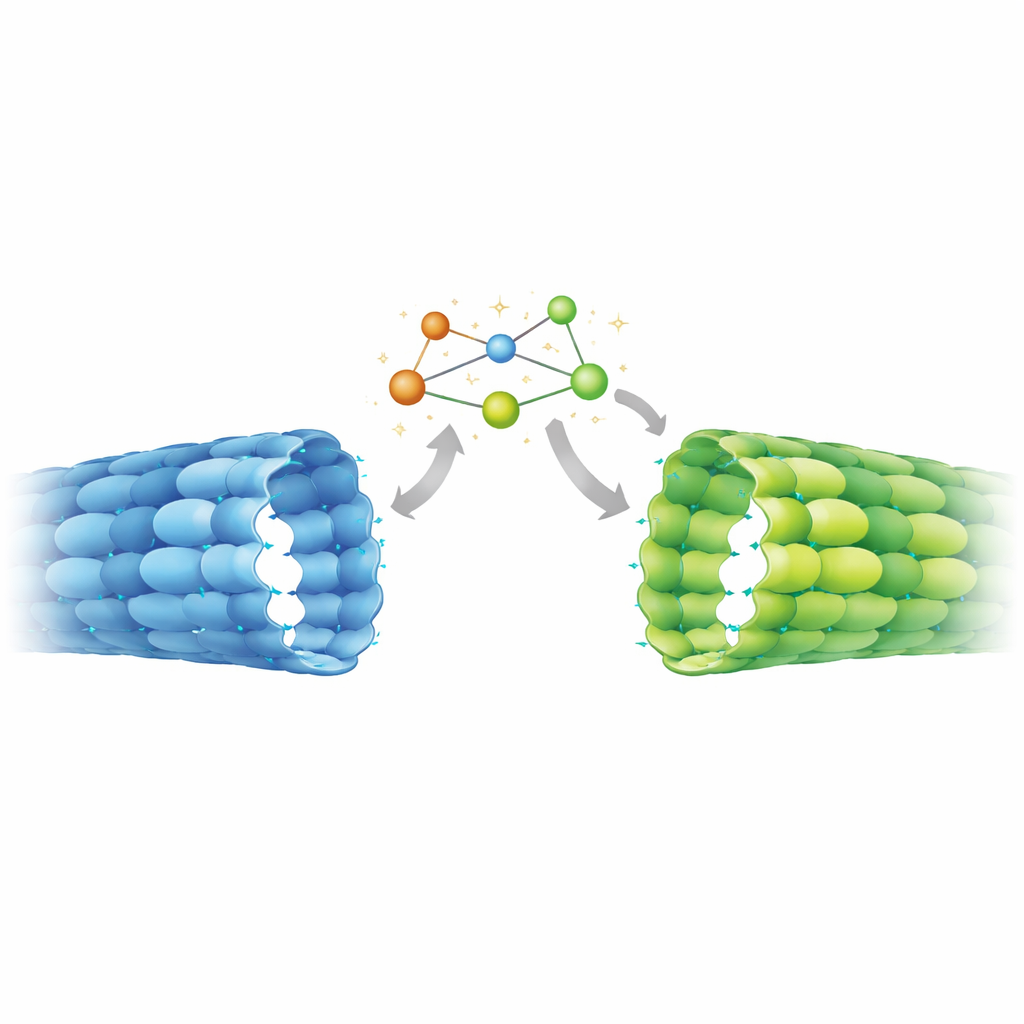
Folgen für Gehirnfunktion und Therapie
Diese Arbeit zeigt, dass axonale Mikrotubuli chemisch in einem GDP‑Zustand sind, strukturell jedoch eine GTP‑ähnlich expandierte Form einnehmen, stabilisiert durch einen internen mechanischen Schalter. Das bedeutet, dass Motoren, regulatorische Proteine und Enzyme, die Mikrotubuli in Neuronen schmücken, mit einem Gittertyp interagieren, der in vielen Standard‑Laborvorbereitungen nicht getreu nachgebildet wird. Da diese Effektoren selbst expandierte oder kompakte Abstände begünstigen können — und einige chemische Modifikationen an Tubulin expandierte Gitter bevorzugen — dürfte der entdeckte Zustand in eine Rückkopplungsschleife einfließen, die Frachttransport und Mikrotubuli‑Langlebigkeit während der Gehirnentwicklung fein abstimmt. Die Ergebnisse deuten außerdem an, dass Wirkstoffe wie Taxol, die das Gitter erweitern, das Axonwachstum teilweise fördern könnten, indem sie Mikrotubuli in dieselbe stabile Konformation drängen, die natürlicherweise beim Vernetzen von Neuronen entsteht.
Zitation: Zehr, E.A., Sun, S., Sarbanes, S.L. et al. Microtubules in the axon are GDP bound but adopt a stable GTP-like expanded state. Nat Struct Mol Biol 33, 631–640 (2026). https://doi.org/10.1038/s41594-026-01787-7
Schlüsselwörter: Mikrotubuli, Axon, neurale Differenzierung, Kryo‑Elektronenmikroskopie, Zytoskelett