Clear Sky Science · it
I microtubuli nell'assone contengono GDP ma adottano uno stato espanso stabile simile al GTP
Come le autostrade cellulari modellano il cablaggio del cervello
All'interno di ogni cellula nervosa corre una rete di tubi microscopici che funzionano come autostrade, trasportando segnali e rifornimenti su lunghe distanze. Perché il cervello funzioni, specialmente quando le cellule nervose sviluppano lunghi assoni, queste vie devono essere insieme robuste e finemente regolate. Questo studio osserva questi tubi all'interno di neuroni umani in condizioni vicine al naturale a dettaglio quasi atomico e scopre che le «strade» assonali usano una strategia inaspettata per restare stabili — una spiegazione potenziale di come i neuroni si sviluppano, di come viene regolato il traffico lungo gli assoni e del motivo per cui alcuni farmaci cerebrali agiscono in un certo modo.
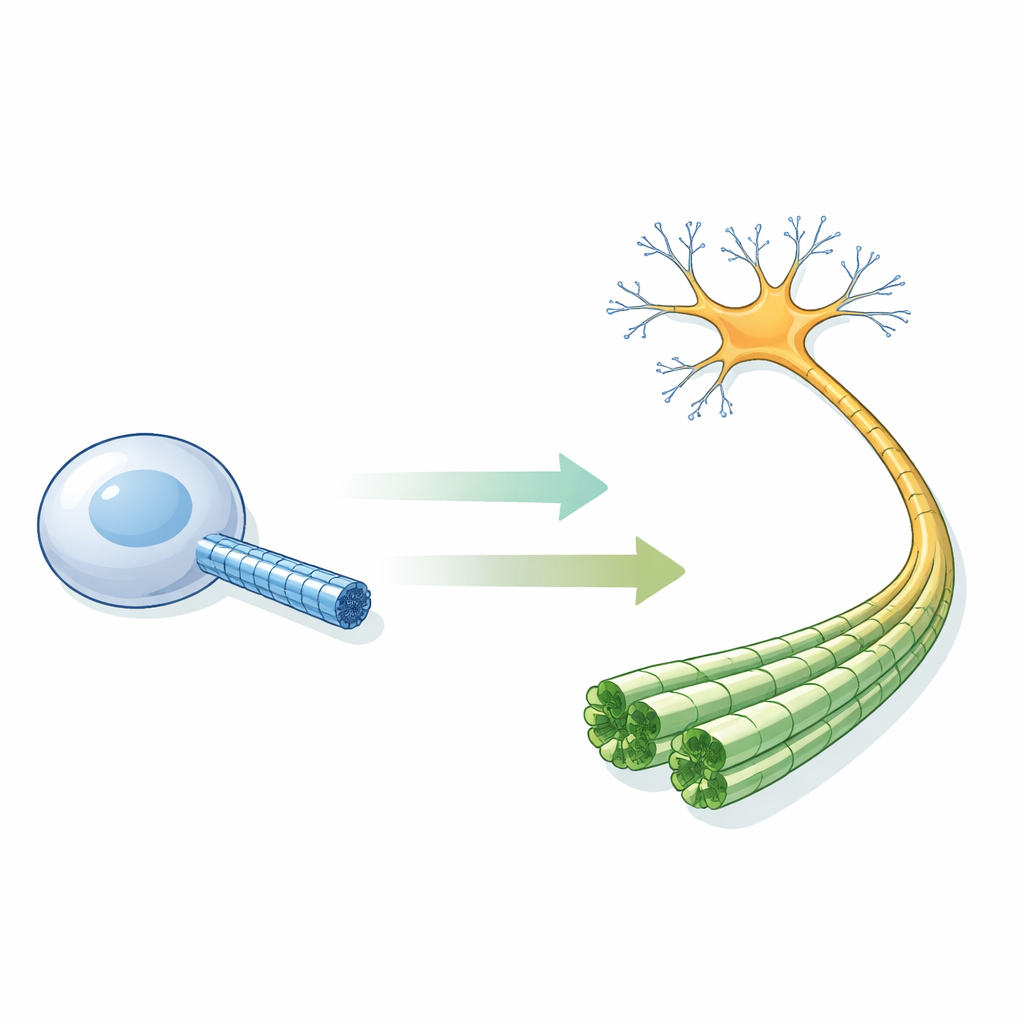
Piccoli tubi che mantengono vivi i neuroni
I microtubuli sono cilindri cavi costruiti da blocchi proteici ripetuti e attraversano quasi tutte le nostre cellule. Nei neuroni sono particolarmente cruciali: raggruppati in array paralleli stretti, danno forma agli assoni e fungono da binari per le proteine motrici che trasportano carichi tra il corpo cellulare e le sinapsi lontane. Esperimenti in provetta avevano a lungo suggerito una regola semplice: quando i mattoni proteici legano una molecola di GTP, la parete del tubo adotta una conformazione «espansa» ed è stabile; dopo che il GTP viene idrolizzato a GDP, la parete si compatta e il tubo diventa fragile e soggetto a disfarsi. Ma nessuno aveva mai osservato, a risoluzione atomica, come appaiono questi microtubuli dentro un vero neurone umano.
Osservare le autostrade assonali atomo per atomo
Gli autori hanno fatto crescere neuroni umani a partire da cellule staminali pluripotenti indotte e li hanno incoraggiati a formare aggregati sferici che estendevano lunghi assoni attraverso griglie speciali per microscopia elettronica. Usando una crio‑microscopia elettronica e tomografia all'avanguardia, hanno registrato migliaia di immagini di microtubuli all'interno di assoni intatti congelati in uno stato vicino al naturale. Mediante l'avgmento computazionale di molte visuali hanno ottenuto una ricostruzione a 2,7 ångström — sufficientemente fine da distinguere le due tubuline correlate, identificare i nucleotidi legati e persino risolvere molecole d'acqua ordinate e ioni metallici. Hanno così potuto determinare non solo la distanza tra i blocchi lungo ciascun protofilamento, ma anche esattamente in quale stato chimico si trovassero quei blocchi.
Un reticolo stabile che infrange le regole abituali
La struttura ad alta risoluzione ha riservato una sorpresa. Nei microtubuli assonali, il sito scambiabile nella β‑tubulina mostrava chiaramente GDP, indicando che il GTP era stato idrolizzato come previsto. Eppure l'intervallo tra le coppie di tubulina lungo il tubo era espanso, corrispondente a quanto osservato in precedenza solo nei reticoli stabili in vitro simili al GTP. Il confronto dettagliato con strutture note ha rivelato uno stato ibrido: regioni della proteina che rilevano la presenza del γ‑fosfato si comportavano come nei classici microtubuli con GDP, mentre elementi più distanti — in particolare un segmento mobile chiamato loop T5 alla giunzione tra dimeri adiacenti — adottavano l'assetto espanso simile al GTP. Una catena di aminoacidi aromatici sembra trasmettere i movimenti da questo loop ai contatti vicini, bloccando il reticolo assonale in una configurazione allungata e stabile nonostante la chimica a base di GDP.
Transizioni di stato durante la maturazione neuronale
Per stabilire se questa geometria insolita fosse una caratteristica speciale degli assoni maturi, il team ha misurato lo spaziamento del reticolo in altri contesti usando tomografia crioelettronica e analisi dello spettro di potenza. Nelle cellule staminali indifferenziate i microtubuli mostravano uno spaziamento più compatto, corrispondente da vicino ai microtubuli GDP assemblati in provetta. Al contrario, i microtubuli all'interno degli assoni di neuroni differenziati presentavano uno spaziamento espanso, simile alla struttura atomica assonale e ai reticoli in vitro stabilizzati da mimetici non idrolizzabili del GTP o dal farmaco Taxol. Questo passaggio da una geometria compatta a una espansa sembra quindi far parte del programma di differenziazione neuronale, coincidente con la necessità di stabilizzare processi assonali lunghi e riorganizzarli in fasci densi.
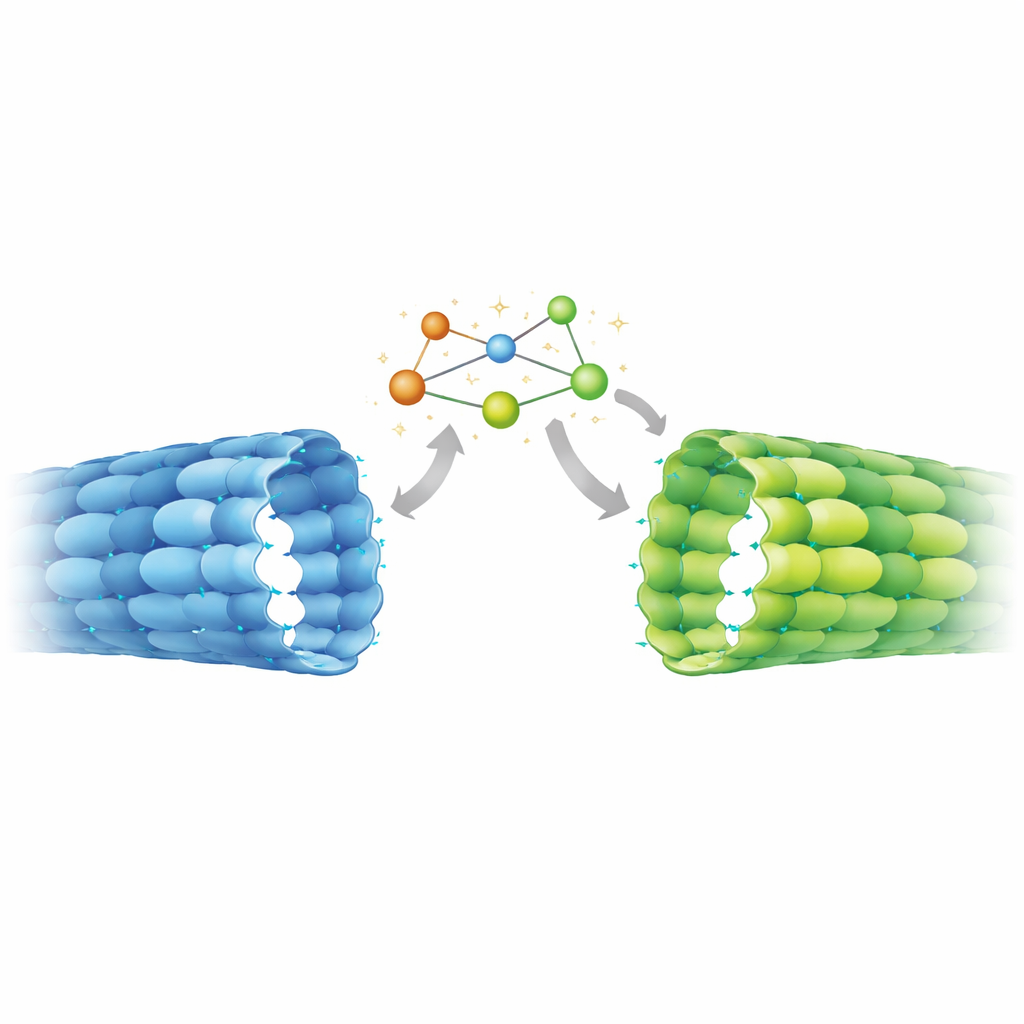
Implicazioni per funzione cerebrale e terapia
Questo lavoro mostra che i microtubuli assonali sono chimicamente in uno stato GDP ma strutturalmente in una forma espansa simile al GTP, stabilizzata da un interruttore meccanico interno. Ciò significa che motori, proteine regolatorie ed enzimi che decorano i microtubuli nei neuroni interagiscono con un tipo di reticolo non fedelmente ricreato da molte preparazioni standard di laboratorio. Poiché questi effettori possono a loro volta favorire spaziamenti espansi o compatti — e alcune modifiche chimiche alla tubulina preferiscono reticoli espansi — lo stato descritto probabilmente alimenta un circuito di retroazione che regola il trasporto di carico e la longevità dei microtubuli durante lo sviluppo cerebrale. I risultati suggeriscono inoltre che farmaci come il Taxol, noti per espandere il reticolo, potrebbero promuovere la crescita degli assoni in parte spingendo i microtubuli verso la stessa conformazione stabile che si manifesta naturalmente durante il cablaggio neuronale.
Citazione: Zehr, E.A., Sun, S., Sarbanes, S.L. et al. Microtubules in the axon are GDP bound but adopt a stable GTP-like expanded state. Nat Struct Mol Biol 33, 631–640 (2026). https://doi.org/10.1038/s41594-026-01787-7
Parole chiave: microtubuli, assone, differenziazione neuronale, crio-microscopia elettronica, cito scheletro