Clear Sky Science · es
Los microtúbulos en el axón están unidos a GDP pero adoptan un estado expandido estable parecido al GTP
Cómo las autopistas celulares moldean el cableado cerebral
Dentro de cada neurona corre una red de tubos microscópicos que actúan como autopistas, transportando señales y suministros a lo largo de grandes distancias. Para que el cerebro funcione, especialmente cuando las neuronas extienden largos axones, estas vías deben ser a la vez robustas y finamente reguladas. Este estudio observa esas estructuras dentro de neuronas humanas con aspecto casi vivo a detalle cercano al atómico y descubre que las “carreteras” axonales usan una estrategia inesperada para mantenerse estables, una que podría ayudar a explicar cómo se desarrollan las neuronas, cómo se controla el tráfico a lo largo de los axones y por qué ciertos medicamentos cerebrales actúan como lo hacen.
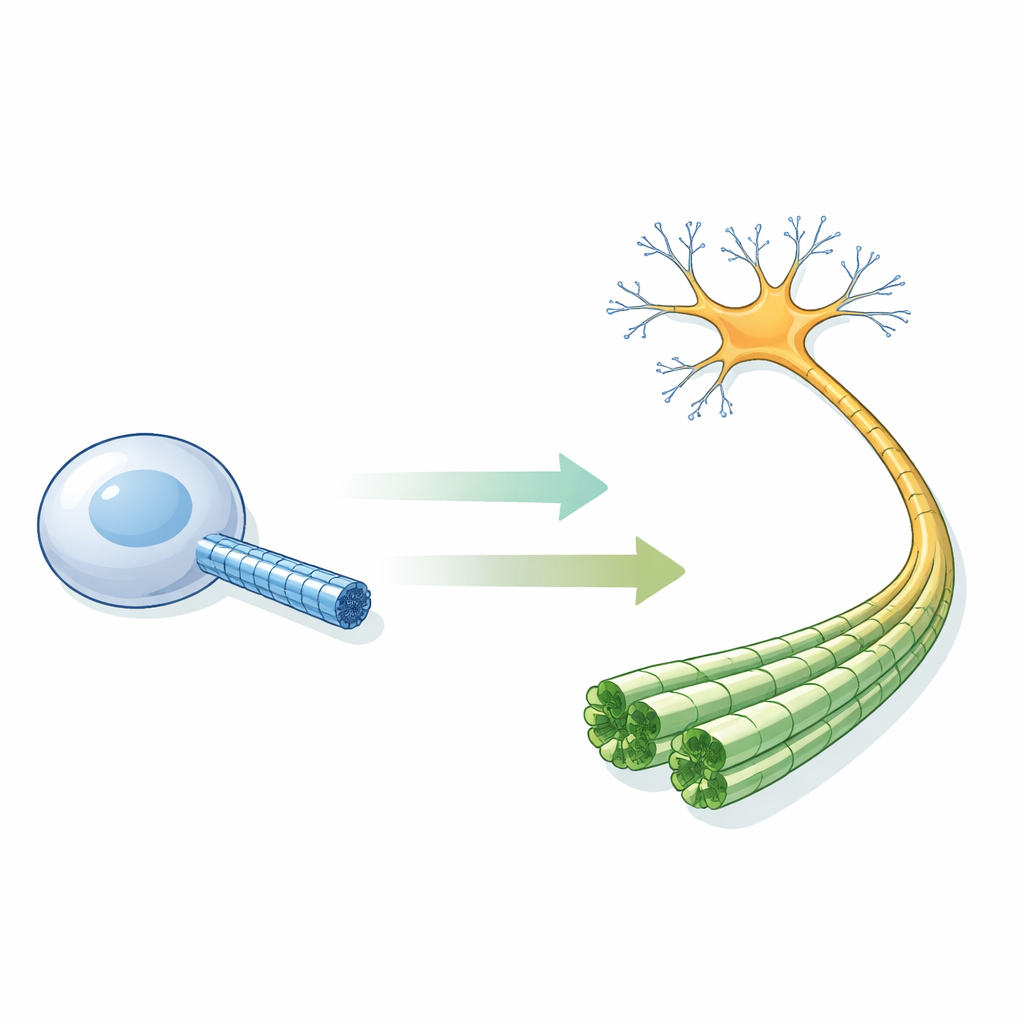
Tubos diminutos que mantienen vivas a las neuronas
Los microtúbulos son cilindros huecos formados por bloques proteicos repetidos y atraviesan casi todas nuestras células. En las neuronas son especialmente cruciales: agrupados en arreglos paralelos compactos, dan forma a los axones y sirven de vías para proteínas motoras que transportan carga entre el soma y sinapsis distantes. Experimentos in vitro habían sugerido una regla simple: cuando los bloques llevan un nucleótido GTP, la pared del tubo adopta una forma “expandida” y es estable; tras la hidrólisis del GTP a GDP, la pared se compacta y el tubo se vuelve frágil y propenso a desintegrarse. Pero nadie había visto, a resolución atómica, cómo son estos microtúbulos dentro de una neurona humana real.
Ver las autopistas axonales átomo a átomo
Los autores cultivaron neuronas humanas a partir de células madre pluripotentes inducidas y las animaron a formar racimos esféricos que extendieron largos axones sobre rejillas especiales para microscopía electrónica. Usando cryo‑microscopía electrónica y tomografía de última generación, registraron miles de imágenes de microtúbulos dentro de axones intactos congelados en un estado casi natural. Mediante el promediado computacional de muchas vistas, obtuvieron una reconstrucción a 2,7 ångström, lo bastante fina para distinguir las dos proteínas relacionadas de tubulina, identificar los nucleótidos unidos e incluso resolver moléculas de agua ordenadas e iones metálicos. Así pudieron determinar no solo la separación entre los bloques a lo largo de cada protofilamento, sino también el estado químico exacto de esos bloques.
Una red estable que rompe las reglas habituales
La estructura de alta resolución ofreció una sorpresa. En los microtúbulos axonales, el sitio intercambiable en la β‑tubulina mostraba claramente GDP, indicando que el GTP se había hidrolizado como se esperaba. Sin embargo, la separación entre pares de tubulina a lo largo del tubo estaba expandida, coincidiendo con lo que antes solo se había observado en redes estables de tipo GTP obtenidas in vitro. La comparación detallada con estructuras conocidas reveló un estado híbrido: regiones de la proteína que detectan la presencia del γ‑fosfato se comportaban como en microtúbulos clásicos con GDP, mientras que elementos más distantes—especialmente un tramo móvil llamado lazo T5 en la unión entre dímeros vecinos—adoptaban el arreglo expandido, parecido al del GTP. Una cadena de aminoácidos aromáticos parece transmitir los movimientos desde este lazo a contactos adyacentes, bloqueando la red axonal en una configuración estirada y estable a pesar de su química ligada a GDP.
Cambio de estados durante la maduración neuronal
Para saber si esta geometría inusual era una característica especial de los axones maduros, el equipo midió el espaciado de la red en otros contextos usando tomografía cryo‑electrónica y análisis del espectro de potencia. En células madre no diferenciadas, los microtúbulos mostraban un espaciado más compacto, coincidiendo estrechamente con microtúbulos con GDP ensamblados en probeta. En contraste, los microtúbulos dentro de axones de neuronas diferenciadas mostraron un espaciado expandido, similar a la estructura atómica axonal y a las redes in vitro estabilizadas por análogos de GTP no hidrolizables o por el fármaco Taxol. Este cambio de una geometría compacta a otra expandida parece ser por tanto parte del programa de diferenciación neuronal, coincidiendo con la necesidad de estabilizar largos procesos axonales y reorganizarlos en haces densos.
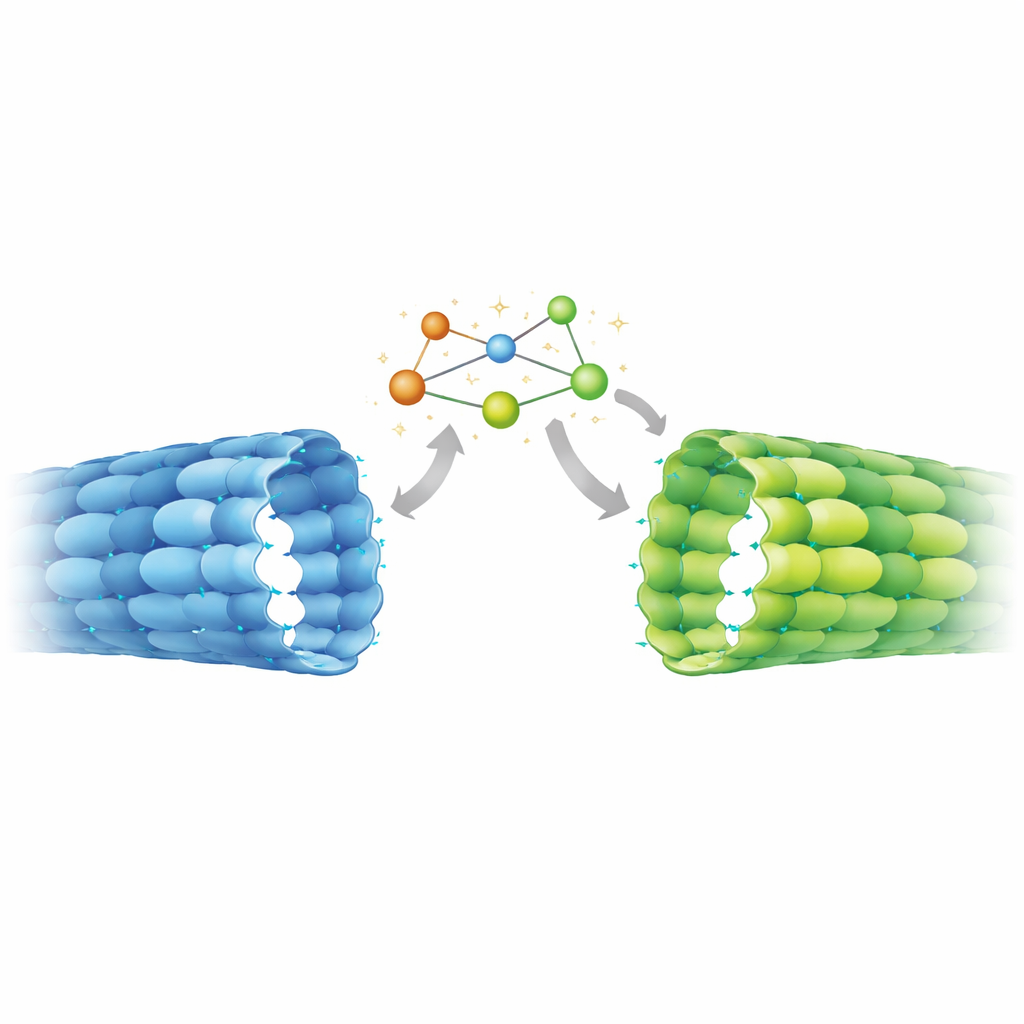
Implicaciones para la función cerebral y la terapia
Este trabajo demuestra que los microtúbulos axonales están químicamente en estado GDP pero estructuralmente en una forma expandida parecida al GTP, estabilizada por un interruptor mecánico interno. Eso significa que motores, proteínas reguladoras y enzimas que decoran los microtúbulos en las neuronas interactúan con un tipo de red que muchos preparados estándar de laboratorio no reproducen fielmente. Dado que estos efectores pueden favorecer por sí mismos un espaciado expandido o compacto—y algunas modificaciones químicas de la tubulina prefieren redes expandidas—el estado descubierto probablemente forma parte de un bucle de retroalimentación que ajusta el transporte de cargas y la longevidad de los microtúbulos durante el desarrollo cerebral. Los hallazgos también sugieren que fármacos como el Taxol, conocidos por expandir la red, pueden promover el crecimiento axonal en parte empujando a los microtúbulos hacia la misma conformación estable que aparece de forma natural durante el cableado neuronal.
Cita: Zehr, E.A., Sun, S., Sarbanes, S.L. et al. Microtubules in the axon are GDP bound but adopt a stable GTP-like expanded state. Nat Struct Mol Biol 33, 631–640 (2026). https://doi.org/10.1038/s41594-026-01787-7
Palabras clave: microtúbulos, axón, diferenciación neuronal, cryo‑microscopía electrónica