Clear Sky Science · pt
Microtúbulos no axônio estão ligados ao GDP, mas adotam um estado expandido estável semelhante ao GTP
Como as rodovias celulares moldam as conexões do cérebro
Dentro de cada neurônio percorre uma rede de tubos microscópicos que funcionam como rodovias, transportando sinais e suprimentos por longas distâncias. Para o cérebro funcionar, especialmente quando os neurônios estendem axônios longos, essas rodovias precisam ser ao mesmo tempo robustas e finamente ajustadas. Este estudo investiga esses tubos dentro de neurônios humanos em estado quase vivo com detalhe próximo ao atômico e descobre que as “vias” axonais usam uma estratégia inesperada para se manterem estáveis — uma estratégia que pode ajudar a explicar como os neurônios se desenvolvem, como o tráfego ao longo dos axônios é regulado e por que certos fármacos cerebrais atuam da maneira que atuam.
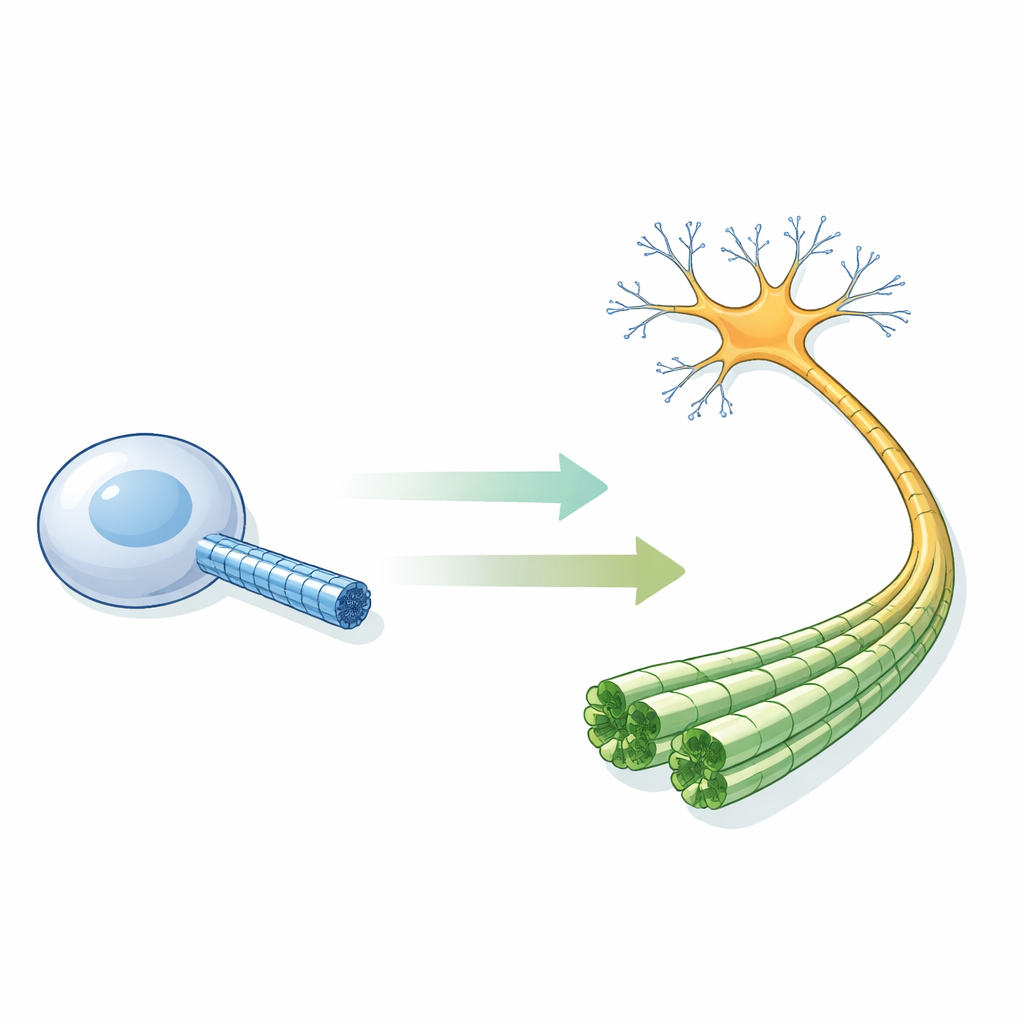
Pequenos tubos que mantêm os neurônios funcionando
Microtúbulos são cilindros ocos construídos a partir de blocos proteicos repetitivos e percorrem quase todas as nossas células. Nos neurônios são especialmente cruciais: agrupados em arranjos paralelos apertados, dão forma aos axônios e servem como trilhos para proteínas motoras que transportam cargas entre o corpo celular e sinapses distantes. Experimentos em tubo de ensaio há muito sugerem uma regra simples: quando os blocos carregam uma molécula de GTP, a parede do tubo adota uma forma “expandida” e é estável; depois que o GTP é hidrolisado para GDP, a parede se compacta e o tubo fica frágil e propenso a se desmontar. Mas ninguém havia visto, em resolução atômica, como esses microtúbulos se apresentam dentro de um neurônio humano real.
Vendo as rodovias axonais átomo a átomo
Os autores cultivaram neurônios humanos a partir de células‑tronco pluripotentes induzidas e os incentivaram a formar aglomerados esféricos que estendiam longos axônios sobre grades especiais para microscopia eletrônica. Usando crio‑microscopia eletrônica e tomografia de última geração, registraram milhares de imagens de microtúbulos dentro de axônios intactos congelados em um estado quase natural. Ao fazer a média computacional de muitas visões, alcançaram uma reconstrução de 2,7 ångström — precisa o suficiente para distinguir as duas proteínas tubulina relacionadas, identificar os nucleotídeos ligados e até resolver moléculas de água ordenadas e íons metálicos. Assim, puderam determinar não apenas o espaçamento entre os blocos ao longo de cada protofilamento, mas também exatamente qual era o estado químico desses blocos.
Uma rede estável que quebra as regras usuais
A estrutura de alta resolução trouxe uma surpresa. Nos microtúbulos axonais, o sítio trocável na β‑tubulina claramente continha GDP, indicando que o GTP havia sido hidrolisado como esperado. Ainda assim, o espaçamento entre pares de tubulina ao longo do tubo estava expandido, correspondendo ao que antes havia sido observado apenas em redes estáveis semelhantes ao GTP produzidas in vitro. A comparação detalhada com estruturas conhecidas revelou um estado híbrido: regiões da proteína que detectam a presença do fosfato γ comportavam‑se como microtúbulos clássicos com GDP, enquanto elementos mais distantes — especialmente um segmento móvel chamado alça T5 na junção entre dímeros vizinhos — adotavam o arranjo expandido, semelhante ao do GTP. Uma cadeia de aminoácidos aromáticos parece transmitir movimentos dessa alça para contatos adjacentes, travando a rede axonal em uma configuração esticada e estável apesar da sua química com GDP.
Trocando de estado conforme os neurônios amadurecem
Para descobrir se essa geometria incomum era uma característica especial de axônios maduros, a equipe mediu o espaçamento da rede em outros contextos usando tomografia por crio‑microscopia eletrônica e análise do espectro de potência. Em células‑tronco indiferenciadas, os microtúbulos mostraram espaçamento mais compacto, correspondendo de perto aos microtúbulos com GDP montados em tubo de ensaio. Em contraste, microtúbulos dentro de axônios de neurônios diferenciados exibiram espaçamento expandido, similar à estrutura atômica axonal e às redes in vitro estabilizadas por análogos de GTP não hidrolisáveis ou pelo fármaco Taxol. Essa mudança de geometria compacta para expandida, portanto, parece fazer parte do programa de diferenciação neuronal, coincidindo com a necessidade de estabilizar processos axonais longos e reorganizá‑los em feixes densos.
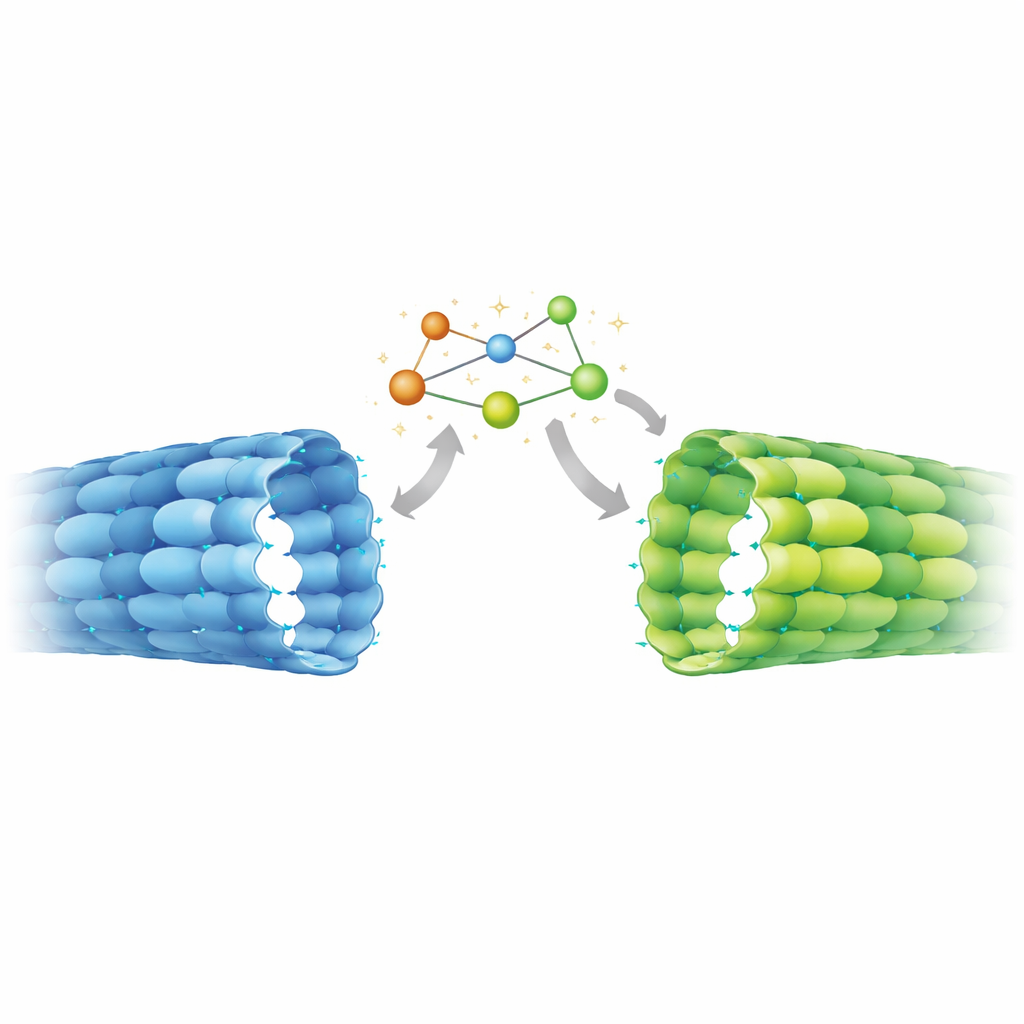
Implicações para a função cerebral e a terapia
Este trabalho mostra que os microtúbulos axonais estão quimicamente em um estado GDP, mas estruturalmente em uma forma expandida semelhante ao GTP, estabilizada por um interruptor mecânico interno. Isso significa que motores, proteínas reguladoras e enzimas que se ligam aos microtúbulos em neurônios interagem com um tipo de rede que muitos preparos experimentais padrão não imitam fielmente. Como esses efetores podem por si mesmos favorecer espaçamentos expandidos ou compactos — e algumas modificações químicas da tubulina preferem redes expandidas —, o estado descoberto provavelmente alimenta um circuito de retroalimentação que ajusta o transporte de cargas e a longevidade dos microtúbulos durante o desenvolvimento cerebral. Os achados também sugerem que fármacos como o Taxol, conhecidos por expandir a rede, podem promover o crescimento axonal em parte ao empurrar os microtúbulos para a mesma conformação estável que aparece naturalmente à medida que os neurônios formam conexões.
Citação: Zehr, E.A., Sun, S., Sarbanes, S.L. et al. Microtubules in the axon are GDP bound but adopt a stable GTP-like expanded state. Nat Struct Mol Biol 33, 631–640 (2026). https://doi.org/10.1038/s41594-026-01787-7
Palavras-chave: microtúbulos, axônio, diferenciação neuronal, crio‑microscopia eletrônica, citoesqueleto