Clear Sky Science · nl
Microtubuli in het axon binden GDP maar nemen een stabiele GTP‑achtige uitgezette toestand aan
Hoe cellulaire snelwegen de bedrading van de hersenen vormen
In elke zenuwcel loopt een netwerk van microscopische buisjes die fungeren als snelwegen en signalen en voorraden over grote afstanden vervoeren. Voor het goed functioneren van de hersenen, en vooral wanneer zenuwcellen lange axonen vormen, moeten deze snelwegen zowel stevig als nauwkeurig afgestemd zijn. Deze studie kijkt naar die buisjes in leven‑achtige menselijke neuronen met bijna atomaire resolutie en vindt dat axonale "wegvakken" een onverwachte strategie gebruiken om stabiel te blijven — een mechanisme dat kan helpen verklaren hoe neuronen zich ontwikkelen, hoe het verkeer langs axonen wordt gereguleerd en waarom bepaalde hersengeneesmiddelen werken zoals ze doen.
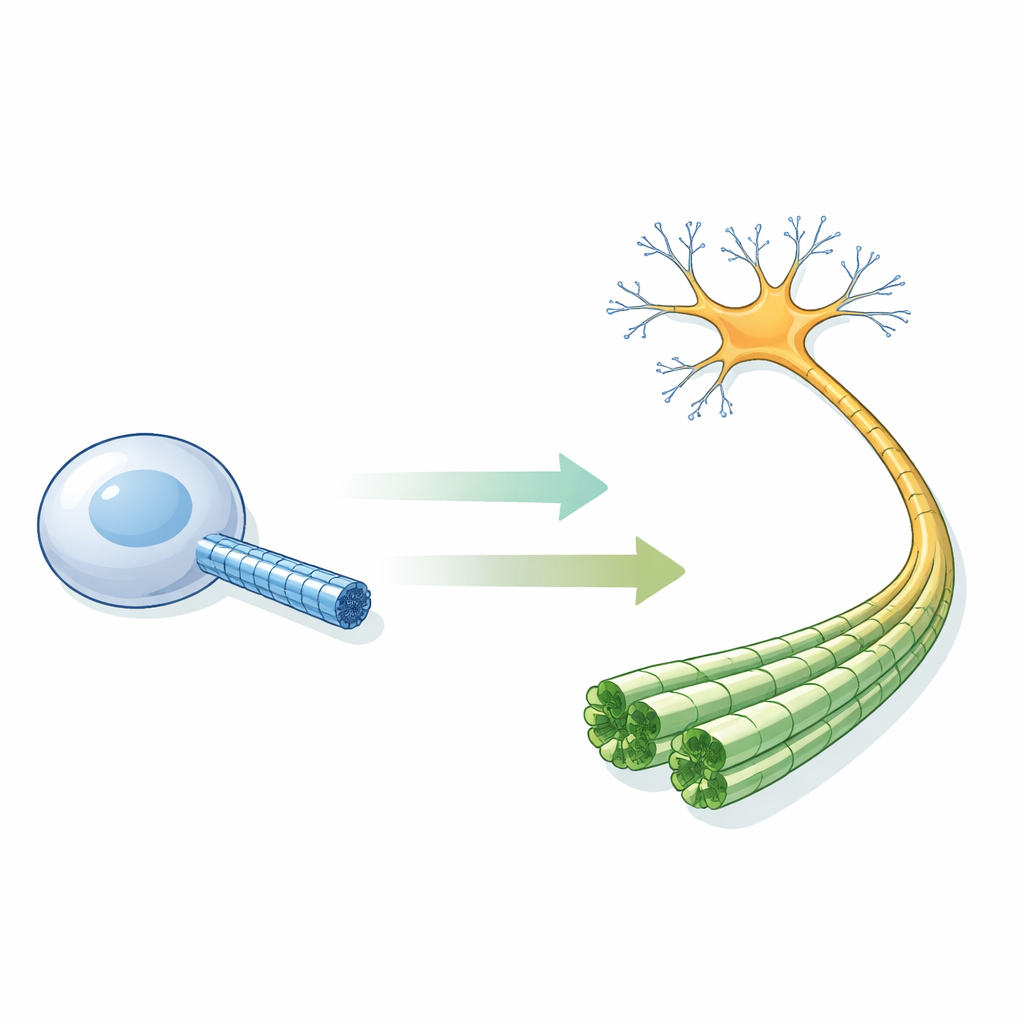
Kleine buisjes die neuronen in stand houden
Microtubuli zijn holle cilinders opgebouwd uit repeterende eiwitbouwstenen en komen in bijna al onze cellen voor. In neuronen zijn ze bijzonder cruciaal: gebundeld in strakke, parallelle arrays geven ze axonen hun vorm en dienen ze als sporen voor motorproteïnen die lading tussen het cellichaam en verre synapsen vervoeren. Proefbuisexperimenten suggereerden lange tijd een simpele regel: wanneer de bouwstenen een GTP‑molecuul dragen, neemt de wand een "uitgezette" vorm aan en is deze stabiel; nadat GTP is afgebroken tot GDP, compacteert de wand en wordt de buis broos en vatbaar om uiteen te vallen. Maar niemand had ooit, met atomaire resolutie, gezien hoe deze microtubuli eruitzien binnen een echte menselijke neuron.
Axonale snelwegen atoom voor atoom waarnemen
De auteurs lieten menselijke neuronen groeien uit geïnduceerde pluripotente stamcellen en brachten ze ertoe bolvormige clusters te vormen die lange axonen over speciale elektronenmicroscooproosters uitstrekten. Met state‑of‑the‑art kryo‑elektronenmicroscopie en tomografie registreerden ze duizenden beelden van microtubuli binnen intacte axonen, ingevroren in een bijna‑natuurlijke toestand. Door veel beelden computationeel te middelen bereikten ze een reconstructie van 2,7 ångström — nauw genoeg om de twee verwante tubuline‑eiwitten te onderscheiden, de gebonden nucleotiden te identificeren en zelfs geordend water en metaalionen te resolueren. Ze konden daardoor niet alleen bepalen hoe ver de bouwstenen langs elk protofilament van elkaar zitten, maar ook precies in welke chemische toestand die bouwstenen verkeerden.
Een stabiel lattice dat de gebruikelijke regels doorbreekt
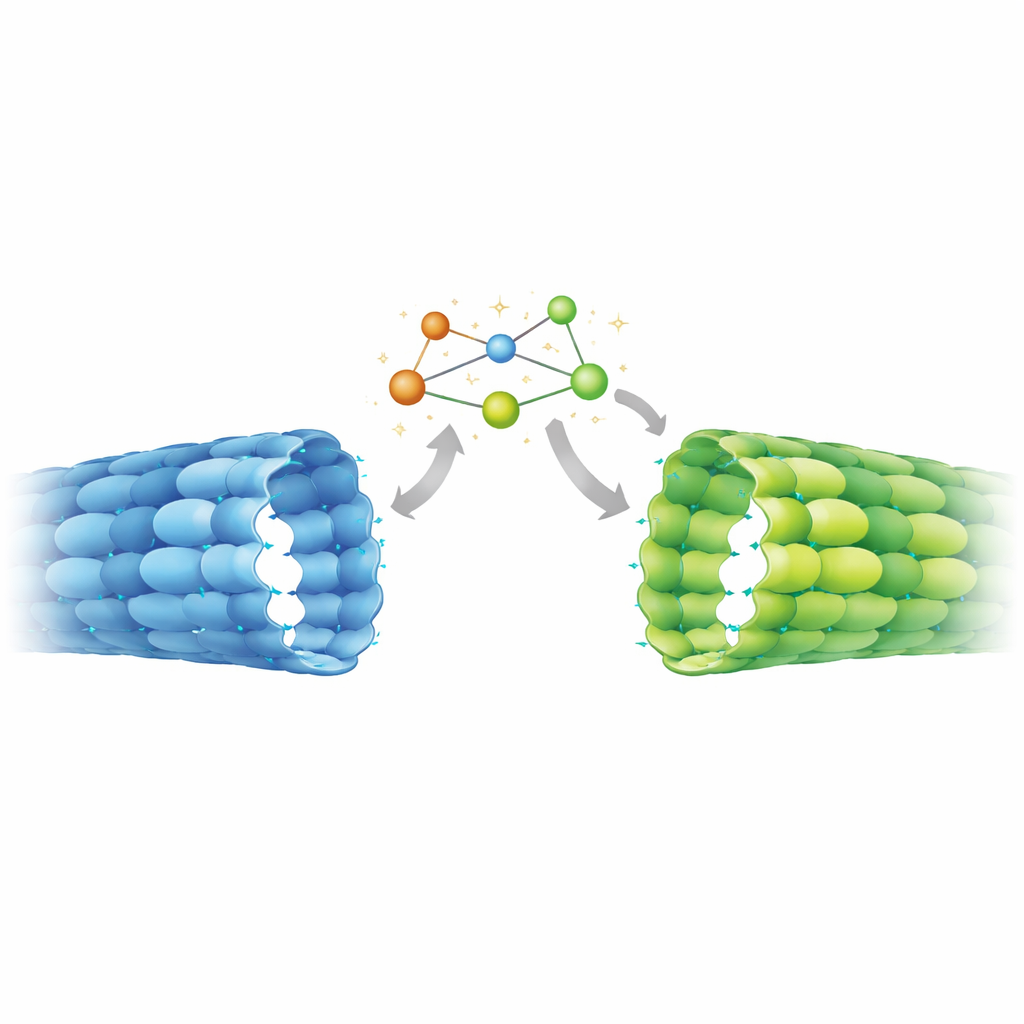
De structuur met hoge resolutie bracht een verrassing aan het licht. In axonale microtubuli hield de verwisselbare plaats in β‑tubuline duidelijk GDP vast, wat aangeeft dat GTP zoals verwacht gehydrolyseerd was. Toch was de afstand tussen tubulineparen langs de buis uitgezet, overeenkomend met wat eerder alleen werd gezien in GTP‑achtige, stabiele lattices gemaakt in vitro. Vergelijking met bekende structuren onthulde een hybride toestand: regio's van het eiwit die de aanwezigheid van het γ‑fosfaat waarnemen gedroegen zich als klassieke GDP‑microtubuli, terwijl elementen verder weg — vooral een beweeglijk segment genaamd de T5‑lus op de grens tussen aangrenzende dimeren — de uitgezette, GTP‑achtige configuratie aannamen. Een keten van aromatische aminozuren lijkt bewegingen van deze lus naar naburige contactpunten over te brengen, waardoor het axonale lattice in een uitgerekte, stabiele configuratie vergrendeld wordt ondanks de GDP‑chemie.
Toestandsschakeling terwijl neuronen rijpen
Om te onderzoeken of deze ongewone geometrie een speciaal kenmerk van rijpe axonen was, maten de onderzoekers de lattice‑afstand in andere contexten met kryo‑elektronentomografie en powerspectrum‑analyse. In niet‑gedifferentieerde stamcellen vertoonden microtubuli een meer compacte afstand, die nauw overeenkwam met GDP‑microtubuli geassembleerd in de proefbuis. In tegenstelling daarmee toonden microtubuli binnen axonen van gedifferentieerde neuronen uitgezette afstanden, vergelijkbaar met de axonale atomaire structuur en met in vitro lattices gestabiliseerd door niet‑hydrolyseerbare GTP‑mimetica of het geneesmiddel Taxol. Deze verschuiving van compacte naar uitgezette geometrie lijkt dus deel uit te maken van het neurale differentiatieprogramma, samenvallend met de noodzaak om lange axonale uitlopers te stabiliseren en ze te herschikken in dichte bundels.
Implicaties voor hersenfunctie en therapie
Dit werk toont aan dat axonale microtubuli chemisch in een GDP‑toestand verkeren, maar structureel in een GTP‑achtige uitgezette vorm — gestabiliseerd door een interne mechanische schakelaar. Dat betekent dat motoren, regulatorische eiwitten en enzymen die microtubuli in neuronen versieren, interacteren met een lattice‑type dat niet altijd getrouw wordt nagebootst door veel standaard laboratoriumpreparaten. Omdat deze effectoren zelf compacte of uitgezette afstanden kunnen bevorderen — en sommige chemische modificaties van tubuline de voorkeur geven aan uitgezette lattices — zal de ontdekte toestand waarschijnlijk deel uitmaken van een terugkoppelingslus die het vrachtvervoer en de levensduur van microtubuli tijdens hersenontwikkeling afstemt. De bevindingen suggereren ook dat geneesmiddelen zoals Taxol, waarvan bekend is dat ze het lattice uitzetten, axongroei gedeeltelijk kunnen bevorderen door microtubuli richting dezelfde stabiele conformatie te duwen die van nature verschijnt wanneer neuronen zich verbinden.
Bronvermelding: Zehr, E.A., Sun, S., Sarbanes, S.L. et al. Microtubules in the axon are GDP bound but adopt a stable GTP-like expanded state. Nat Struct Mol Biol 33, 631–640 (2026). https://doi.org/10.1038/s41594-026-01787-7
Trefwoorden: microtubuli, axon, neurale differentiatie, kryo-elektronenmicroscopie, cytoskelet