Clear Sky Science · pl
Mikrotubule w aksonie są związane z GDP, ale przyjmują stabilny, rozszerzony stan podobny do GTP
Jak komórkowe autostrady kształtują okablowanie mózgu
W każdej komórce nerwowej przebiega sieć mikroskopijnych rur, które działają jak autostrady — przewożą sygnały i zaopatrzenie na duże odległości. Aby mózg funkcjonował, zwłaszcza gdy neurony wydłużają swoje aksony, te szlaki muszą być jednocześnie wytrzymałe i precyzyjnie dostrojone. Badanie to zagląda do tych rurek w komórkach ludzkich przypominających żywe neurony z niemal atomową szczegółowością i wykrywa, że aksonalne „drogi” utrzymują stabilność za pomocą nieoczekiwanej strategii — co może pomóc wyjaśnić, jak neurony rozwijają się, jak kontrolowany jest ruch wzdłuż aksonów i dlaczego niektóre leki działają w taki, a nie inny sposób.
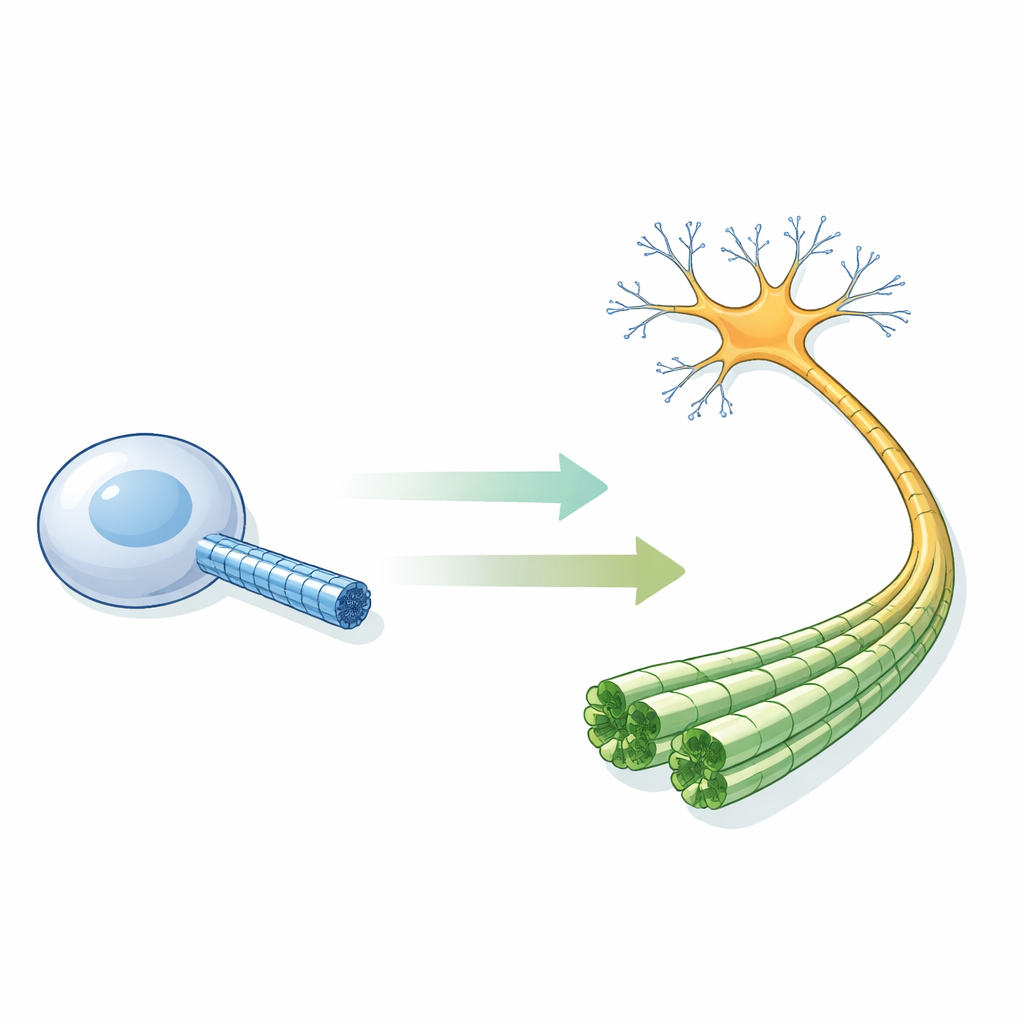
Bardzo drobne rurki, które podtrzymują neurony
Mikrotubule to puste cylindry zbudowane z powtarzalnych bloków białkowych i występują niemal we wszystkich komórkach. W neuronach mają szczególne znaczenie: uporządkowane w ciasne, równoległe wiązki nadają aksonom kształt i służą jako tory dla białek motorowych transportujących ładunki między ciałem komórkowym a odległymi synapsami. Doświadczenia w probówce sugerowały prostą regułę: gdy elementy składowe mają przyłączony nukleotyd GTP, ściana rurki przyjmuje „rozszerzony” kształt i jest stabilna; po rozłożeniu GTP do GDP ściana się kompaktuje, a rurka staje się krucha i podatna na rozpady. Jednak nikt wcześniej nie widział, w rozdzielczości atomowej, jak te mikrotubule wyglądają wewnątrz prawdziwego, ludzkiego neuronu.
Oglądanie aksonalnych autostrad atom po atomie
Autorzy hodowali ludzkie neurony z indukowanych komórek pluripotencjalnych i zachęcali je do tworzenia kulistych skupisk, z których wychodziły długie aksony rozciągające się po specjalnych rusztowaniach do mikroskopii elektronowej. Korzystając z najnowocześniejszej kriomikroskopii elektronowej i tomografii, zarejestrowali tysiące obrazów mikrotubul w nienaruszonych aksonach zamrożonych w stanie bliskim naturalnemu. Dzięki obliczeniowemu uśrednianiu wielu widoków uzyskali rekonstrukcję o rozdzielczości 2,7 ångströma — na tyle precyzyjną, by rozróżnić dwa pokrewne białka tubuliny, zlokalizować przyłączone nukleotydy, a nawet wyodrębnić uporządkowane cząsteczki wody i jony metali. Dzięki temu mogli określić nie tylko, jak daleko od siebie leżą bloki wzdłuż każdego protofilamentu, lecz także dokładny stan chemiczny tych bloków.
Stabilna sieć, która łamie zwykłe reguły
Struktura o wysokiej rozdzielczości przyniosła zaskoczenie. W aksonalnych mikrotubulach wymienialne miejsce w β‑tubulinie wyraźnie zawierało GDP, co wskazuje, że GTP zostało jak oczekiwano hydrolizowane. Jednak odstęp między parami tubulin wzdłuż rurki był rozszerzony, odpowiadając temu, co wcześniej obserwowano tylko w stabilnych, GTP‑podobnych sieciach tworzonych in vitro. Szczegółowe porównanie ze znanymi strukturami ujawniło stan hybrydowy: regiony białka, które wykrywają obecność γ‑fosforanu, zachowywały się jak klasyczne mikrotubule z GDP, podczas gdy elementy położone dalej — zwłaszcza ruchomy odcinek zwany pętlą T5 na styku sąsiednich dimerów — przyjęły rozszerzone, GTP‑podobne ułożenie. Łańcuch aromatycznych aminokwasów zdaje się przekazywać ruchy z tej pętli do sąsiednich kontaktów, blokując aksonalną sieć w rozciągniętej, stabilnej konfiguracji mimo jej chemii opartej na GDP.
Przełączanie stanów w miarę dojrzewania neuronów
Aby sprawdzić, czy ta nietypowa geometria jest cechą dojrzałych aksonów, zespół mierzył odstępy sieci w innych kontekstach, używając kriotomografii elektronowej i analizy widma mocy. W komórkach macierzystych niedifferencjonowanych mikrotubule wykazywały bardziej zwarte odstępy, bardzo podobne do mikrotubul z GDP zmontowanych w probówce. Dla porównania, mikrotubule w aksonach zróżnicowanych neuronów wykazywały rozszerzone odstępy, podobne do struktury atomowej aksonu i do in vitro sieci stabilizowanych przez niehydrolizowalne analogi GTP lub lek Taksol. Ta zmiana od zwartej do rozszerzonej geometrii wydaje się więc być częścią programu różnicowania neuronalnego, zbieżną z potrzebą stabilizacji długich wypustek aksonalnych i ich reorganizacji w gęste wiązki.
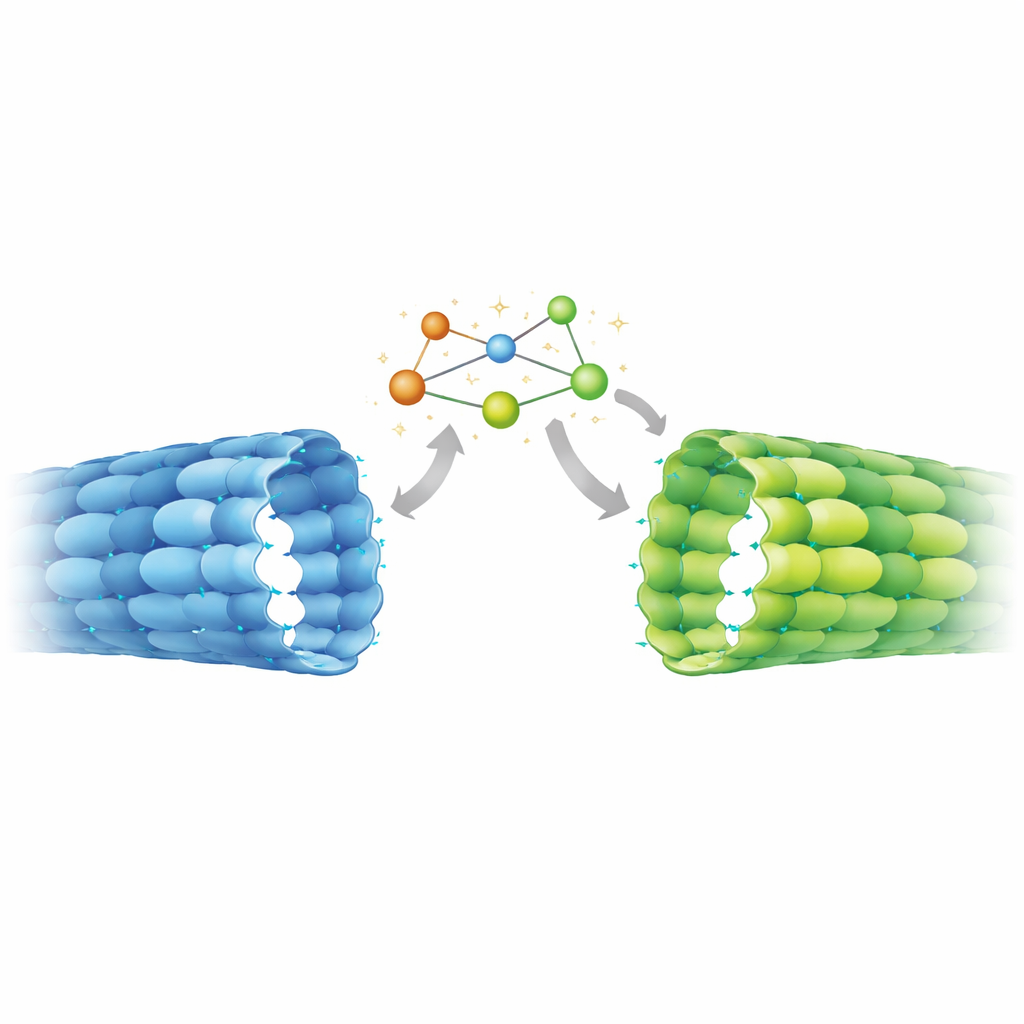
Implikacje dla funkcji mózgu i terapii
Praca ta pokazuje, że aksonalne mikrotubule są chemicznie w stanie związanym z GDP, a jednocześnie strukturalnie w formie rozszerzonej, podobnej do GTP, stabilizowane przez wewnętrzny przełącznik mechaniczny. Oznacza to, że motorowe białka, regulatory i enzymy ozdabiające mikrotubule w neuronach oddziałują z typem sieci, który nie jest wiernie odtwarzany przez wiele standardowych preparatów laboratoryjnych. Ponieważ te efektory same mogą sprzyjać odstępom rozszerzonym lub zwartym — i ponieważ niektóre modyfikacje chemiczne tubuliny preferują rozszerzone sieci — odkryty stan prawdopodobnie wchodzi w pętlę sprzężenia zwrotnego, która dostraja transport ładunków i trwałość mikrotubul podczas rozwoju mózgu. Wyniki sugerują też, że leki takie jak Taksol, znane z rozszerzania sieci, mogą sprzyjać wzrostowi aksonów częściowo przez przesuwanie mikrotubul w kierunku tej samej stabilnej konformacji, która naturalnie pojawia się w trakcie formowania połączeń neuronalnych.
Cytowanie: Zehr, E.A., Sun, S., Sarbanes, S.L. et al. Microtubules in the axon are GDP bound but adopt a stable GTP-like expanded state. Nat Struct Mol Biol 33, 631–640 (2026). https://doi.org/10.1038/s41594-026-01787-7
Słowa kluczowe: mikrotubule, akson, różnicowanie neuronów, kriotransmisyjna mikroskopia elektronowa, cytoszkielet