Clear Sky Science · sv
Rumslig kromatinanalys med METALoci avslöjar 3D-regulatoriska nav som bestämmer kön
Hur genomets form hjälper till att avgöra kön
Varje däggdjur börjar livet med små gonader som kan utvecklas till antingen testiklar eller äggstockar. Vi har länge känt till många av de gener som driver utvecklingen åt manligt eller kvinnligt håll, men mycket mindre om hur DNA:s tredimensionella vikning i kärnan bidrar till det valet. Den här studien visar att kromosomernas fysiska utformning skapar kraftfulla kontrollcenter — tredimensionella regulatoriska nav — som hjälper avgöra om det embryonala gonadet blir testikel eller äggstock, och avslöjar nya aktörer och dolda strömbrytare i det beslutet. 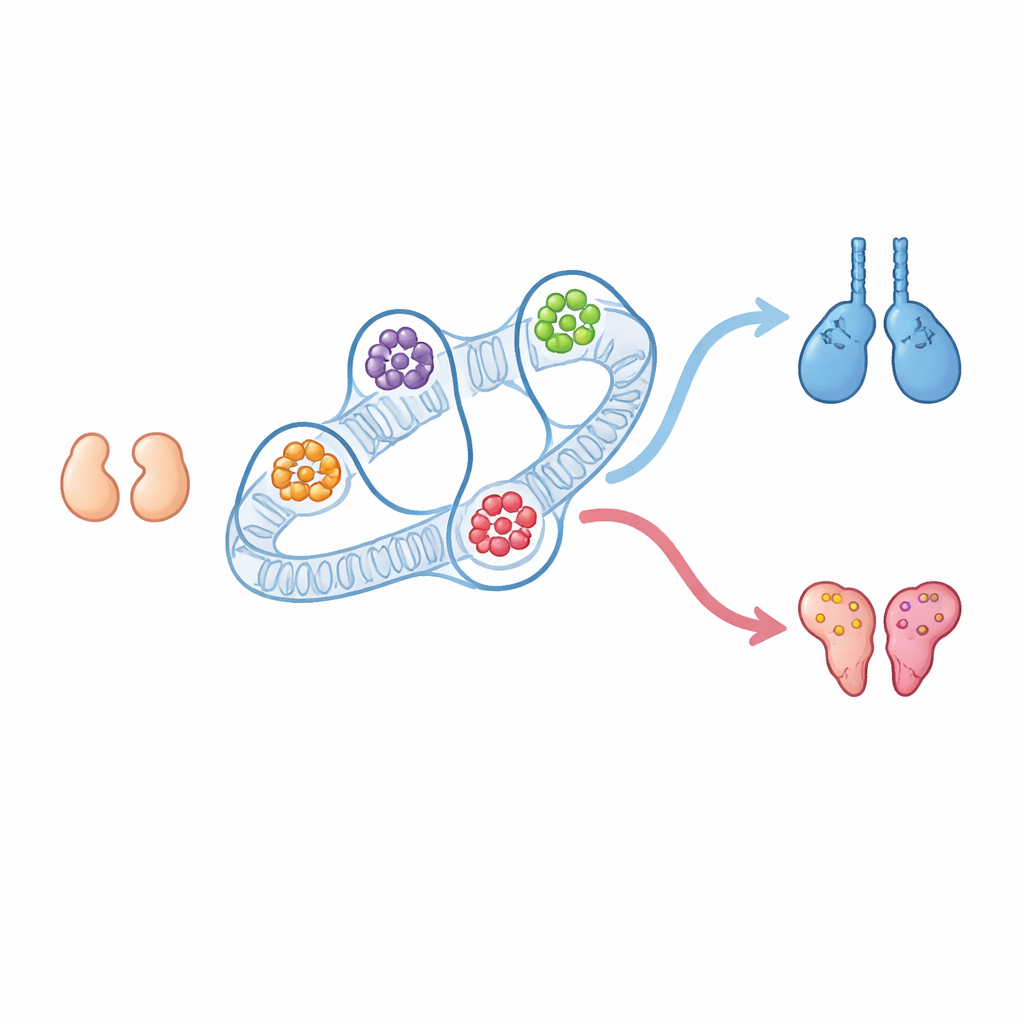
Det tidiga gonadet vid ett vägskäl
I tidiga musembryon ser och beter sig gonader hos XX- och XY-individer nästan likadant. De är "bipotentiella", vilket betyder att de fortfarande kan bli antingen äggstockar eller testiklar. Senare utlöser en aktivitetsutbrott från den Y-bundna Sry-genen i XY-embryon testikelvägen via genen Sox9 och signalsubstansen Fgf9, medan XX-embryon, som saknar Sry, aktiverar ovariala gener som Wnt4 och Foxl2. Författarna isolerade specifika stödjeceller från dessa tidiga gonader, både före och efter att könet bestämts, och kartlade hur deras DNA viks och vilka regioner som är aktiva. Överraskande nog förändrades de breda kromosomområdena som kontaktar varandra mest — kända som kompartment och domäner — knappt mellan den obestämda och den könsspecifika fasen, trots att genaktiviteten skiftar dramatiskt.
Upptäckt av dolda 3D-kontrollnav
Denna mismatch mellan stabil storskalig vikning och mycket dynamisk genaktivitet antydde att den viktiga aktiviteten kanske sker på finare skala. För att hitta detta utvecklade teamet METALoci, en beräkningsmetod som lånar verktyg från geografi, där de används för att upptäcka hetfläckar av till exempel föroreningar i en stad. I stället för kvarter behandlar METALoci små stycken av genomet som platser och använder Hi-C-kontaktdata för att placera dem i en virtuell karta beroende på hur ofta de rör vid varandra. Metoden lägger sedan över kemiska aktivitetsmarkörer, såsom H3K27ac, för att identifiera "heta" kluster där aktiva förstärkare och promotorer samlas i 3D-utrymme. Dessa kluster, eller metaloci, fungerar som regulatoriska nav där grupper av DNA-strömbrytare och deras målgen samarbetar.
Omskopning under könsbestämning
I hela genomet avslöjade METALoci att dessa 3D-nav omskopas i stor utsträckning när gonaderna åtar sig att bli äggstock eller testikel. Antalet starkt aktiva nav ungefär fördubblades under differentieringen, liksom antalet starkt inaktiva zoner, vilket speglar samtidig aktivering och avstängning av hela genprogram. Kända könsgener uppvisade förväntade beteenden: till exempel fick Sox9 ett starkt aktivt nav i framtida Sertoli- (testikel-) celler, medan Bmp2 fick en aktiv omgivning i framtida granulosa- (ovariala-) celler. Författarna följde hur varje gens lokala miljö rörde sig mellan inaktiva och aktiva tillstånd över tid och mellan könen, och visade att manliga specifika gener ofta upplever särskilt starka ökningar i regulatorisk aktivitet under testikelbildning. 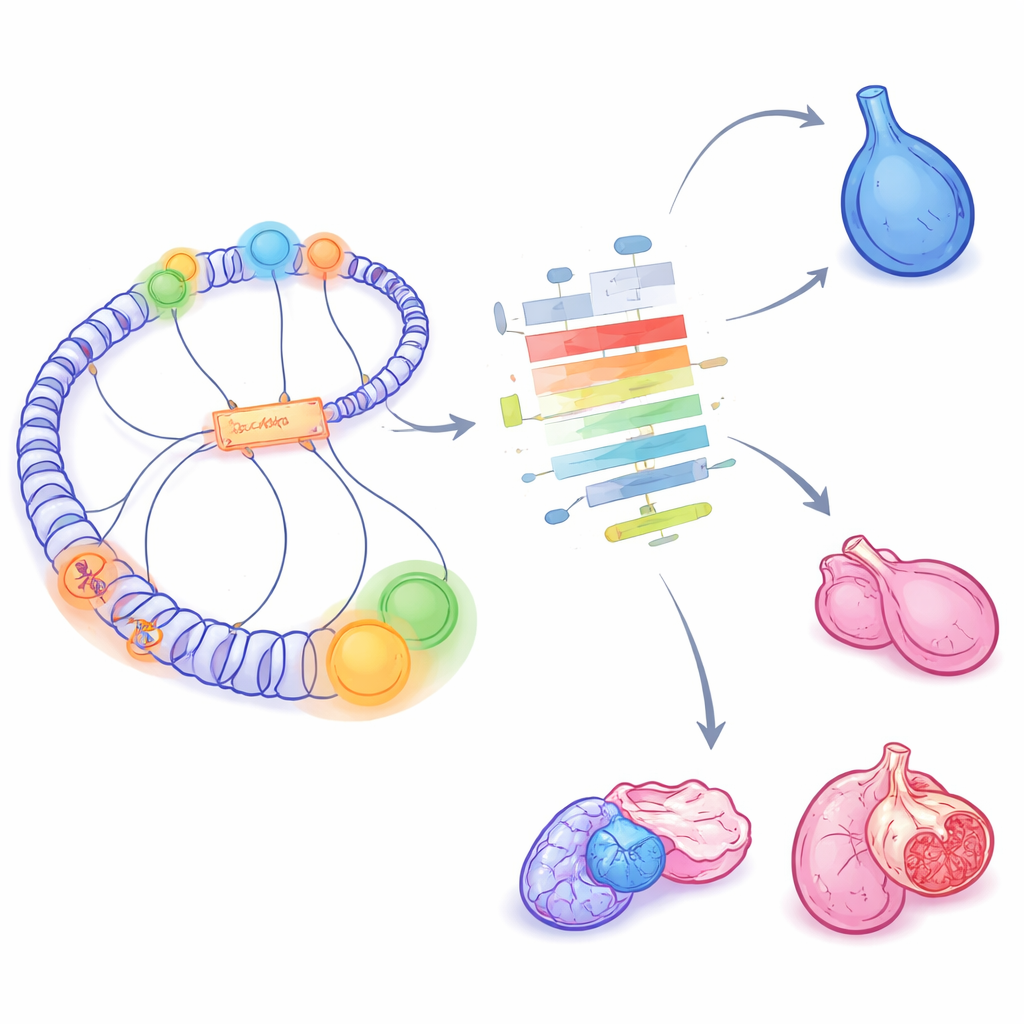
En icke-kodande strömbrytare för en nyckelgen för kön
Ett slående exempel kom från Fgf9, en gen som är avgörande för att främja testikelvägen och hämma den ovariala. Människor och möss med defekter i FGF9 kan genomgå manlig-till-kvinnlig könsreversering, men de element som styr dess aktivitet i gonaden var okända. Genom att använda METALoci simulerade forskarna borttagning av små DNA-bitar runt Fgf9 in silico och undersökte vilka bortfall som skulle rubba dess 3D-regulatoriska nav. Detta pekade ut ett brett, genfritt streck cirka en kvarts miljon baser nedströms. När teamet tog bort ett 306 kilobas stort stycke som täckte större delen av denna region i möss sjönk Fgf9-uttrycket i fostrets testiklar med ungefär hälften. XY-embryon utvecklade gonader som variera från blandade ovotestiklar till äggstocksliknande organ, vilket nära efterliknade kompletta Fgf9-utstängningar — men utan de dödliga lungdefekter som sådana utstängningar vanligtvis orsakar. Mindre deletioner visade att mycket av kontrollen är koncentrerad till en central 93 kilobas subregion, men att regulatorisk styrka är delad mellan flera förstärkare, vilket ger redundans.
Delade regulatorer för manlig och kvinnlig identitet
För att förstå hur dessa nav kopplar ihop sig till bredare genkretsar kombinerade författarna sina 3D-kartor med enkelcells-RNA-data och rekonstruerade regulatoriska nätverk. De fann kända könsbestämmande faktorer i nyckelpositioner, men lyfte också fram transkriptionsfaktorer som tidigare inte kopplats till könsbestämning. Bland dem fanns Meis1 och Meis2, som framträdde som starka "negativa regulatorer" av både manliga och kvinnliga differentieringsprogram. Funktionella tester i genetiskt modifierade möss visade att borttagning av Meis1 ensam, eller tre av de fyra Meis1/Meis2-genkopiorna, orsakar att fläckar av celler i XY-gonader antar äggstockslik identitet och, motsatt, att vissa XX-celler antar testikellik identitet. Detta indikerar att Meis-generna verkar redundanta som väktare av korrekt sexuell identitet i båda riktningarna.
Varför detta arbete är viktigt
För en icke-specialist är huvudbudskapet att könsbestämning inte bara styrs av vilka gener du har, utan också av hur ditt DNA är vikt i 3D och hur kluster av avlägsna regulatoriska element kommunicerar med sina målgener. METALoci avslöjar dessa dolda nav och visar att även när det övergripande genomskellet ser stabilt ut kan den interna kopplingen inom domäner dramatiskt omskopas för att skifta cellens öde. Genom att peka ut en kraftfull icke-kodande region som styr Fgf9 och genom att upptäcka nya faktorer som Meis-generna, erbjuder detta arbete nya ledtrådar för förståelsen av störningar i sexuell utveckling och visar hur 3D-genomkartläggning kan avslöja avgörande regulatoriska strömbrytare som traditionella genfokuserade metoder missar.
Citering: Mota-Gómez, I., Rodríguez, J.A., Dupont, S. et al. Chromatin spatial analysis by METALoci unveils sex-determining 3D regulatory hubs. Nat Struct Mol Biol 33, 577–589 (2026). https://doi.org/10.1038/s41594-026-01749-z
Nyckelord: könsbestämning, 3D-genom, kromatinarkitektur, genreglering, icke-kodande DNA