Clear Sky Science · it
Analisi spaziale della cromatina con METALoci svela hub regolatori 3D che determinano il sesso
Come la forma del genoma aiuta a decidere il sesso
Ogni mammifero inizia la vita con piccoli gonadi che possono diventare sia testicoli sia ovaie. Conosciamo da tempo molti dei geni che spingono lo sviluppo verso il percorso maschile o femminile, ma molto meno su come il ripiegamento tridimensionale del DNA all’interno del nucleo contribuisca a orientare quella scelta. Questo studio mostra che la disposizione fisica dei cromosomi crea potenti centri di controllo—hub regolatori tridimensionali—che aiutano a determinare se il gonade embrionale diventerà testicolo o ovaio, e rivela nuovi attori e interruttori nascosti coinvolti in quella decisione. 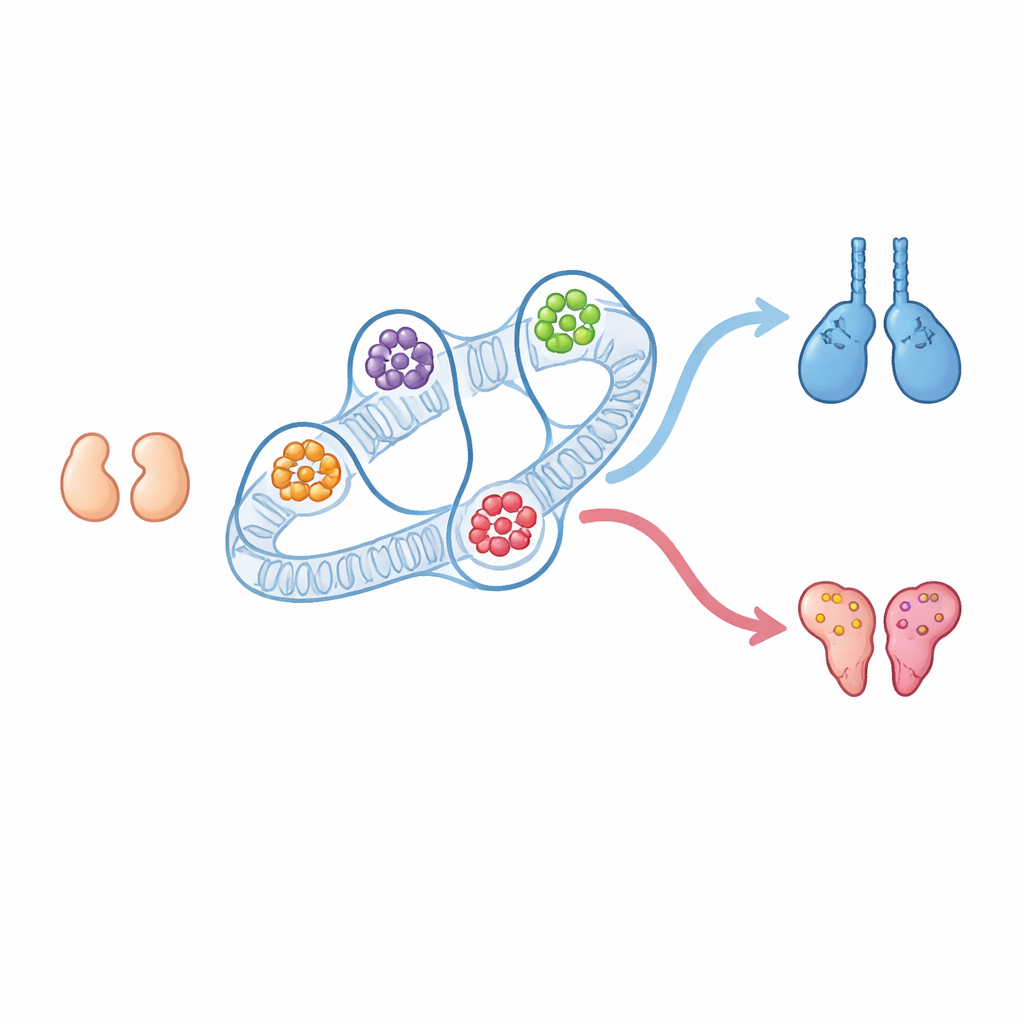
Il gonade precoce a un bivio
Nei primi embrioni di topo, i gonadi negli individui XX e XY appaiono e si comportano quasi allo stesso modo. Sono “bipotenziali”, cioè possono ancora diventare ovaie o testicoli. Più tardi, un’ondata di attività del gene Sry legato al cromosoma Y negli embrioni XY avvia il percorso verso il testicolo tramite il gene Sox9 e la molecola di segnalazione Fgf9, mentre negli embrioni XX, che non possiedono Sry, si attivano geni ovarici come Wnt4 e Foxl2. Gli autori hanno isolato cellule di supporto specifiche da questi gonadi precoci, sia prima sia dopo la decisione sessuale, e hanno mappato come il loro DNA si piega e quali regioni sono attive. Sorprendentemente, i grandi quartieri cromosomici che si contattano più frequentemente—conosciuti come compartimenti e domini—sono cambiati pochissimo tra le fasi indeterminate e quelle specifiche per sesso, nonostante le forti variazioni nell’attività genica.
Scoprire hub di controllo 3D nascosti
Questa discrepanza tra un ripiegamento su larga scala stabile e un’attività genica altamente dinamica suggeriva che l’azione importante potesse avvenire a scale più fini. Per scoprirla, il gruppo ha sviluppato METALoci, un metodo computazionale che prende in prestito strumenti dalla geografia, dove vengono usati per individuare hot‑spot, ad esempio di inquinamento in città. Invece dei blocchi cittadini, METALoci tratta piccoli segmenti del genoma come posizioni e usa dati di contatto Hi‑C per collocarli in una mappa virtuale in base a quanto spesso si toccano. Sovrappone poi marcatori chimici di attività, come H3K27ac, per identificare ammassi “caldi” dove potenziatori e promotori attivi si raggruppano nello spazio 3D. Questi ammassi, o metaloci, agiscono come hub regolatori in cui gruppi di interruttori del DNA e i loro geni bersaglio funzionano insieme.
Riconfigurazioni durante la determinazione del sesso
In tutto il genoma, METALoci ha rivelato che questi hub 3D vengono ampiamente riconfigurati quando i gonadi si impegnano verso ovaio o testicolo. Il numero di hub fortemente attivi è circa raddoppiato durante la differenziazione, così come il numero di zone fortemente inattive, riflettendo l’accensione e lo spegnimento simultanei di interi programmi genici. I geni noti per determinare il sesso si sono comportati in modo coerente: per esempio, Sox9 ha guadagnato un hub attivo potente nelle future cellule di Sertoli (testicolo), mentre Bmp2 ha acquisito un ambiente attivo nelle future cellule della granulosa (ovaio). Gli autori hanno seguito come l’ambiente locale di ciascun gene si spostava tra stati inattivi e attivi nel tempo e tra i sessi, mostrando che i geni specifici maschili normalmente subiscono guadagni particolarmente forti di attività regolatoria durante la formazione del testicolo. 
Un interruttore non codificante per un gene chiave del sesso
Un esempio notevole è emerso da Fgf9, un gene essenziale per promuovere il percorso testicolare e bloccare quello ovarico. Persone e topi con difetti in FGF9 possono subire inversioni sessuali da maschio a femmina, eppure gli elementi che controllano la sua attività nel gonade erano sconosciuti. Usando METALoci, i ricercatori hanno simulato in silico la cancellazione di piccoli frammenti di DNA attorno a Fgf9 e hanno chiesto quali perdite avrebbero compromesso il suo hub regolatorio 3D. Questo ha indicato un’ampia regione priva di geni di circa un quarto di milione di basi a valle. Quando il gruppo ha rimosso nei topi un blocco di 306 kilobasi che abbracciava la maggior parte di questa regione, l’espressione di Fgf9 nei testicoli fetali è scesa di circa la metà. Gli embrioni XY hanno sviluppato gonadi che andavano da ovotestìs misti a organi simili ad ovaio, rispecchiando da vicino i knockout completi di Fgf9—ma senza i letali difetti polmonari che quei knockout solitamente causano. Delezioni più piccole hanno mostrato che gran parte del controllo è concentrata in una sotto‑regione centrale di 93 kilobasi, sebbene il potere regolatorio sia condiviso tra diversi potenziatori, fornendo ridondanza.
Regolatori condivisi dell’identità maschile e femminile
Per capire come questi hub si connettano in circuiti genici più ampi, gli autori hanno combinato le loro mappe 3D con dati di RNA a singola cellula e hanno ricostruito reti regolatorie. Hanno trovato fattori noti della determinazione sessuale in posizioni chiave, ma hanno anche evidenziato fattori di trascrizione non precedentemente collegati a questo processo. Tra questi figurano Meis1 e Meis2, emersi come forti “regolatori negativi” sia dei programmi di differenziazione maschile sia femminile. Test funzionali in topi geneticamente modificati hanno mostrato che la rimozione di Meis1 da sola, o di tre delle quattro copie geniche Meis1/Meis2, provoca che chiazze di cellule nei gonadi XY assumano identità di tipo ovarico e, viceversa, che alcune cellule XX assumano identità simili al testicolo. Ciò indica che i geni Meis agiscono in modo ridondante come guardiani della corretta identità sessuale in entrambe le direzioni.
Perché questo lavoro è importante
Per un non specialista, il messaggio chiave è che la determinazione del sesso non è controllata solo da quali geni possiedi, ma anche da come il tuo DNA è ripiegato in 3D e da come ammassi di elementi regolatori distanti comunicano con i loro geni bersaglio. METALoci rivela questi hub nascosti e mostra che, anche quando l’impalcatura complessiva del genoma sembra stabile, l’impianto interno all’interno dei domini può essere drasticamente riorganizzato per spostare il destino cellulare. Identificando una potente regione non codificante che governa Fgf9 e scoprendo nuovi fattori come i geni Meis, questo lavoro offre piste nuove per comprendere i disordini dello sviluppo sessuale e dimostra come la mappatura del genoma 3D possa rivelare interruttori regolatori cruciali che gli approcci tradizionali focalizzati sui geni potrebbero perdere.
Citazione: Mota-Gómez, I., Rodríguez, J.A., Dupont, S. et al. Chromatin spatial analysis by METALoci unveils sex-determining 3D regulatory hubs. Nat Struct Mol Biol 33, 577–589 (2026). https://doi.org/10.1038/s41594-026-01749-z
Parole chiave: determinazione del sesso, genoma 3D, architettura della cromatina, regolazione genica, DNA non codificante