Clear Sky Science · ja
METALociによるクロマチン空間解析が明らかにする性決定の3D制御ハブ
ゲノムの立体構造が性を決める仕組み
すべての哺乳類は、精巣にも卵巣にもなり得る小さな生殖器(生殖腺)として発生を始めます。発生を雄または雌へと導く多くの遺伝子は長く知られてきましたが、核内でのDNAの三次元折りたたみがその選択をどう補助するかについてははるかに不明な点が多く残っています。本研究は、染色体の物理的配置が強力な制御センター、つまり三次元の制御ハブを形成し、胚性生殖腺が精巣になるか卵巣になるかを決めるのを助けていることを示し、その決定に関与する新たな因子や隠れたスイッチを明らかにします。 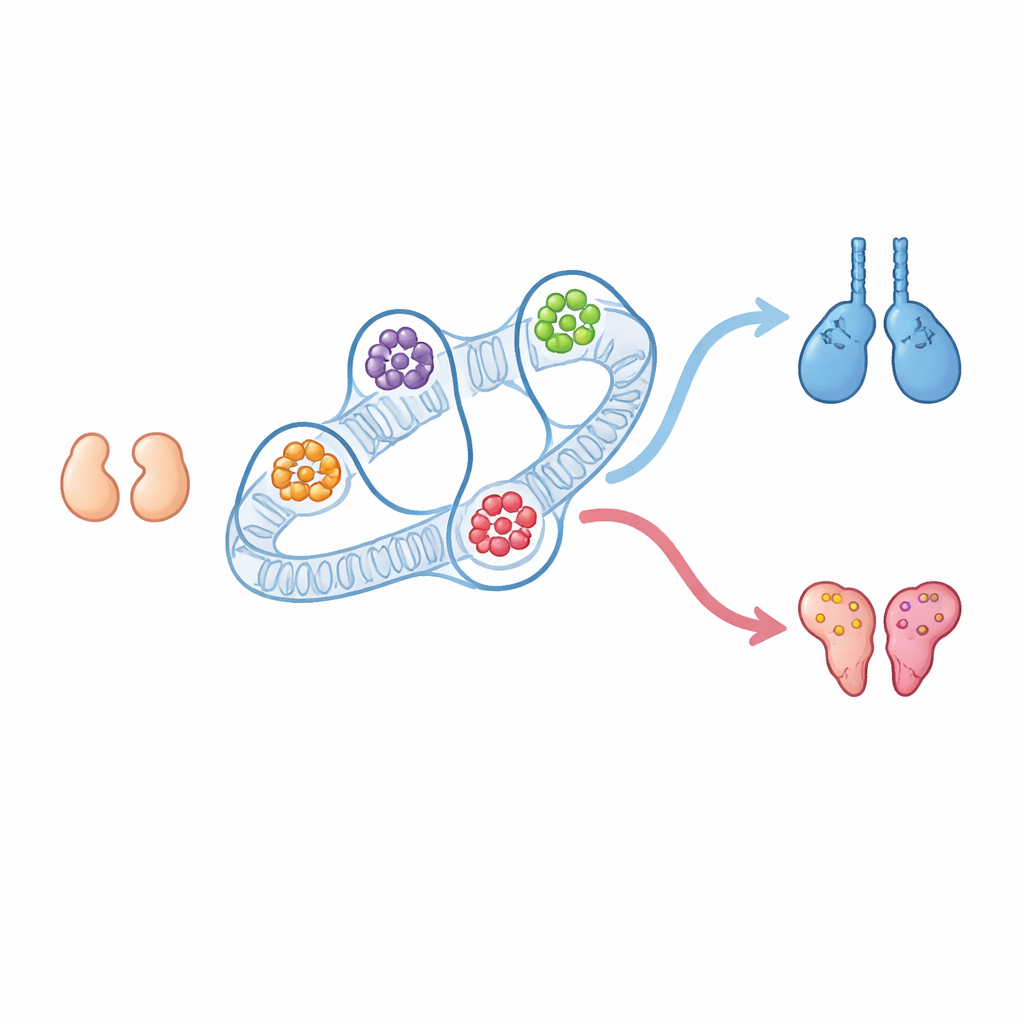
岐路に立つ初期生殖腺
マウス胚の初期段階では、XXとXYの個体の生殖腺は見た目も挙動もほとんど同じです。これらは“二方向性(bipotential)”で、まだ精巣にも卵巣にもなり得ます。後に、Y染色体上のSry遺伝子の一時的な活性化がXY胚での精巣経路を誘導し、Sox9やシグナル分子Fgf9を介して進行します。一方、Sryを持たないXX胚ではWnt4やFoxl2といった卵巣遺伝子が活性化されます。著者らは、性が決まる前後のこれら初期生殖腺から支持細胞を分離し、DNAの折りたたみ方と活性化されている領域をマップしました。驚くべきことに、相互接触の頻度が高い広域の染色体近隣(コンパートメントやドメインとして知られる)は、遺伝子発現が劇的に変化しているにもかかわらず、未決定段階と性特異的段階の間でほとんど変化しませんでした。
隠れた3D制御ハブの発見
大規模な折りたたみの安定性と遺伝子活性の高度な動態との不一致は、重要な変化がより細かいスケールで起きていることを示唆しました。これを解明するため、研究チームはMETALociという計算手法を開発しました。これは、都市内の汚染ホットスポットなどを検出する地理学の手法を応用したものです。METALociは市街区の代わりにゲノムの小領域を“位置”として扱い、Hi-C接触データを用いて、それらがどれだけ頻繁に接触するかに基づいて仮想マップ上に配置します。次にH3K27acなどの化学的活性マーカーを重ね合わせて、活性エンハンサーやプロモーターが3D空間に集まる“ホット”なクラスターを同定します。これらのクラスター、すなわちmetalociは、DNAスイッチ群と標的遺伝子が共同で働く制御ハブとして機能します。
性決定時の配線の書き換え
METALociはゲノム全体にわたって、これらの3Dハブが生殖腺が卵巣または精巣に分化する際に大規模に再配線されることを明らかにしました。分化の過程で強く活性なハブの数はほぼ倍増し、同時に強く不活性な領域の数も増え、遺伝子プログラム全体のオンとオフが同時並行で進む様子が反映されました。既知の性決定遺伝子は直感的な振る舞いを示しました。例えばSox9は将来のセルトリ細胞(精巣)で強い活性ハブを獲得し、Bmp2は将来の顆粒膜細胞(卵巣)で活性な環境を得ました。著者らは各遺伝子の局所環境が時間や性の違いで不活性から活性へどのように移動するかを追跡し、雄特異的な遺伝子は通常、精巣形成時に特に強い制御活性の獲得を経験することを示しました。 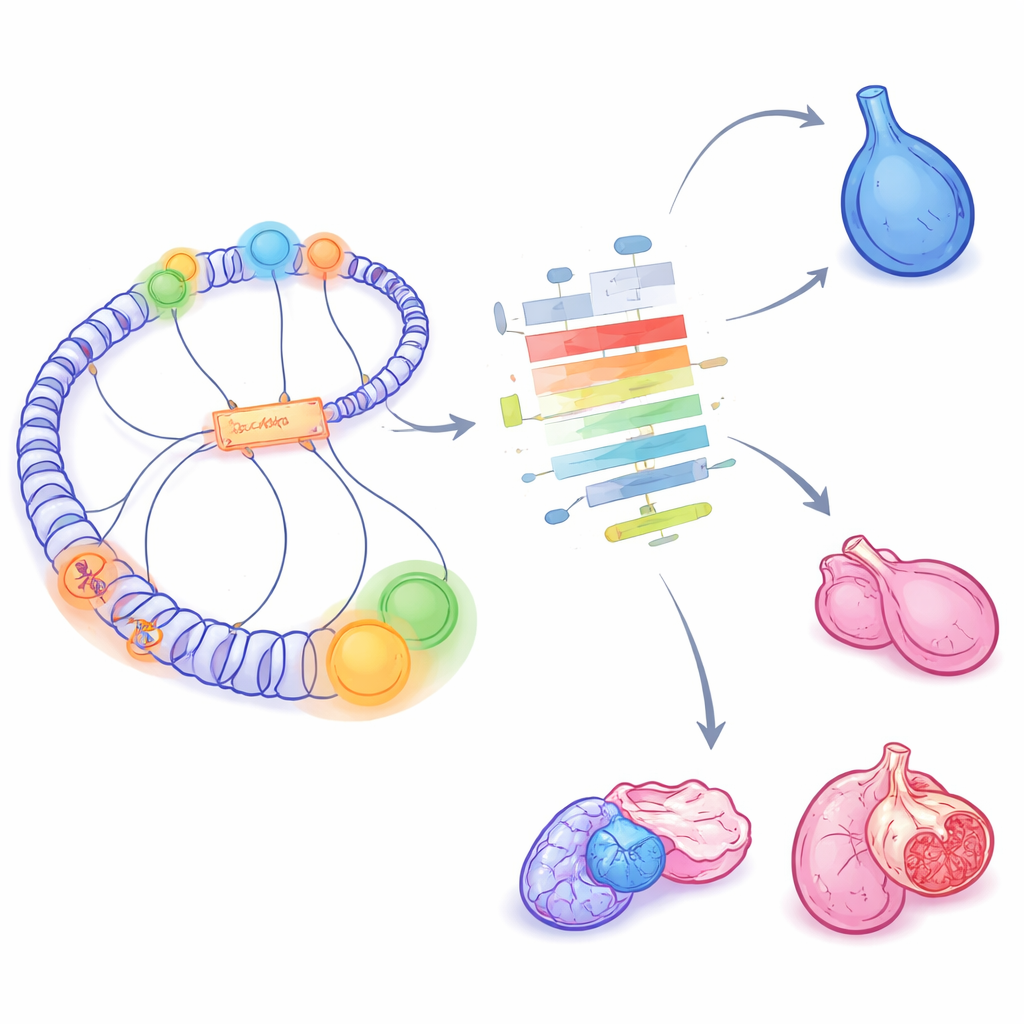
主要な性遺伝子のための非コードスイッチ
注目に値する例の一つがFgf9です。Fgf9は精巣経路を促進し卵巣経路を阻害する上で必須の遺伝子であり、FGF9に欠損のある人やマウスは雄から雌への性逆転を起こすことがありますが、生殖腺内でその活性を制御する要素は不明でした。METALociを用いて、研究者たちはFgf9周辺の小領域を計算上で“削除”し、どの欠失がその3D制御ハブを破壊するかを調べました。その結果、下流約25万塩基にわたる遺伝子を含まない広い領域が候補として浮上しました。この領域の大部分を含む306キロベースの塊をマウスで削除すると、胎児精巣におけるFgf9の発現は約半分に低下しました。XY胚は混合的な卵精巣(ovotestis)から卵巣様の器官まで多様な形の生殖腺を発達させ、完全なFgf9ノックアウトに近い表現型を示しましたが、通常そのノックアウトで伴う致死的な肺欠損はありませんでした。より小さな欠失では、制御は中央の93キロベースの部分に集中していることが示されましたが、複数のエンハンサーに制御能力が分散しており冗長性があることも分かりました。
雄性・雌性の同時制御因子
これらのハブが広い遺伝子回路にどのように組み込まれているかを理解するため、著者らは3Dマップを単一細胞RNAデータと組み合わせて制御ネットワークを再構築しました。既知の性決定因子が要所に見られた一方で、これまで性決定と関連づけられてこなかった転写因子も浮かび上がりました。その中にはMeis1とMeis2があり、これらは雄・雌双方の分化プログラムの強い“負の制御因子”として出現しました。遺伝子改変マウスでの機能試験により、Meis1を単独で欠失させる、もしくはMeis1/Meis2の四コピー中三コピーを欠失させると、XY生殖腺の一部細胞が卵巣様の同一性を獲得し、逆にXXの一部細胞が精巣様の同一性を示すことが確認されました。これはMeis遺伝子が冗長的に作用し、両側への適切な性同一性を守る番人として働くことを示しています。
この研究が重要な理由
専門外の読者に向けた主なメッセージは、性決定は保有する遺伝子の種類だけで制御されるのではなく、DNAの三次元折りたたみや遠隔の制御要素のクラスターが標的遺伝子とどのようにやり取りするかにも依存している、ということです。METALociはこれらの隠れたハブを明らかにし、全体的なゲノム骨格が安定して見えても、ドメイン内の内部配線が大きく書き換えられて細胞運命を変えることを示します。Fgf9を支配する強力な非コード領域を特定し、Meis遺伝子のような新しい因子を明らかにすることで、この研究は性分化疾患を理解するための新たな手がかりを提供するとともに、従来の遺伝子中心のアプローチでは見落とされがちな重要な制御スイッチを3Dゲノムマッピングが明らかにできることを示しています。
引用: Mota-Gómez, I., Rodríguez, J.A., Dupont, S. et al. Chromatin spatial analysis by METALoci unveils sex-determining 3D regulatory hubs. Nat Struct Mol Biol 33, 577–589 (2026). https://doi.org/10.1038/s41594-026-01749-z
キーワード: 性決定, 3Dゲノム, クロマチン構造, 遺伝子制御, 非コードDNA