Clear Sky Science · de
Räumliche Chromatinanalyse mit METALoci enthüllt geschlechtsbestimmende 3D-Regulierungshubs
Wie die Form des Genoms bei der Geschlechtsentscheidung hilft
Jedes Säugetier beginnt sein Leben mit winzigen Gonaden, die sich entweder zu Hoden oder Eierstöcken entwickeln können. Viele der Gene, die die Entwicklung in Richtung Männchen oder Weibchen treiben, sind seit langem bekannt, doch deutlich weniger versteht man darüber, wie die dreidimensionale Faltung der DNA im Zellkern diese Entscheidung lenkt. Diese Studie zeigt, dass die physische Anordnung unserer Chromosomen mächtige Steuerzentren – dreidimensionale Regulationshubs – erzeugt, die mitbestimmen, ob sich die embryonale Gonade zu Hoden oder Eierstock entwickelt, und offenbart neue Akteure sowie versteckte Schalter, die an dieser Entscheidung beteiligt sind. 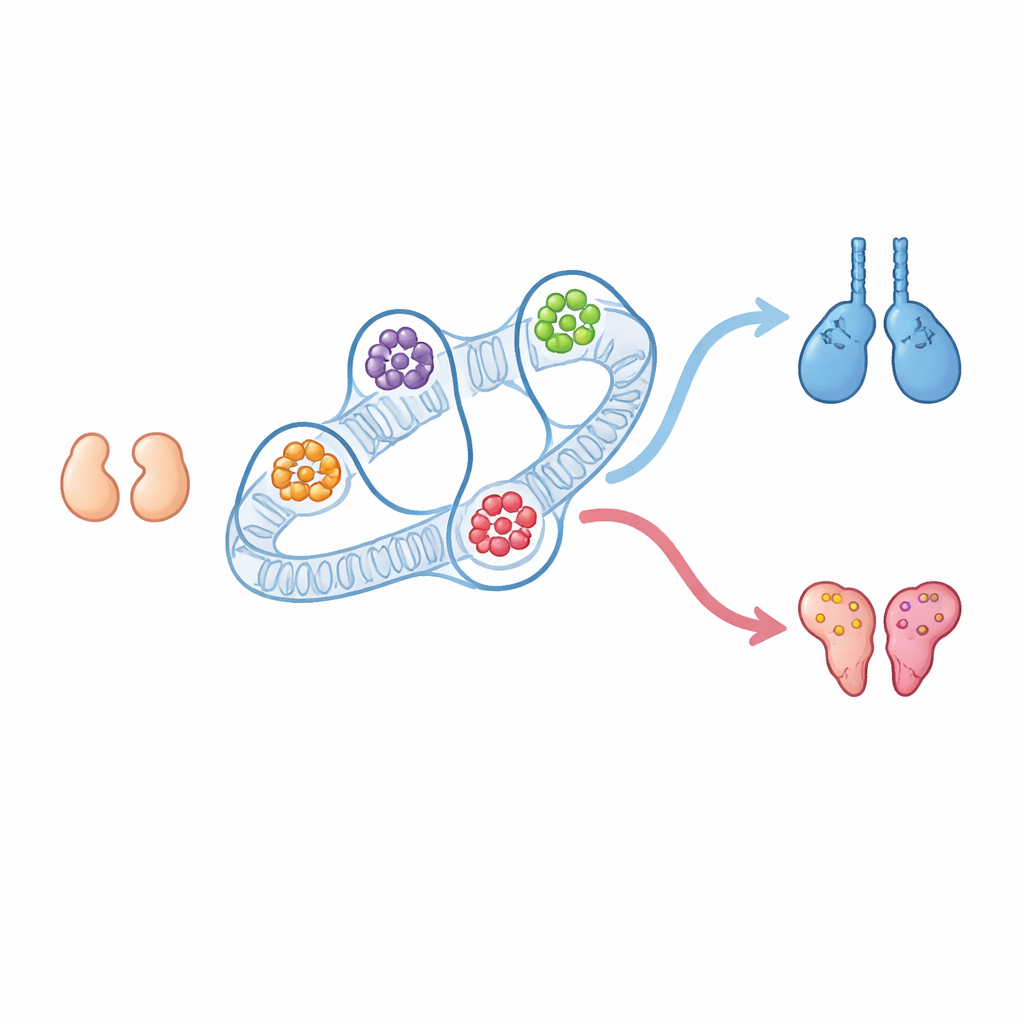
Die frühe Gonade an einem Scheideweg
In frühen Mausembryonen sehen und verhalten sich die Gonaden von XX- und XY-Individuen fast gleich. Sie sind „bipotent“, das heißt, sie können noch entweder zu Eierstöcken oder zu Hoden werden. Später löst ein Aktivitätsschub des Y‑gebundenen Sry-Gens in XY-Embryonen den Hodenweg über das Gen Sox9 und das Signalmolekül Fgf9 aus, während XX-Embryonen, denen Sry fehlt, ovarielle Gene wie Wnt4 und Foxl2 hochfahren. Die Autoren isolierten spezifische Stützzellen aus diesen frühen Gonaden, sowohl vor als auch nach der Geschlechtsentscheidung, und kartierten, wie sich deren DNA faltet und welche Regionen aktiv sind. Überraschenderweise änderten sich die großräumigen Chromosomennachbarschaften, die sich am häufigsten berühren – bekannt als Kompartmente und Domains – kaum zwischen der unbestimmten und der geschlechtsspezifischen Phase, obwohl die Genaktivität sich dramatisch veränderte.
Entdeckung versteckter 3D-Regulierungshubs
Diese Diskrepanz zwischen stabiler großskaliger Faltung und hochdynamischer Genaktivität deutete darauf hin, dass die entscheidende Aktion auf feineren Skalen stattfindet. Um das aufzudecken, entwickelte das Team METALoci, eine rechnerische Methode, die Werkzeuge aus der Geographie übernimmt, wo sie verwendet werden, um Hotspots etwa für Verschmutzung in einer Stadt zu finden. Statt Stadtblöcken behandelt METALoci kleine Stücke des Genoms als Orte und verwendet Hi‑C-Kontaktdaten, um sie auf einer virtuellen Karte entsprechend ihrer Berührungsfrequenz zu platzieren. Anschließend legt es chemische Aktivitätsmarker wie H3K27ac darüber, um „heiße“ Cluster zu identifizieren, in denen aktive Enhancer und Promotoren sich im 3D-Raum versammeln. Diese Cluster, oder Metaloci, fungieren als Regulationshubs, in denen Gruppen von DNA‑Schaltern und ihre Zielgene zusammenwirken.
Umverdrahtung während der Geschlechtsbestimmung
Im gesamten Genom zeigte METALoci, dass diese 3D-Hubs beim Festlegen von Eierstock‑ oder Hodenzellschicksalen umfangreich umverdrahtet werden. Die Anzahl stark aktiver Hubs verdoppelte sich ungefähr während der Differenzierung, ebenso wie die Anzahl stark inaktiver Zonen, was das gleichzeitige An‑ und Abschalten ganzer Genprogramme widerspiegelt. Bekannte Geschlechtsgene verhielten sich erwartungsgemäß: Beispielsweise gewann Sox9 in zukünftigen Sertoli- (Hoden-)Zellen einen starken aktiven Hub, während Bmp2 in zukünftigen Granulosa- (Ovarial-)Zellen ein aktives Umfeld erwarb. Die Autoren verfolgten, wie sich die lokale Umgebung jedes Gens im Lauf der Zeit und zwischen den Geschlechtern von inaktiv zu aktiv bewegte und zeigten, dass männlich-spezifische Gene typischerweise besonders starke Zuwächse an regulatorischer Aktivität während der Hodenbildung erfahren. 
Ein nichtkodierender Schalter für ein Schlüsselgeschlechtsgen
Ein eindrückliches Beispiel betraf Fgf9, ein Gen, das wesentlich ist, um den Hodenweg zu fördern und den Ovarialweg zu blockieren. Menschen und Mäuse mit Defekten in FGF9 können eine männlich‑zu‑weiblich‑Geschlechtsumkehr durchlaufen, doch die Elemente, die seine Aktivität in der Gonade steuern, waren unbekannt. Mithilfe von METALoci simulierten die Forschenden in silico das Löschen kleiner DNA‑Abschnitte rund um Fgf9 und fragten, welche Verluste sein 3D‑Regulierungs‑Hub stören würden. Das zielte auf einen breiten, genfreien Abschnitt etwa ein Viertel Million Basen stromabwärts. Als das Team in Mäusen ein 306 Kilobasen großes Stück entfernte, das den Großteil dieser Region umfasste, sank die Fgf9‑Expression in fetalen Hoden um etwa die Hälfte. XY‑Embryonen entwickelten Gonaden, die von gemischten Ovotestes bis zu ovarähnlichen Organen reichten und damit vollständig den Fgf9‑Knockouts ähnelten — jedoch ohne die tödlichen Lungenfehler, die diese Knockouts sonst hervorrufen. Kleinere Deletionen zeigten, dass ein großer Teil der Kontrolle in einer zentralen 93 Kilobasen großen Subregion konzentriert ist, wobei die regulatorische Kraft jedoch auf mehrere Enhancer verteilt ist und so Redundanz bietet.
Geteilte Regulatoren männlicher und weiblicher Identität
Um zu verstehen, wie diese Hubs in größere Gennetzwerke eingebunden sind, kombinierten die Autoren ihre 3D‑Karten mit Einzelzell‑RNA‑Daten und rekonstruierten regulatorische Netzwerke. Sie fanden bekannte geschlechtsbestimmende Faktoren an Schlüsselpositionen, hoben aber auch Transkriptionsfaktoren hervor, die zuvor nicht mit der Geschlechtsbestimmung in Verbindung gebracht worden waren. Dazu gehörten Meis1 und Meis2, die als starke „negative Regulatoren“ sowohl der männlichen als auch der weiblichen Differenzierungsprogramme hervorgingen. Funktionelle Tests in genetisch veränderten Mäusen zeigten, dass das Entfernen von Meis1 allein oder von drei der vier Meis1/Meis2‑Genkopien dazu führt, dass Bereiche von Zellen in XY‑Gonaden eine ovarielle Identität annehmen und umgekehrt einige XX‑Zellen eine hodentypische Identität annehmen. Das deutet darauf hin, dass Meis‑Gene redundant als Wächter korrekter sexueller Identität in beide Richtungen wirken.
Warum diese Arbeit wichtig ist
Für nicht‑Spezialisten lautet die Kernbotschaft, dass die Geschlechtsbestimmung nicht nur davon abhängt, welche Gene vorhanden sind, sondern auch davon, wie die DNA dreidimensional gefaltet ist und wie Cluster entfernter regulatorischer Elemente mit ihren Zielgenen kommunizieren. METALoci macht diese versteckten Hubs sichtbar und zeigt, dass selbst wenn das Gesamtgerüst des Genoms stabil erscheint, die interne Verkabelung innerhalb von Domains dramatisch umverdrahtet werden kann, um das Zellschicksal zu verschieben. Indem ein mächtiges nichtkodierendes Gebiet identifiziert wurde, das Fgf9 steuert, und neue Faktoren wie die Meis‑Gene entdeckt wurden, liefert diese Arbeit neue Ansätze zum Verständnis von Störungen der Geschlechtsentwicklung und demonstriert, wie 3D‑Genomkartierung entscheidende regulatorische Schalter offenlegen kann, die traditionelle, genzentrierte Methoden übersehen.
Zitation: Mota-Gómez, I., Rodríguez, J.A., Dupont, S. et al. Chromatin spatial analysis by METALoci unveils sex-determining 3D regulatory hubs. Nat Struct Mol Biol 33, 577–589 (2026). https://doi.org/10.1038/s41594-026-01749-z
Schlüsselwörter: Geschlechtsbestimmung, 3D-Genom, Chromatinarchitektur, Genregulation, nichtkodierende DNA