Clear Sky Science · es
Análisis espacial de la cromatina mediante METALoci revela centros reguladores 3D que determinan el sexo
Cómo la forma del genoma ayuda a decidir el sexo
Cada mamífero comienza la vida con gonadas diminutas que pueden convertirse en testículos u ovarios. Durante mucho tiempo hemos conocido muchos de los genes que empujan el desarrollo hacia masculino o femenino, pero mucho menos sobre cómo el plegamiento tridimensional del ADN en el núcleo contribuye a guiar esa elección. Este estudio muestra que la disposición física de nuestros cromosomas crea centros de control potentes—hubs regulatorios tridimensionales—que ayudan a decidir si la gónada embrionaria se convierte en testículo u ovario, y revela nuevos actores y conmutadores ocultos implicados en esa decisión. 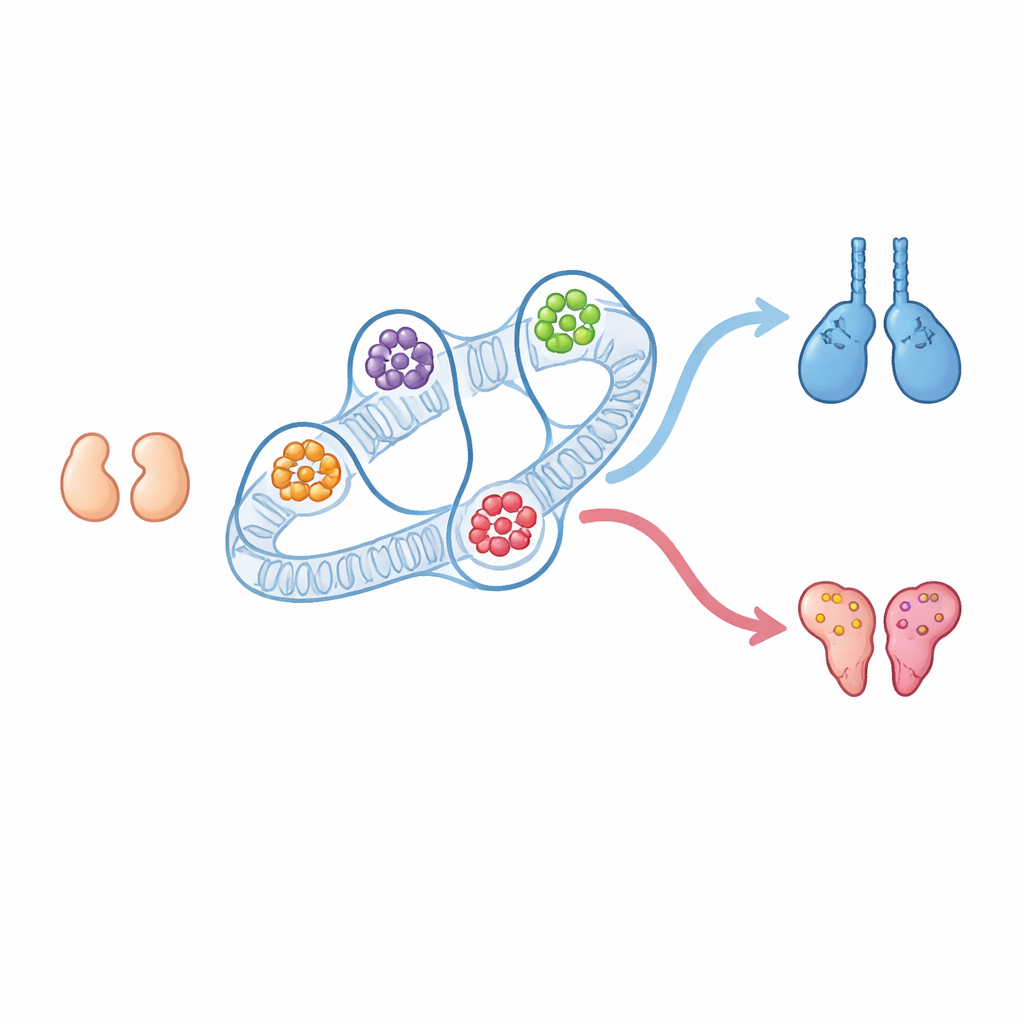
La gónada temprana en una encrucijada
En embriones de ratón tempranos, las gónadas en individuos XX y XY se parecen y se comportan casi igual. Son “bipotenciales”, lo que significa que aún pueden convertirse en ovarios o en testículos. Más tarde, un estallido de actividad del gen Sry ligado al cromosoma Y en embriones XY desencadena la vía testicular a través del gen Sox9 y la molécula de señalización Fgf9, mientras que en embriones XX, que carecen de Sry, se activan genes ováricos como Wnt4 y Foxl2. Los autores aislaron células de soporte específicas de estas gónadas tempranas, tanto antes como después de que se decidiera el sexo, y cartografiaron cómo se pliega su ADN y qué regiones están activas. Sorprendentemente, los vecindarios cromosómicos amplios que más se contactan entre sí—conocidos como compartimentos y dominios—apenas cambiaron entre las etapas indiferenciadas y las específicas por sexo, aunque la actividad génica cambiara de forma dramática.
Descubriendo hubs regulatorios 3D ocultos
Este desajuste entre un plegamiento estable a gran escala y una actividad génica muy dinámica sugería que la acción importante podría ocurrir a escalas más finas. Para descubrirla, el equipo desarrolló METALoci, un método computacional que toma prestadas herramientas de la geografía, donde se usan para detectar puntos calientes de, por ejemplo, contaminación en una ciudad. En lugar de manzanas urbanas, METALoci trata pequeños fragmentos del genoma como ubicaciones y utiliza datos de contactos Hi-C para colocarlos en un mapa virtual según la frecuencia con que contactan. Luego superpone marcadores químicos de actividad, como H3K27ac, para identificar conglomerados “calientes” donde enhancers y promotores activos se reúnen en el espacio 3D. Estos conglomerados, o metaloci, actúan como hubs regulatorios en los que grupos de interruptores de ADN y sus genes diana funcionan conjuntamente.
Reconfiguración durante la determinación sexual
A lo largo del genoma, METALoci reveló que estos hubs 3D se reconfiguran ampliamente a medida que las gónadas se comprometen con ovario o testículo. El número de hubs fuertemente activos aproximadamente se duplicó durante la diferenciación, al igual que el número de zonas fuertemente inactivas, reflejando la activación y el apagado simultáneos de programas génicos enteros. Los genes sexuales conocidos se comportaron de forma intuitiva: por ejemplo, Sox9 ganó un hub activo fuerte en las futuras células de Sertoli (testículo), mientras que Bmp2 adquirió un entorno activo en las futuras células de la granulosa (ovario). Los autores siguieron cómo el entorno local de cada gen pasaba entre estados inactivos y activos a lo largo del tiempo y entre sexos, mostrando que los genes específicos de macho suelen experimentar ganancias particularmente intensas en actividad regulatoria durante la formación del testículo. 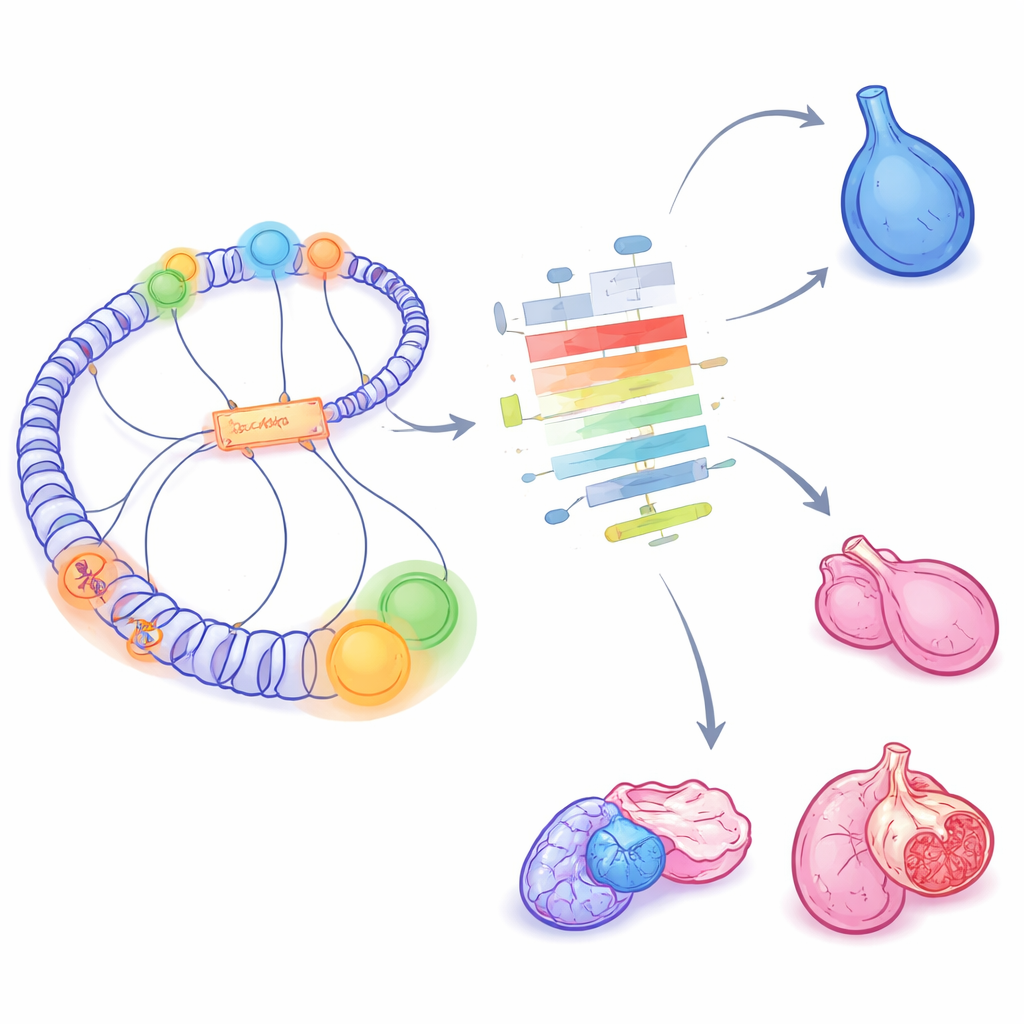
Un conmutador no codificante para un gen clave del sexo
Un ejemplo llamativo provino de Fgf9, un gen esencial para promover la vía testicular y bloquear la ovárica. Personas y ratones con defectos en FGF9 pueden presentar inversión sexual de macho a hembra, y sin embargo los elementos que controlan su actividad en la gónada eran desconocidos. Usando METALoci, los investigadores simularon la eliminación de pequeños fragmentos de ADN alrededor de Fgf9 in silico y evaluaron qué pérdidas desorganizarían su hub regulatorio 3D. Esto señaló a un tramo amplio libre de genes de alrededor de un cuarto de millón de bases corriente abajo. Cuando el equipo eliminó un fragmento de 306 kilobases que abarcaba la mayor parte de esta región en ratones, la expresión de Fgf9 en testículos fetales se redujo aproximadamente a la mitad. Los embriones XY desarrollaron gónadas que iban desde ovotestis mixtos hasta órganos con apariencia de ovario, reflejando de cerca los nulos completos de Fgf9—pero sin los defectos pulmonares letales que esos nulos suelen causar. Deleciones más pequeñas mostraron que gran parte del control se concentra en una subregión central de 93 kilobases, aunque el poder regulatorio se comparte entre varios enhancers, proporcionando redundancia.
Reguladores compartidos de la identidad masculina y femenina
Para entender cómo estos hubs se conectan en circuitos génicos más amplios, los autores combinaron sus mapas 3D con datos de ARN unicelular y reconstruyeron redes regulatorias. Encontraron factores determinantes del sexo conocidos en posiciones clave, pero también destacaron factores de transcripción no vinculados previamente a la determinación sexual. Entre ellos estaban Meis1 y Meis2, que surgieron como potentes “reguladores negativos” de los programas de diferenciación tanto masculinos como femeninos. Pruebas funcionales en ratones genéticamente modificados mostraron que eliminar Meis1 solo, o tres de las cuatro copias génicas Meis1/Meis2, provoca que parches de células en gónadas XY adopten identidad similar a la ovárica y, a la inversa, que algunas células XX adopten identidad similar a la testicular. Esto indica que los genes Meis actúan de forma redundante como guardianes de la identidad sexual adecuada en ambas direcciones.
Por qué importa este trabajo
Para el público no especializado, el mensaje clave es que la determinación del sexo no está controlada solo por qué genes posees, sino también por cómo se pliega tu ADN en 3D y cómo conglomerados de elementos reguladores distantes se comunican con sus genes diana. METALoci revela estos hubs ocultos y muestra que, incluso cuando el armazón general del genoma parece estable, el cableado interno dentro de los dominios puede reconfigurarse de forma drástica para cambiar el destino celular. Al identificar una región no codificante potente que gobierna Fgf9 y descubrir nuevos factores como los genes Meis, este trabajo ofrece pistas valiosas para comprender los trastornos del desarrollo sexual y demuestra cómo la cartografía del genoma 3D puede desvelar conmutadores reguladores cruciales que los enfoques tradicionales centrados en genes no detectan.
Cita: Mota-Gómez, I., Rodríguez, J.A., Dupont, S. et al. Chromatin spatial analysis by METALoci unveils sex-determining 3D regulatory hubs. Nat Struct Mol Biol 33, 577–589 (2026). https://doi.org/10.1038/s41594-026-01749-z
Palabras clave: determinación del sexo, genoma 3D, arquitectura de la cromatina, regulación génica, ADN no codificante