Clear Sky Science · ru
Пространственный анализ хроматина с помощью METALoci выявляет 3D-регуляторные узлы, определяющие пол
Как форма генома помогает определить пол
У каждого млекопитающего на ранних стадиях развития есть крошечные гонады, которые могут развиться либо в яички, либо в яичники. Нам давно известны многие гены, направляющие развитие в мужскую или женскую сторону, но гораздо меньше известно о том, как трехмерная укладка ДНК в ядре помогает принять это решение. В этом исследовании показано, что физическая организация хромосом формирует мощные центры управления — трехмерные регуляторные узлы — которые помогают решить, станет ли эмбриональная гонада яичком или яичником, и выявлены новые участники и скрытые переключатели, вовлеченные в это решение. 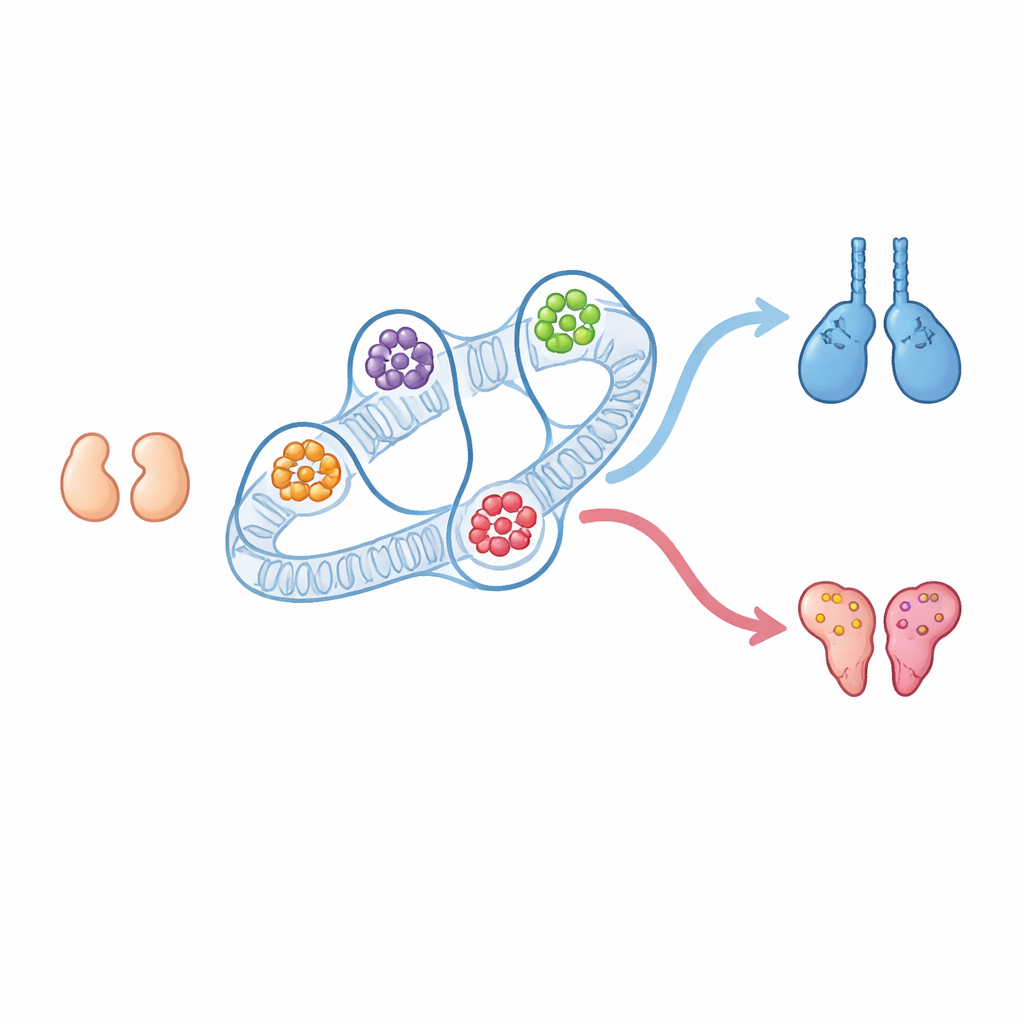
Ранняя гонада на распутье
В ранних эмбрионах мышей гонады у XX и XY особей выглядят и ведут себя практически одинаково. Они «бипотентны», то есть все ещё могут превратиться либо в яичники, либо в яички. Позже в XY-эмбрионах скачок активности Y-связанного гена Sry запускает путь развития в сторону яичек через ген Sox9 и сигнальную молекулу Fgf9, тогда как у XX-эмбрионов, у которых отсутствует Sry, включаются овариальные гены, такие как Wnt4 и Foxl2. Авторы выделили специфические поддерживающие клетки из этих ранних гонад до и после принятия полового решения и восстановили, как складывается их ДНК и какие участки активны. Удивительно, но широкие хромосомные «районы», которые контактируют друг с другом чаще всего — известные как компартменты и домены — почти не менялись между недифференцированным и половоспецифичным стадиями, несмотря на драматические сдвиги в активности генов.
Открытие скрытых 3D-регуляторных узлов
Это несоответствие между стабильной крупномасштабной укладкой и высоко динамичной активностью генов навело на мысль, что важные события происходят на более мелких масштабах. Чтобы раскрыть их, команда разработала METALoci — вычислительный метод, заимствующий приёмы из географии, где их используют для выявления «горячих точек», например, загрязнения в городе. Вместо городских кварталов METALoci рассматривает небольшие фрагменты генома как локации и использует Hi-C данные контактов, чтобы расположить их на виртуальной карте в соответствии с частотой взаимодействий. Затем он накладывает химические маркеры активности, такие как H3K27ac, чтобы идентифицировать «горячие» кластеры, где активные энхансеры и промоторы собираются в 3D-пространстве. Эти кластеры, или metaloci, действуют как регуляторные узлы, в которых группы ДНК-переключателей и их целевые гены работают совместно.
Перенастройка при определении пола
По всему геному METALoci показал, что эти 3D-узлы широко перенастраиваются по мере того, как гонады дифференцируются в яичники или яички. Количество сильно активных узлов примерно удвоилось во время дифференцировки, как и количество сильно неактивных зон, отражая одновременное включение и выключение целых генетических программ. Известные половые гены вели себя интуитивно: например, у Sox9 появился мощный активный узел в будущих сертоли (яичковые клетки), тогда как у Bmp2 сформировалась активная среда в будущих гранулёзных (яичниковых) клетках. Авторы проследили, как локальная среда каждого гена переходила между неактивными и активными состояниями во времени и между полами, показав, что у мужских специфичных генов обычно наблюдаются особенно сильные приросты регуляторной активности во время формирования яичек. 
Некодирующий переключатель для ключевого полового гена
Одним из ярких примеров стал Fgf9, ген, необходимый для продвижения пути формирования яичек и подавления овариального пути. У людей и мышей с дефектами FGF9 может происходить обращение пола с мужского на женский, однако элементы, контролирующие его активность в гонаде, были неизвестны. Используя METALoci, исследователи имитировали удаление небольших участков ДНК вокруг Fgf9 in silico и выясняли, какие потери нарушат его 3D-регуляторный узел. Это указало на обширный ген-свободный участок примерно в четверть миллиона пар оснований вниз по течению. Когда команда удалила 306-килобазный фрагмент, охватывающий большую часть этой области у мышей, экспрессия Fgf9 в эмбриональных яичках снизилась примерно вдвое. У XY-эмбрионов развивались гонады от смешанных овотестисов до органов, похожих на яичники, что тесно соответствовало полным нокаутам Fgf9 — но без летальных пороков лёгких, которые обычно сопровождают эти нокауты. Меньшие делеции показали, что значительная часть контроля сосредоточена в центральном 93-килобазном субрегионе, однако регуляторная сила распределена между несколькими энхансерами, обеспечивая избыточность.
Общие регуляторы мужской и женской идентичности
Чтобы понять, как эти узлы интегрируются в более широкие генетические цепи, авторы объединили свои 3D-карты с данными одиночных клеток по РНК и восстановили регуляторные сети. Они обнаружили известные факторы, определяющие пол, на ключевых позициях, но также выделили факторы транскрипции, ранее не связанные с определением пола. Среди них оказались Meis1 и Meis2, которые проявили себя как сильные «негативные регуляторы» обоих программ — как мужской, так и женской дифференцировки. Функциональные тесты в генетически модифицированных мышах показали, что удаление только Meis1 или трёх из четырёх копий генов Meis1/Meis2 вызывает появление участков клеток в XY-гонадах с овариальной идентичностью и, наоборот, в некоторых XX-клетках — тестикулоподобной идентичности. Это указывает на то, что гены Meis действуют в избыточности как стражи правильной половой идентичности в обоих направлениях.
Почему эта работа важна
Для неспециалиста ключевое послание состоит в том, что определение пола зависит не только от набора генов, но и от того, как ваша ДНК сложена в 3D и как кластеры удалённых регуляторных элементов связываются со своими целевыми генами. METALoci выявляет эти скрытые узлы и показывает, что даже при кажущейся стабильности общей структуры генома внутренняя проводка внутри доменов может радикально перенастраиваться, чтобы изменить судьбу клетки. Выявив мощный некодирующий регион, контролирующий Fgf9, и обнаружив новые факторы, такие как гены Meis, это исследование открывает новые пути для понимания расстройств развития пола и демонстрирует, как 3D-картирование генома может обнаруживать критические регуляторные переключатели, которые традиционные подходы, ориентированные на отдельные гены, пропускают.
Цитирование: Mota-Gómez, I., Rodríguez, J.A., Dupont, S. et al. Chromatin spatial analysis by METALoci unveils sex-determining 3D regulatory hubs. Nat Struct Mol Biol 33, 577–589 (2026). https://doi.org/10.1038/s41594-026-01749-z
Ключевые слова: определение пола, 3D геном, архитектура хроматина, регуляция генов, некодирующая ДНК