Clear Sky Science · pt
Análise espacial da cromatina por METALoci revela centros regulatórios 3D determinantes do sexo
Como a forma do genoma ajuda a decidir o sexo
Cada mamífero inicia a vida com gônadas pequenas que podem se tornar testículos ou ovários. Já conhecíamos muitos dos genes que empurram o desenvolvimento rumo ao sexo masculino ou feminino, mas sabemos bem menos sobre como o dobramento tridimensional do DNA dentro do núcleo orienta essa escolha. Este estudo mostra que o layout físico dos cromossomos cria centros de controle poderosos — hubs regulatórios tridimensionais — que ajudam a determinar se a gônada embrionária vira testículo ou ovário, e revela novos atores e chaves ocultas envolvidos nessa decisão. 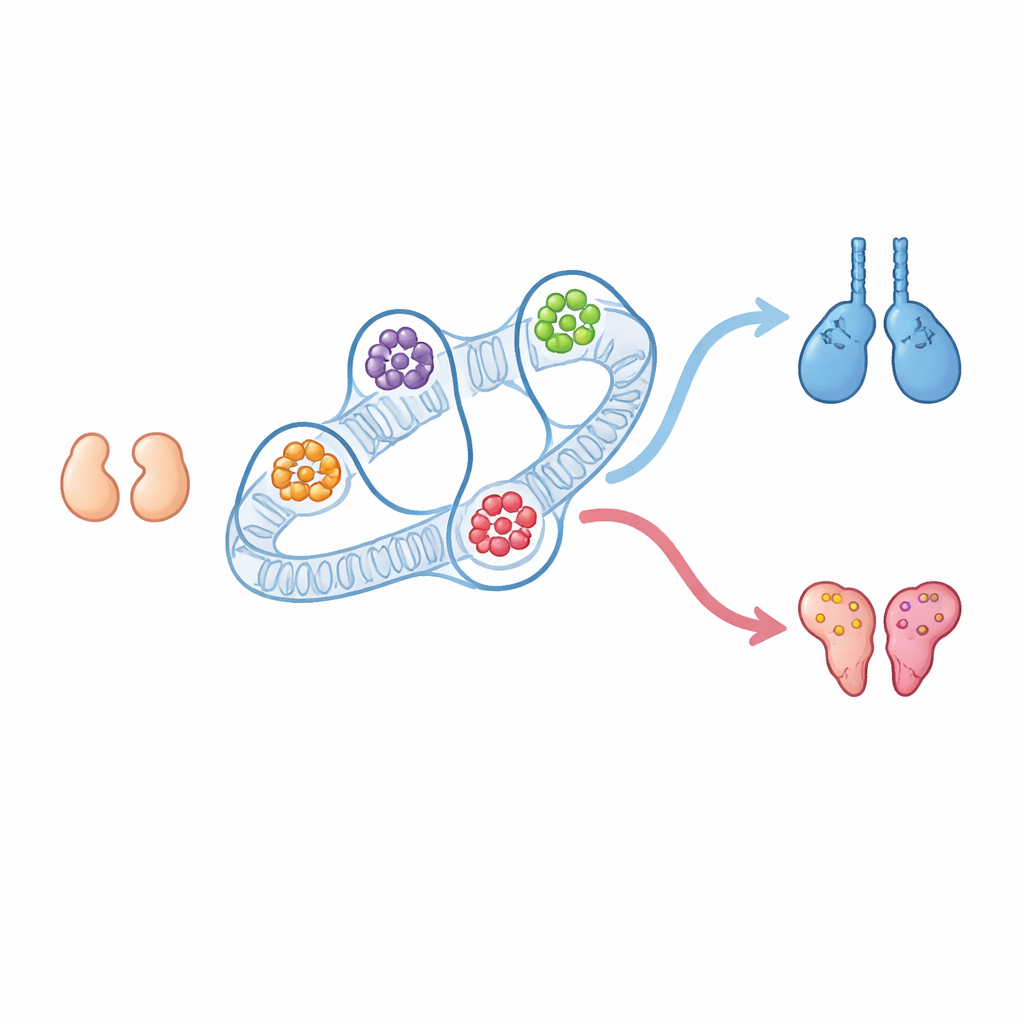
A gônada inicial em uma encruzilhada
Em embriões de camundongo no estágio inicial, as gônadas de indivíduos XX e XY parecem e se comportam quase da mesma forma. Elas são “bipotenciais”, ou seja, ainda podem se tornar ovários ou testículos. Mais tarde, um surto de atividade do gene Sry, que fica no cromossomo Y, em embriões XY desencadeia a via testicular através do gene Sox9 e do mensageiro Fgf9, enquanto embriões XX, que não têm Sry, ativam genes ovarianos como Wnt4 e Foxl2. Os autores isolaram células de suporte específicas dessas gônadas iniciais, tanto antes quanto depois da decisão de sexo, e mapearam como o DNA se dobra e quais regiões estão ativas. Surpreendentemente, os bairros cromossômicos amplos que mais se contatam — conhecidos como compartimentos e domínios — mal mudaram entre os estágios indiferenciados e os específicos do sexo, mesmo com mudanças dramáticas na atividade gênica.
Descobrindo hubs regulatórios 3D ocultos
Essa discrepância entre um dobramento em larga escala estável e uma atividade gênica altamente dinâmica sugeriu que a ação importante poderia ocorrer em escalas mais finas. Para descobri-la, a equipe desenvolveu o METALoci, um método computacional que toma emprestado ferramentas da geografia, onde são usadas para detectar pontos críticos, por exemplo, de poluição numa cidade. Em vez de quarteirões, o METALoci trata pequenos trechos do genoma como locais e usa dados de contato Hi-C para posicioná-los em um mapa virtual de acordo com a frequência com que se tocam. Em seguida, sobrepõe marcadores químicos de atividade, como H3K27ac, para identificar aglomerados “quentes” onde enhancers e promotores ativos se reúnem no espaço 3D. Esses aglomerados, ou metaloci, atuam como hubs regulatórios nos quais grupos de interruptores de DNA e seus genes-alvo trabalham em conjunto.
Reconfiguração durante a determinação sexual
Ao longo do genoma, o METALoci revelou que esses hubs 3D são amplamente reconfigurados à medida que as gônadas se comprometem com ovário ou testículo. O número de hubs fortemente ativos aproximadamente dobrou durante a diferenciação, assim como o número de zonas fortemente inativas, refletindo o ligar e desligar simultâneo de programas gênicos inteiros. Genes sexuais conhecidos se comportaram de maneira intuitiva: por exemplo, Sox9 ganhou um hub ativo forte em futuras células de Sertoli (testículo), enquanto Bmp2 adquiriu um ambiente ativo em futuras células da granulosa (ovário). Os autores acompanharam como o ambiente local de cada gene transitou entre estados inativos e ativos ao longo do tempo e entre sexos, mostrando que genes específicos do sexo masculino tipicamente experimentam ganhos particularmente fortes em atividade regulatória durante a formação do testículo. 
Um interruptor não codificante para um gene sexual-chave
Um exemplo marcante veio de Fgf9, um gene essencial para promover a via testicular e bloquear a via ovariana. Pessoas e camundongos com defeitos em FGF9 podem sofrer reversão sexual de masculino para feminino, porém os elementos que controlam sua atividade na gônada eram desconhecidos. Usando o METALoci, os pesquisadores simularam em silico a deleção de pequenos trechos de DNA ao redor de Fgf9 e perguntaram quais perdas perturbariam seu hub regulatório 3D. Isso apontou para um trecho amplo e sem genes de cerca de um quarto de milhão de bases a jusante. Quando a equipe removeu um bloco de 306 kilobases que abrange a maior parte dessa região em camundongos, a expressão de Fgf9 em testículos fetais caiu cerca de metade. Embriões XY desenvolveram gônadas que variaram de ovotestes mistos a órgãos com aspecto de ovário, espelhando de perto nocauteamentos completos de Fgf9 — porém sem os defeitos pulmonares letais que esses nocauteamentos normalmente causam. Deleções menores mostraram que grande parte do controle está concentrada em uma sub-região central de 93 kilobases, embora o poder regulatório seja compartilhado entre vários enhancers, conferindo redundância.
Reguladores compartilhados da identidade masculina e feminina
Para entender como esses hubs se conectam em circuitos gênicos mais amplos, os autores combinaram seus mapas 3D com dados de RNA de célula única e reconstruíram redes regulatórias. Eles encontraram fatores de determinação sexual conhecidos em posições-chave, mas também destacaram fatores de transcrição não previamente ligados à determinação sexual. Entre eles estavam Meis1 e Meis2, que emergiram como fortes “reguladores negativos” dos programas de diferenciação masculino e feminino. Testes funcionais em camundongos geneticamente modificados mostraram que remover apenas Meis1, ou três das quatro cópias dos genes Meis1/Meis2, provoca manchas de células em gônadas XY que assumem identidade semelhante à ovariana e, inversamente, algumas células XX que assumem identidade semelhante à testicular. Isso indica que os genes Meis atuam de forma redundante como guardiões da identidade sexual correta em ambas as direções.
Por que este trabalho importa
Para um público não especialista, a mensagem-chave é que a determinação sexual não é controlada apenas por quais genes você tem, mas também por como seu DNA é dobrado em 3D e por como aglomerados de elementos regulatórios distantes se comunicam com seus genes-alvo. O METALoci revela esses hubs ocultos e mostra que, mesmo quando a estrutura global do genoma parece estável, a fiação interna dentro dos domínios pode ser dramaticamente reconfigurada para mudar o destino celular. Ao identificar uma região não codificante poderosa que governa Fgf9 e ao descobrir novos fatores como os genes Meis, este trabalho oferece pistas novas para entender distúrbios do desenvolvimento sexual e demonstra como o mapeamento do genoma 3D pode revelar chaves regulatórias cruciais que abordagens tradicionais centradas em genes deixam passar.
Citação: Mota-Gómez, I., Rodríguez, J.A., Dupont, S. et al. Chromatin spatial analysis by METALoci unveils sex-determining 3D regulatory hubs. Nat Struct Mol Biol 33, 577–589 (2026). https://doi.org/10.1038/s41594-026-01749-z
Palavras-chave: determinação sexual, genoma 3D, arquitetura da cromatina, regulação gênica, DNA não codificante