Clear Sky Science · fr
Analyse spatiale de la chromatine par METALoci révèle des hubs régulateurs 3D déterminant le sexe
Comment la forme du génome aide à décider du sexe
Tous les mammifères commencent la vie avec de petites gonades capables de devenir soit des testicules, soit des ovaires. Nous connaissons depuis longtemps de nombreux gènes qui orientent le développement vers le mâle ou la femelle, mais beaucoup moins comment le repliement tridimensionnel de l’ADN dans le noyau participe à ce choix. Cette étude montre que l’agencement physique de nos chromosomes crée des centres de contrôle puissants — des hubs régulateurs tridimensionnels — qui contribuent à déterminer si la gonade embryonnaire deviendra testicule ou ovaire, et révèle de nouveaux acteurs et des interrupteurs cachés impliqués dans cette décision. 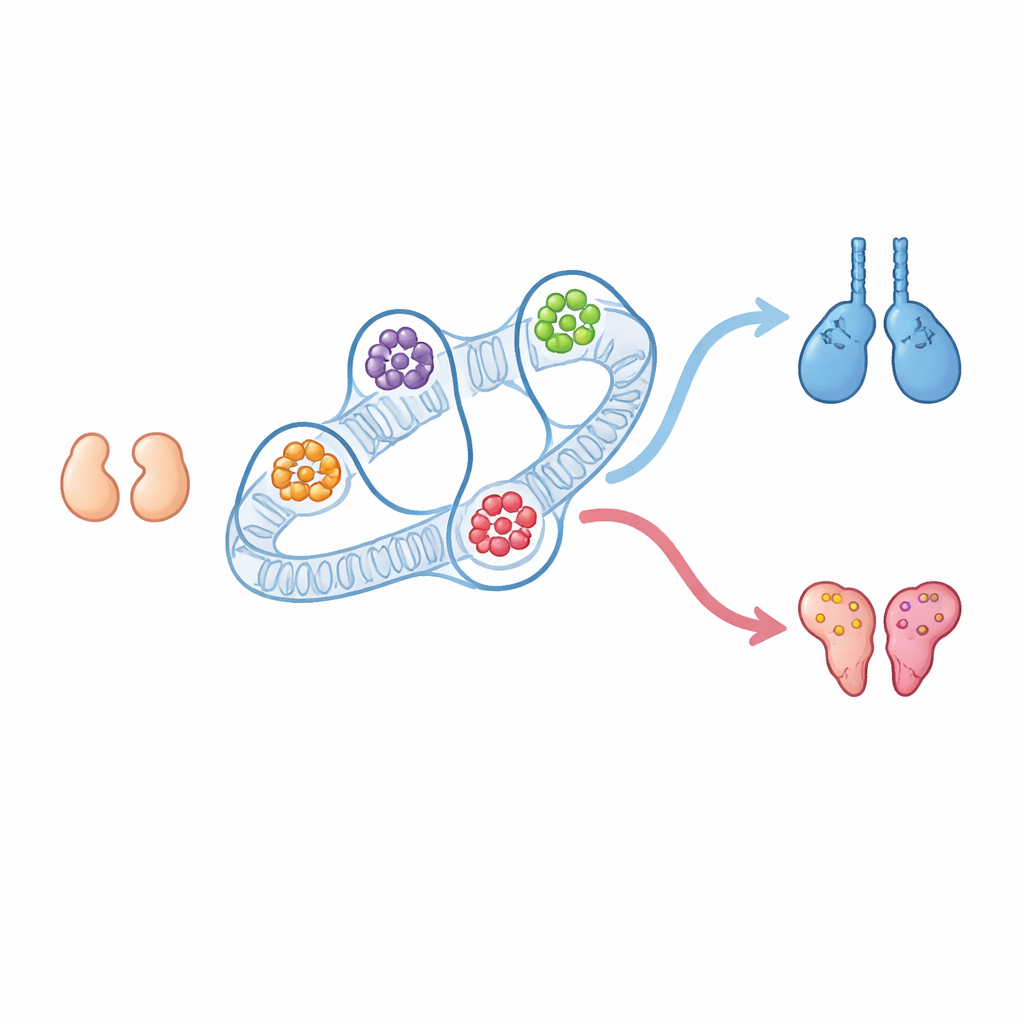
La jeune gonade à la croisée des chemins
Chez les premiers embryons de souris, les gonades des individus XX et XY semblent et se comportent presque de la même manière. Elles sont « bipotentielles », c’est‑à‑dire qu’elles peuvent encore devenir soit ovaires soit testicules. Plus tard, une explosion d’activité du gène Sry porté par le chromosome Y chez les embryons XY déclenche la voie testiculaire via le gène Sox9 et la molécule de signalisation Fgf9, tandis que les embryons XX, dépourvus de Sry, activent des gènes ovariens tels que Wnt4 et Foxl2. Les auteurs ont isolé des cellules souches de soutien spécifiques de ces gonades précoces, avant et après la décision sexuelle, et ont cartographié la façon dont leur ADN se replie et quelles régions sont actives. De manière surprenante, les grands quartiers chromosomiques qui se contactent le plus souvent — connus sous les noms de compartiments et de domaines — ont à peine changé entre les stades indéterminés et spécifiques au sexe, alors même que l’activité génique évolue de façon spectaculaire.
Découvrir des hubs de contrôle 3D cachés
Ce décalage entre la stabilité du repliement à grande échelle et la dynamique forte de l’activité génique suggérait que l’action importante se produisait à des échelles plus fines. Pour la mettre en évidence, l’équipe a développé METALoci, une méthode computationnelle qui emprunte des outils à la géographie, où ils servent à repérer des points chauds, par exemple de pollution, dans une ville. Au lieu des quartiers urbains, METALoci considère de petits segments du génome comme des lieux et utilise des données Hi‑C pour les placer sur une carte virtuelle selon la fréquence de leurs contacts. Elle superpose ensuite des marqueurs chimiques d’activité, tels que H3K27ac, pour identifier des amas « chauds » où enhancers et promoteurs actifs se rassemblent en 3D. Ces amas, ou metaloci, fonctionnent comme des hubs régulateurs dans lesquels des groupes d’interrupteurs d’ADN et leurs gènes cibles coopèrent.
Reconfiguration pendant la détermination sexuelle
À l’échelle du génome, METALoci a révélé que ces hubs 3D sont largement reconfigurés lorsque les gonades s’engagent vers l’ovaire ou le testicule. Le nombre de hubs fortement actifs a grossièrement doublé pendant la différenciation, de même que le nombre de zones fortement inactives, reflétant l’activation et l’inhibition simultanées de programmes géniques entiers. Les gènes sexuels connus se comportaient de façon intuitive : par exemple, Sox9 a gagné un hub actif puissant dans les futures cellules de Sertoli (testiculaires), tandis que Bmp2 a acquis un environnement actif dans les futures cellules de la granulosa (ovariens). Les auteurs ont suivi comment l’environnement local de chaque gène basculait entre états inactifs et actifs au fil du temps et entre les sexes, montrant que les gènes spécifiques au mâle subissent typiquement des gains particulièrement forts d’activité régulatrice lors de la formation du testicule. 
Un commutateur non codant pour un gène sexuel clé
Un exemple frappant concernait Fgf9, un gène essentiel pour promouvoir la voie testiculaire et bloquer la voie ovarienne. Des personnes et des souris présentant des défauts de FGF9 peuvent subir une inversion sexuelle mâle→femelle, pourtant les éléments qui contrôlent son activité dans la gonade étaient inconnus. En utilisant METALoci, les chercheurs ont simulé in silico la suppression de petits segments d’ADN autour de Fgf9 et ont cherché quelles pertes perturberaient son hub régulateur 3D. Cela a pointé une large étendue dépourvue de gènes, d’environ un quart de million de bases en aval. Lorsque l’équipe a supprimé un fragment de 306 kilobases couvrant la majeure partie de cette région chez la souris, l’expression de Fgf9 dans les testicules fœtaux a chuté d’environ moitié. Les embryons XY ont développé des gonades allant d’ovotestes mixtes à des organes de type ovaire, reproduisant fidèlement les phénotypes des knockouts complets de Fgf9 — mais sans les défauts pulmonaires létaux que ces knockouts provoquent habituellement. Des suppressions plus petites ont montré qu’une grande part du contrôle se concentre dans une sous‑région centrale de 93 kilobases, tandis que le pouvoir régulateur est partagé entre plusieurs enhancers, assurant une redondance.
Régulateurs partagés de l’identité mâle et femelle
Pour comprendre comment ces hubs s’intègrent dans des circuits géniques plus larges, les auteurs ont combiné leurs cartes 3D avec des données d’ARN unicellulaires et reconstruit des réseaux de régulation. Ils ont retrouvé des facteurs connus de détermination sexuelle à des positions clés, mais ont aussi mis en lumière des facteurs de transcription non auparavant liés à la détermination du sexe. Parmi eux figuraient Meis1 et Meis2, qui sont apparus comme de puissants « régulateurs négatifs » des programmes de différenciation mâle et femelle. Des tests fonctionnels chez des souris génétiquement modifiées ont montré que la suppression de Meis1 seule, ou de trois des quatre copies des gènes Meis1/Meis2, provoque des îlots de cellules dans les gonades XY adoptant une identité de type ovarien et, inversement, que certaines cellules XX prennent une identité de type testiculaire. Cela indique que les gènes Meis agissent de manière redondante comme gardiens de l’identité sexuelle correcte dans les deux directions.
Pourquoi ce travail est important
Pour un public non spécialiste, le message clé est que la détermination du sexe n’est pas contrôlée uniquement par les gènes que vous possédez, mais aussi par la manière dont votre ADN est replié en 3D et par la façon dont des groupes d’éléments régulateurs distants communiquent avec leurs gènes cibles. METALoci révèle ces hubs cachés et montre que, même lorsque l’ossature générale du génome semble stable, le câblage interne au sein des domaines peut être radicalement réorganisé pour orienter le destin cellulaire. En identifiant une région non codante puissante qui régit Fgf9 et en découvrant de nouveaux facteurs comme les gènes Meis, ce travail propose de nouvelles pistes pour comprendre les troubles du développement sexuel et démontre comment la cartographie du génome 3D peut mettre au jour des commutateurs régulateurs cruciaux que les approches traditionnelles centrées sur les gènes manquent.
Citation: Mota-Gómez, I., Rodríguez, J.A., Dupont, S. et al. Chromatin spatial analysis by METALoci unveils sex-determining 3D regulatory hubs. Nat Struct Mol Biol 33, 577–589 (2026). https://doi.org/10.1038/s41594-026-01749-z
Mots-clés: détermination du sexe, génome 3D, architecture de la chromatine, régulation des gènes, ADN non codant