Clear Sky Science · sv
CREsted: modellering av genomiska och syntetiska celltypsspecifika förstärkare över vävnader och arter
Varför små brytare i DNA spelar roll
Varje cell i din kropp bär på samma DNA, ändå beter sig hjärnceller, blodceller och muskelceller mycket olika. En stor anledning är ett dolt kontrollager bestående av korta DNA‑brytare kallade förstärkare, som avgör när och var gener aktiveras. Denna artikel presenterar CREsted, ett programverktyg som använder modern artificiell intelligens för att läsa dessa brytare direkt från DNA och till och med designa nya. Arbetet visar hur vi kan gå från att bara lista genetiska delar till att aktivt förstå och konstruera dem över vävnader och arter.
Läsa cellens kontrollbrytare
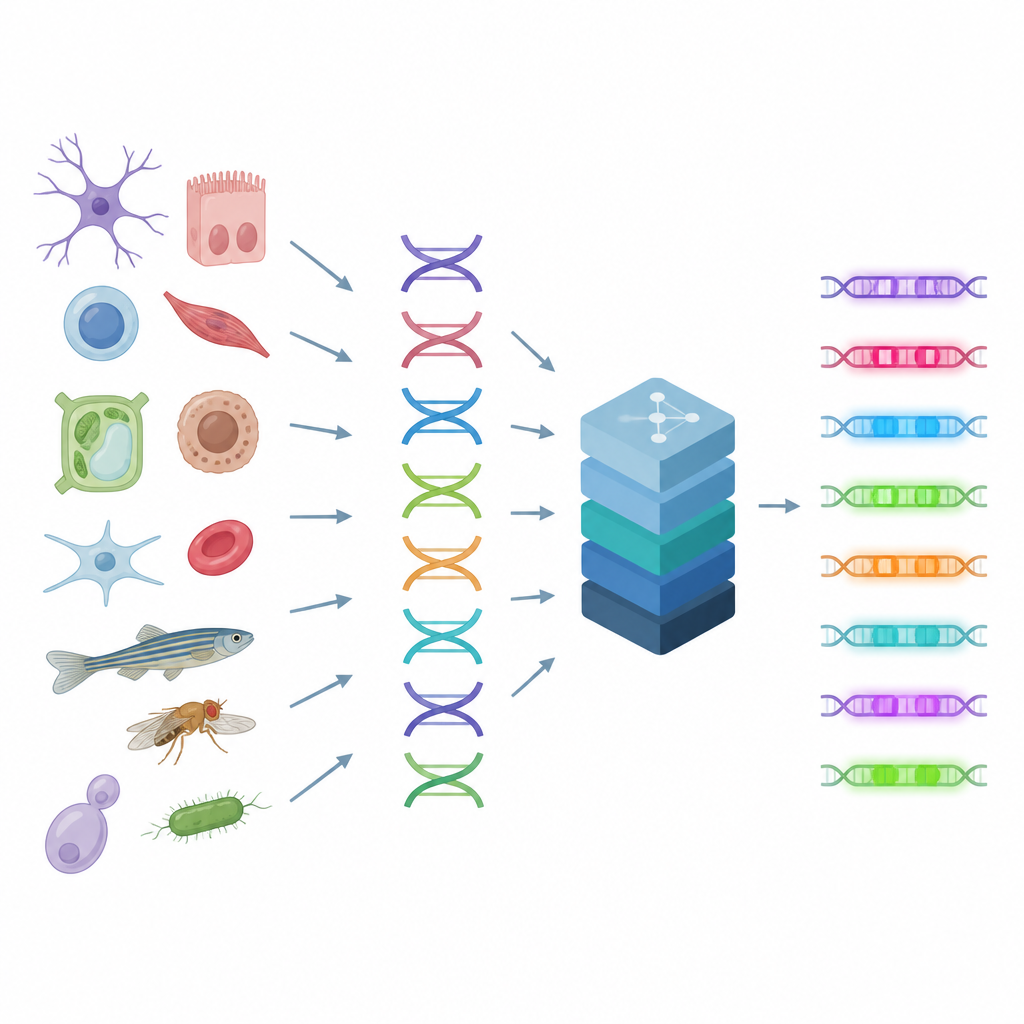
Förstärkare fungerar som rattar på ett ljudbord och kombinerar signaler från många proteiner för att finjustera genaktiviteten i varje celltyp. Eftersom flera DNA‑mönster kan ge liknande utfall är reglerna bakom förstärkare komplexa och svåra att gissa med blotta ögat. Författarna bygger vidare på en teknik som mäter hur öppen eller stängd varje DNA‑region är i tusentals enskilda celler — en ledtråd som avslöjar var aktiva förstärkare sitter i genomet. CREsted tar dessa mätningar, länkar dem till den underliggande DNA‑sekvensen och tränar djupinlärningsmodeller för att förutsäga hur åtkomlig varje region kommer att vara i många celltyper samtidigt. Detta förvandlar rå sekvens till en karta över regulatorisk aktivitet.
Ett verktyg från data till insikt
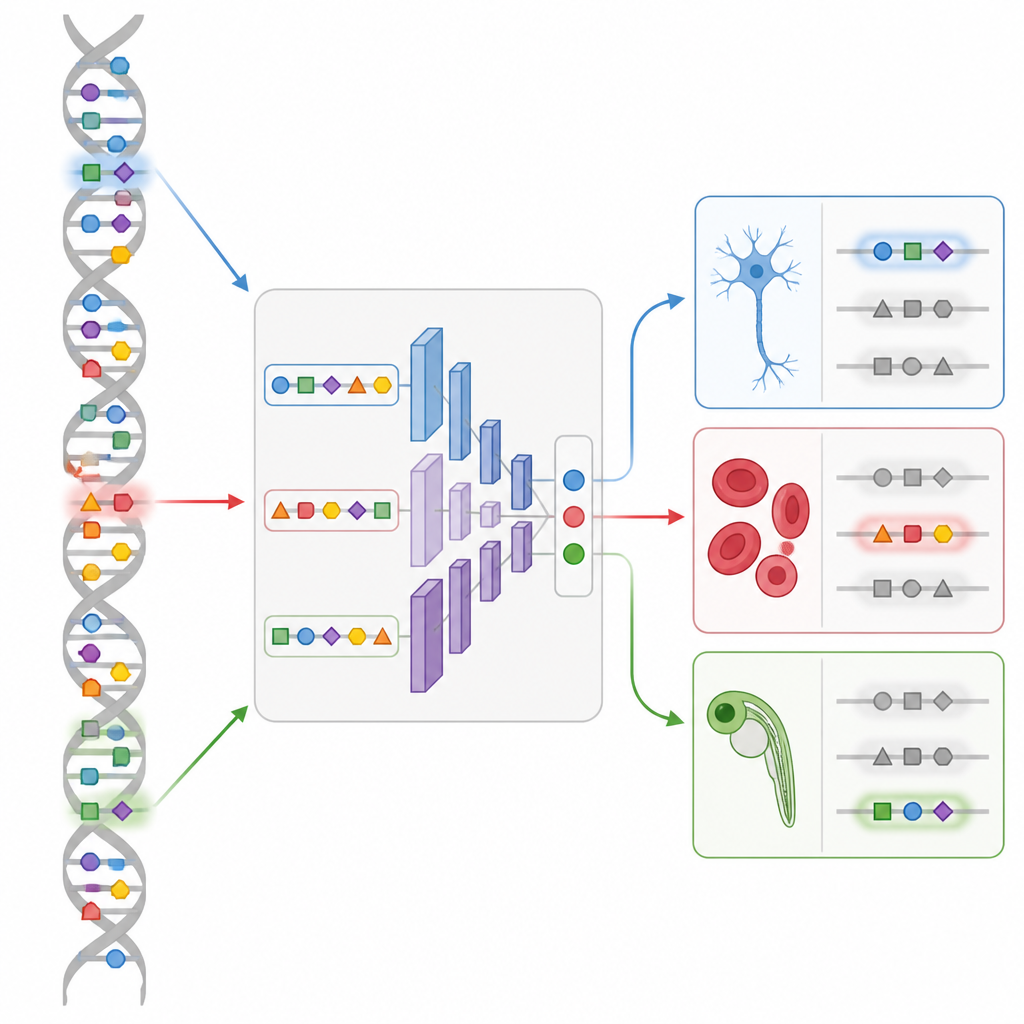
CREsted är mer än en enskild modell: det är en hel pipeline. Först rensar och omformar den enkelcellsdata till ett format som minskar tekniska snedvridningar mellan celltyper. Därefter tränar den flexibla neurala nätverk som antingen kan klassificera aktiva regioner eller förutsäga graderade åtkomlighetsvärden. Viktigt är att CREsted inte stannar vid prediktion. Det kan zooma in för att identifiera vilka enskilda DNA‑bokstäver som betyder mest för en given celltyp, klustra återkommande mönster och matcha dessa mönster till sannolika regulatoriska proteiner med hjälp av befintliga databaser och genuttrycksdata. Slutligen innehåller det designverktyg som iterativt ”utvecklar” syntetiska DNA‑sekvenser så att modellen förutser stark aktivitet i en utvald celltyp och liten aktivitet på andra ställen.
Testning av verktyget i hjärna, blod, cancer och fisk
Författarna visar upp CREsted på flera rika dataset. I musens motoriska cortex förutspår deras modeller vilka DNA‑regioner som är öppna i olika neuron‑ och stödcellstyper med hög noggrannhet och överträffar en ledande allmänram. Genom att lyfta fram viktiga sekvensmönster återfinner CREsted kända regulatoriska proteiner för specifika neuronklasser och kan till och med förklara hur en enda bokstavsändring i ett motif kan växla aktivitet mellan neuron‑subtyper. I mänskliga blodceller återupptäcker en relaterad modell många tidigare testade bindningsställen i klassiska immunsförstärkare och ligger väl i linje med oberoende protebindningsexperiment, vilket stöder att de inlärda sekvensmönstren är biologiskt meningsfulla.
CREsted undersöker också mer tillämpade frågor. Inom cancer jämför man ett ”mesenkymal‑likt” celltillstånd som förekommer i både melanom och glioblastom, med modeller tränade på cellinjer och på patienttumörprover. Förstärkarna visar delade teman men också viktiga skillnader, såsom specifika motif som bara finns i tumörer. I ett annat test frågar författarna om specialiserade ”foundation”‑modeller tränade på enorma genomiska dataset verkligen överträffar mindre, uppgiftsfokuserade modeller. Efter noggrann finjustering kämpar dessa stora modeller fortfarande med att matcha CREsteds egen arkitekturs celltypsspecifika upplösning, vilket antyder att dedikerad träning på högkvalitativ enkelcellsdata förblir avgörande.
Designa nya brytare i ett levande embryo
Den mest slående demonstrationen kommer från zebrafiskens utveckling. Med en enkelcellskarta över DNA‑åtkomlighet i många embryostadier tränar teamet en CREsted‑modell kallad DeepZebrafish. Sedan låter de designmodulen generera helt syntetiska förstärkare som förutses slå på endast i hjärtmuskel, endast i kroppsmuskel, endast i blodkärlsendotel eller i kontrollerade kombinationer av hjärta och muskel. När dessa artificiella sekvenser placeras framför en fluorescerande rapportör och injiceras i fiskägg, lyser många upp exakt i de avsedda vävnaderna. Analys av deras sekvenser avslöjar igenkännbara mönster för stora utvecklingsregulatorer, vilket bekräftar att modellen fångat meningsfull ”grammatik” snarare än slumpmässiga egenheter.
Vad detta betyder för förståelse och ingenjörskonst av genom
För en icke‑specialist kan CREsted ses som ett mikroskop för genomet regulatoriska lager och ett ritverktyg för nya genetiska delar. Det översätter DNA‑stycken till förutsägelser om vilka celltyper som kommer att använda dem, pekar ut de nyckelbokstäver och motif som driver detta beteende och kan föreslå nya sekvenser som bör uppträda på önskat sätt. Genom att arbeta över hjärna, blod, cancer och hela utvecklande djur visar studien att ett enhetligt tillvägagångssätt kan avslöja både delade och celltypsspecifika regler för genkontroll. På längre sikt kan sådana verktyg hjälpa forskare att bygga mer precisa genetiska markörer, förbättra sjukdomsmodeller och bättre förstå hur små förändringar i DNA kan få ringar på vattnet genom celler och vävnader.
Citering: Kempynck, N., De Winter, S., Blaauw, C.H. et al. CREsted: modeling genomic and synthetic cell-type-specific enhancers across tissues and species. Nat Methods 23, 946–959 (2026). https://doi.org/10.1038/s41592-026-03057-2
Nyckelord: modellering av förstärkare, djupinlärning i genomik, enkelcells‑kromatin, cis‑regulatoriska element, syntetiska förstärkare