Clear Sky Science · es
CREsted: modelado de potenciadores genómicos y sintéticos específicos de tipo celular a través de tejidos y especies
Por qué importan los diminutos interruptores del ADN
Cada célula de tu cuerpo contiene el mismo ADN, pero las neuronas, las células sanguíneas y las musculares se comportan de forma muy distinta. Una razón importante es una capa de control oculta formada por cortos interruptores de ADN llamados potenciadores, que deciden cuándo y dónde se activan los genes. Este artículo presenta CREsted, un conjunto de herramientas de software que usa inteligencia artificial moderna para leer estos interruptores directamente del ADN e incluso diseñar otros nuevos. El trabajo muestra cómo podemos pasar de simplemente listar piezas genéticas a comprenderlas y diseñarlas activamente a través de tejidos y especies.
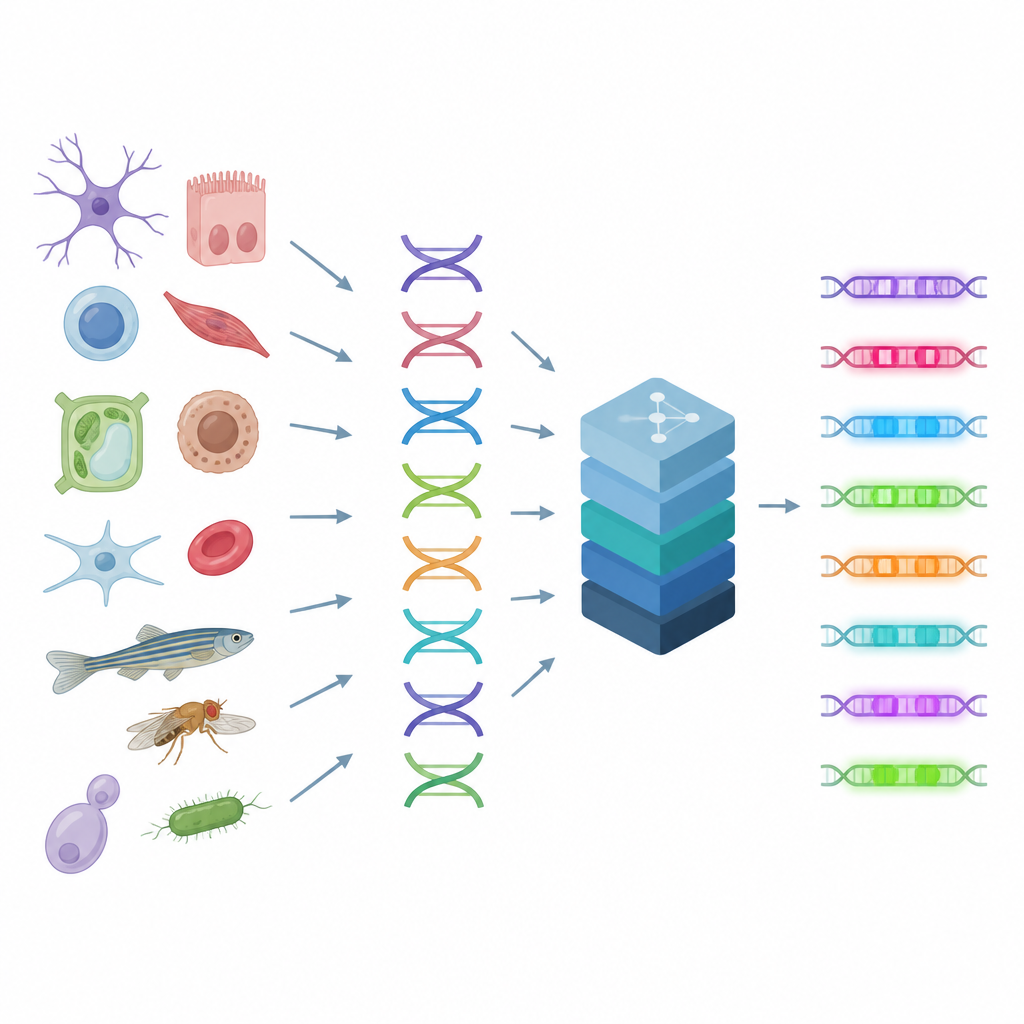
Leer los interruptores de control de la célula
Los potenciadores actúan como perillas en una mesa de mezclas, combinando señales de muchas proteínas para ajustar la actividad génica en cada tipo celular. Dado que varios patrones de ADN pueden producir resultados similares, las reglas que rigen los potenciadores son complejas y difíciles de deducir a simple vista. Los autores se basan en una técnica que mide qué tramos de ADN están abiertos o cerrados en miles de células individuales, una pista que revela dónde se ubican los potenciadores activos en el genoma. CREsted toma estas mediciones, las vincula con las secuencias de ADN subyacentes y entrena modelos de aprendizaje profundo para predecir cómo de accesible será cada región en muchos tipos celulares a la vez. Esto convierte la secuencia cruda en un mapa de actividad reguladora.
Un kit de herramientas de los datos al conocimiento
CREsted es más que un único modelo: es una canalización de extremo a extremo. Primero limpia y transforma los datos de célula única en una forma que reduce el sesgo técnico entre tipos celulares. Luego entrena redes neuronales flexibles que pueden clasificar regiones activas o predecir valores de accesibilidad graduados. De forma importante, CREsted no se limita a la predicción. Puede acercarse para identificar qué letras individuales del ADN importan más para un tipo celular dado, agrupar patrones recurrentes y asociar esos patrones con proteínas reguladoras probables usando bases de datos existentes y datos de expresión génica. Finalmente, incluye herramientas de diseño que “evolucionan” iterativamente secuencias de ADN sintéticas para que el modelo prediga una fuerte actividad en un tipo celular elegido y poca actividad en otros.
Probar la herramienta en cerebro, sangre, cáncer y pez
Los autores muestran CREsted en varios conjuntos de datos ricos. En la corteza motora de ratón, sus modelos predicen con alta precisión qué regiones del ADN están abiertas en diferentes tipos de neuronas y células de soporte, y superan a un marco de referencia de uso general. Al resaltar patrones de secuencia clave, CREsted recupera proteínas reguladoras conocidas para clases neuronales específicas e incluso puede explicar cómo un cambio de una sola letra en un motivo puede cambiar la actividad entre subtipos neuronales. En células sanguíneas humanas, un modelo relacionado redescubre muchos sitios de unión previamente probados en potenciadores inmunitarios clásicos y se alinea bien con experimentos independientes de unión de proteínas, lo que respalda que los patrones de secuencia aprendidos son biológicamente significativos.
CREsted también explora preguntas más aplicadas. En cáncer, compara un estado celular “tipo mesenquimal” que aparece tanto en melanoma como en glioblastoma, usando modelos entrenados en líneas celulares y en muestras tumorales de pacientes. Los patrones de potenciadores muestran temas compartidos pero también diferencias importantes, como motivos específicos presentes solo en tumores. En otra prueba, los autores preguntan si modelos “fundacionales” especializados entrenados con vastos conjuntos de datos genómicos realmente superan a modelos más pequeños y enfocados en la tarea. Tras una afinación cuidadosa, estos modelos grandes siguen teniendo dificultades para igualar la resolución específica de tipo celular de la propia arquitectura de CREsted, lo que sugiere que el entrenamiento dedicado con datos de célula única de alta calidad sigue siendo crucial.
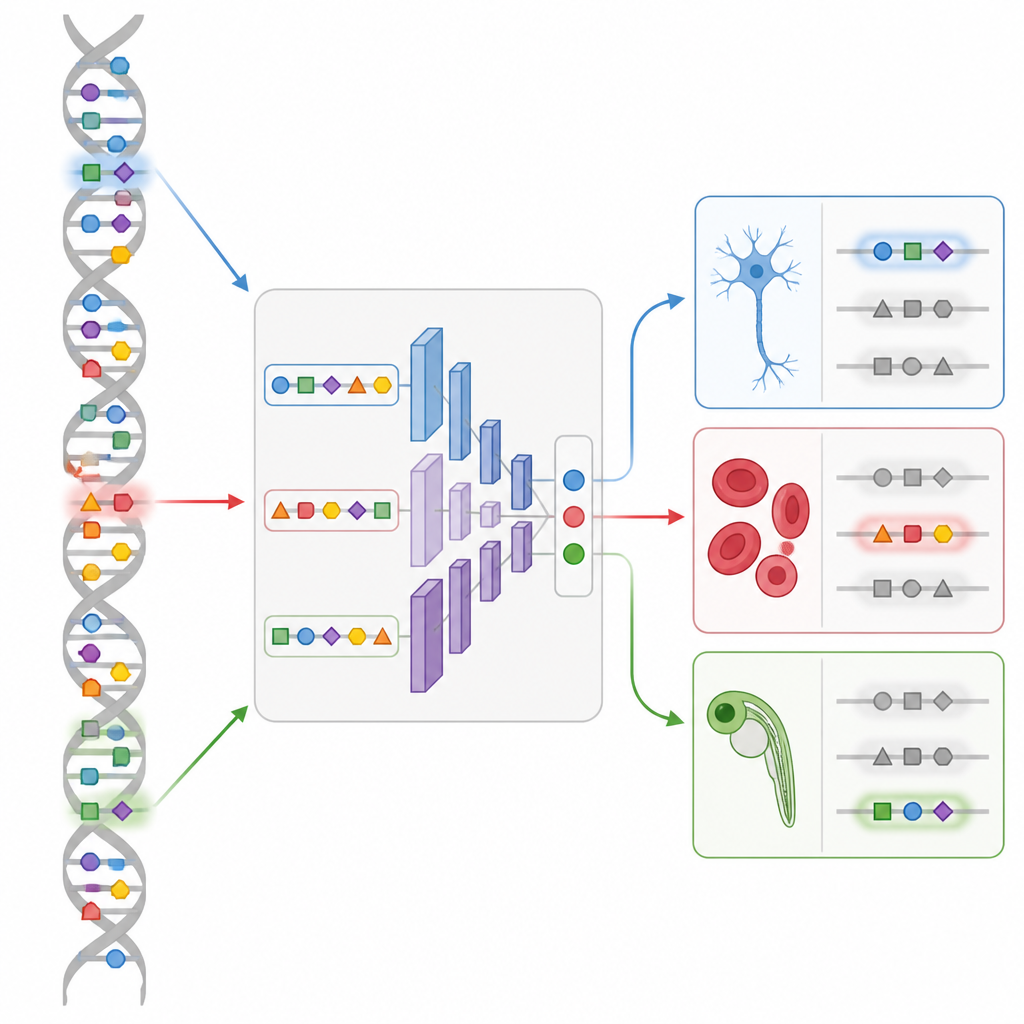
Diseñar nuevos interruptores en un embrión vivo
La demostración más llamativa proviene del desarrollo del pez cebra. Utilizando un mapa de accesibilidad del ADN a nivel de célula única a lo largo de varias etapas del embrión, el equipo entrena un modelo CREsted llamado DeepZebrafish. A continuación, el módulo de diseño genera potenciadores completamente sintéticos que se predice se activarán solo en músculo cardíaco, solo en músculo corporal, solo en el revestimiento de vasos sanguíneos o en combinaciones controladas de corazón y músculo. Cuando estas secuencias artificiales se colocan delante de un reportero fluorescente e inyectan en huevos de pez, muchas se iluminan exactamente en los tejidos previstos. El análisis de sus secuencias revela patrones reconocibles de reguladores del desarrollo principales, confirmando que el modelo ha capturado una “gramática” significativa más que curiosidades aleatorias.
Qué significa esto para comprender e ingeniería de genomas
Para un no especialista, CREsted puede verse como un microscopio para la capa reguladora del genoma y una herramienta de diseño para nuevas piezas genéticas. Traduce tramos de ADN en predicciones sobre qué tipos celulares los usarán, señala las letras y los motivos clave que impulsan ese comportamiento y puede sugerir nuevas secuencias que deberían comportarse de la manera deseada. Al trabajar en cerebro, sangre, cáncer y animales en desarrollo completos, el estudio muestra que un enfoque unificado puede revelar reglas compartidas y específicas de tipo celular del control génico. A largo plazo, tales herramientas pueden ayudar a los investigadores a construir marcadores genéticos más precisos, mejorar modelos de enfermedad y comprender mejor cómo pequeños cambios en el ADN pueden propagarse a través de células y tejidos.
Cita: Kempynck, N., De Winter, S., Blaauw, C.H. et al. CREsted: modeling genomic and synthetic cell-type-specific enhancers across tissues and species. Nat Methods 23, 946–959 (2026). https://doi.org/10.1038/s41592-026-03057-2
Palabras clave: modelado de potenciadores, genómica con aprendizaje profundo, cromatina de célula única, elementos reguladores cis, potenciadores sintéticos