Clear Sky Science · pt
CREsted: modelando aprimoradores genômicos e sintéticos específicos por tipo celular através de tecidos e espécies
Por que pequenos interruptores no DNA importam
Cada célula do seu corpo carrega o mesmo DNA, ainda assim células do cérebro, do sangue e do músculo se comportam de forma muito diferente. Uma grande razão é uma camada oculta de controle composta por pequenos interruptores de DNA chamados aprimoradores, que decidem quando e onde genes são ativados. Este artigo apresenta o CREsted, um conjunto de ferramentas que usa inteligência artificial moderna para ler esses interruptores diretamente do DNA e até projetar novos. O trabalho mostra como podemos passar de simplesmente listar partes genéticas para compreender e engenheirar ativamente essas partes através de tecidos e espécies.
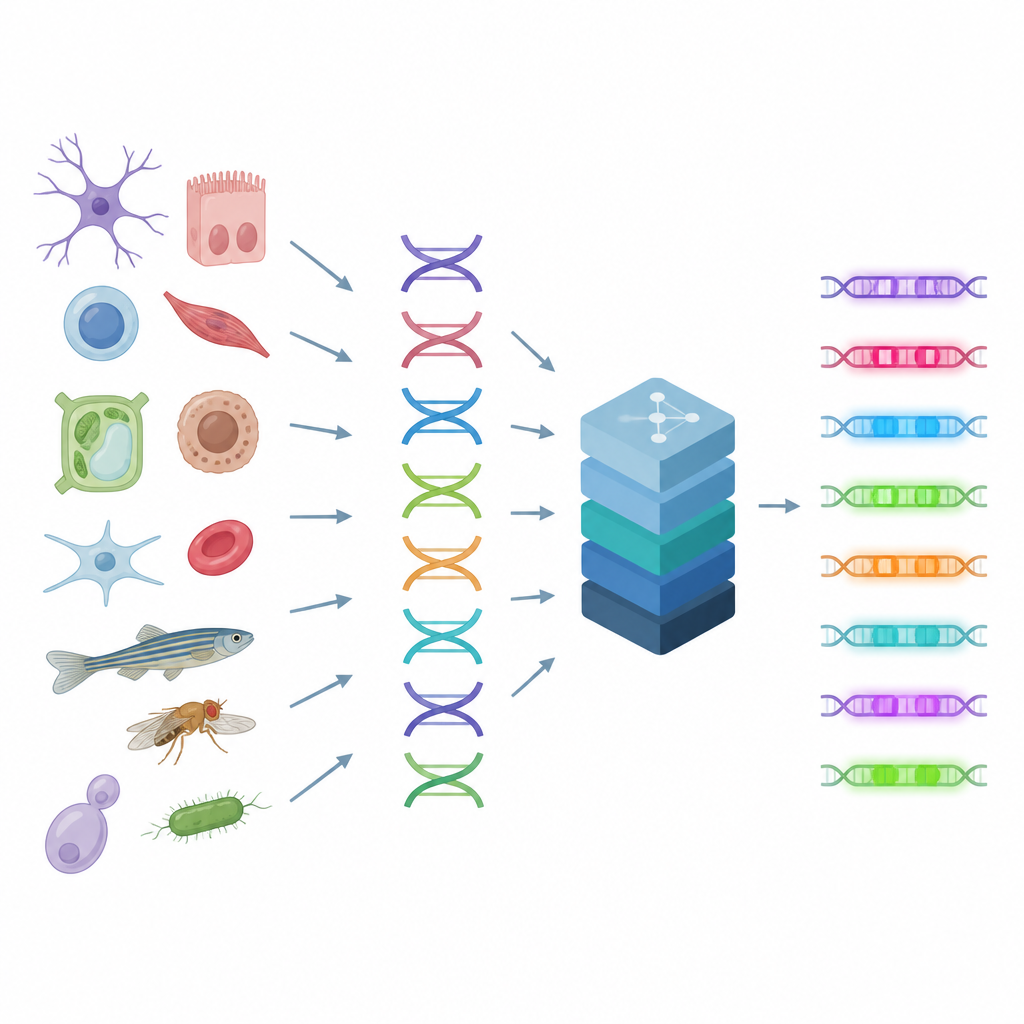
Lendo os interruptores de controle da célula
Os aprimoradores atuam como botões em uma mesa de som, combinando sinais de muitas proteínas para ajustar finamente a atividade gênica em cada tipo celular. Como múltiplos padrões de DNA podem produzir resultados semelhantes, as regras por trás dos aprimoradores são complexas e difíceis de inferir à vista. Os autores se baseiam em uma técnica que mede quão aberto ou fechado cada trecho de DNA está em milhares de células individuais, uma pista que revela onde se localizam aprimoradores ativos no genoma. O CREsted usa essas medições, as conecta às sequências de DNA subjacentes e treina modelos de deep learning para prever quão acessível cada região será em muitos tipos celulares ao mesmo tempo. Isso transforma sequência bruta em um mapa de atividade regulatória.
Um conjunto de ferramentas dos dados à compreensão
O CREsted é mais que um único modelo: é um pipeline de ponta a ponta. Primeiro limpa e remodela dados de célula única em uma forma que reduz viés técnico entre tipos celulares. Em seguida, treina redes neurais flexíveis que podem tanto classificar regiões ativas quanto prever valores graduais de acessibilidade. Importante, o CREsted não para na predição. Ele pode ampliar para identificar quais letras individuais do DNA importam mais para um dado tipo celular, agrupar padrões recorrentes e emparelhar esses padrões a proteínas regulatórias prováveis usando bancos de dados existentes e dados de expressão gênica. Por fim, inclui ferramentas de design que iterativamente “evoluem” sequências de DNA sintéticas para que o modelo preveja forte atividade em um tipo celular escolhido e pouca atividade em outros.
Testando o conjunto de ferramentas em cérebro, sangue, câncer e peixes
Os autores demonstram o CREsted em vários conjuntos de dados ricos. No córtex motor de camundongo, seus modelos prevêem com alta precisão quais regiões do DNA estão abertas em diferentes tipos de neurônios e células de suporte, superando uma estrutura de propósito geral líder. Ao destacar padrões de sequência chave, o CREsted recupera proteínas reguladoras conhecidas para classes específicas de neurônios e pode até explicar como uma mudança de uma única letra em um motivo pode alternar a atividade entre subtipos neuronais. Em células sanguíneas humanas, um modelo relacionado redescobre muitos sítios de ligação previamente testados em aprimoradores imunológicos clássicos e alinha-se bem com experimentos independentes de ligação proteica, apoiando que os padrões de sequência aprendidos são biologicamente significativos.
O CREsted também investiga questões mais aplicadas. Em câncer, compara um estado celular “semelhante a mesenquimal” que aparece tanto em melanoma quanto em glioblastoma, usando modelos treinados em linhagens celulares e em amostras tumorais de pacientes. Os padrões de aprimoradores mostram temas compartilhados, mas também diferenças importantes, como motivos específicos presentes apenas em tumores. Em outro teste, os autores perguntam se modelos “fundação” especializados treinados em vastos conjuntos genômicos realmente superam modelos menores e focados em tarefas. Após ajuste fino cuidadoso, esses grandes modelos ainda têm dificuldade em igualar a resolução específica por tipo celular da própria arquitetura do CREsted, sugerindo que treinamento dedicado em dados de célula única de alta qualidade continua sendo crucial.
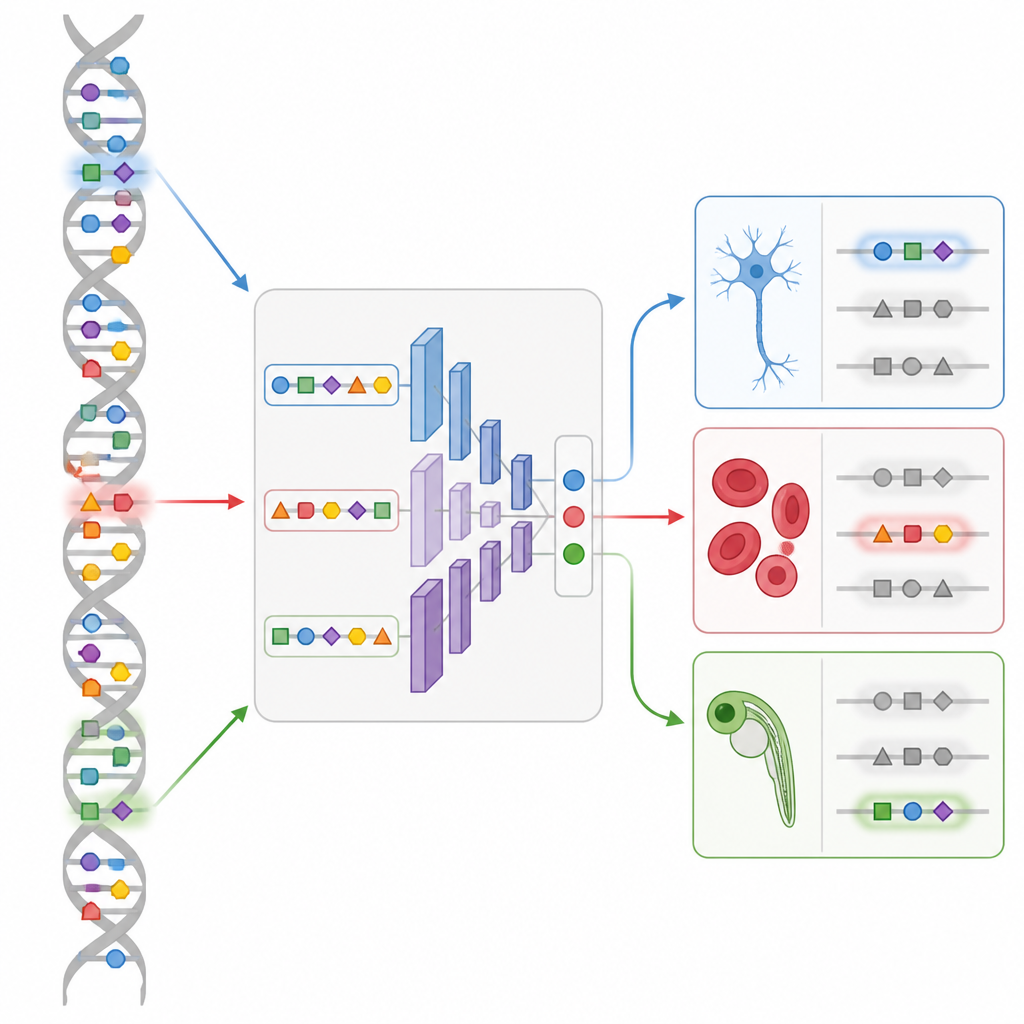
Projetando novos interruptores em um embrião vivo
A demonstração mais marcante vem do desenvolvimento do peixe-zebra. Usando um mapa de acessibilidade do DNA em célula única ao longo de muitos estágios do embrião, a equipe treina um modelo CREsted chamado DeepZebrafish. Eles então deixam o módulo de design gerar aprimoradores completamente sintéticos previstos para ativar somente em músculo cardíaco, somente em músculo corporal, somente no revestimento de vasos sanguíneos, ou em combinações controladas de coração e músculo. Quando essas sequências artificiais são colocadas diante de um repórter fluorescente e injetadas em ovos de peixe, muitas acendem exatamente nos tecidos pretendidos. A análise de suas sequências revela padrões reconhecíveis para reguladores de desenvolvimento principais, confirmando que o modelo capturou uma “gramática” significativa em vez de peculiaridades aleatórias.
O que isso significa para entender e engenheirar genomas
Para um não especialista, o CREsted pode ser visto como um microscópio para a camada regulatória do genoma e uma ferramenta de projeto para novas partes genéticas. Ele traduz trechos de DNA em previsões sobre quais tipos celulares os utilizarão, aponta as letras e motivos chave que dirigem esse comportamento e pode sugerir novas sequências que devam se comportar de maneira desejada. Ao trabalhar através de cérebro, sangue, câncer e animais em desenvolvimento, o estudo mostra que uma abordagem unificada pode revelar tanto regras compartilhadas quanto específicas por tipo celular do controle gênico. A longo prazo, tais ferramentas podem ajudar pesquisadores a construir marcadores genéticos mais precisos, melhorar modelos de doença e compreender melhor como pequenas mudanças no DNA podem repercutir através de células e tecidos.
Citação: Kempynck, N., De Winter, S., Blaauw, C.H. et al. CREsted: modeling genomic and synthetic cell-type-specific enhancers across tissues and species. Nat Methods 23, 946–959 (2026). https://doi.org/10.1038/s41592-026-03057-2
Palavras-chave: modelagem de aprimadores, genômica por deep learning, cromatina de célula única, elementos regulatórios cis, aprimoradores sintéticos