Clear Sky Science · fr
CREsted : modéliser des enhancers génomiques et synthétiques spécifiques aux types cellulaires à travers tissus et espèces
Pourquoi de tout petits interrupteurs dans l’ADN comptent
Toutes les cellules de votre corps portent le même ADN, et pourtant les cellules du cerveau, du sang et du muscle se comportent de façon très différente. Une grande part de cette différence tient à une couche de contrôle cachée composée de courts interrupteurs d’ADN appelés enhancers, qui décident quand et où les gènes s’activent. Cet article présente CREsted, une boîte à outils logicielle qui utilise l’intelligence artificielle moderne pour lire ces interrupteurs directement à partir de l’ADN et même en concevoir de nouveaux. Le travail montre comment passer de la simple énumération de composants génétiques à la compréhension active et à l’ingénierie de ces éléments à travers tissus et espèces.
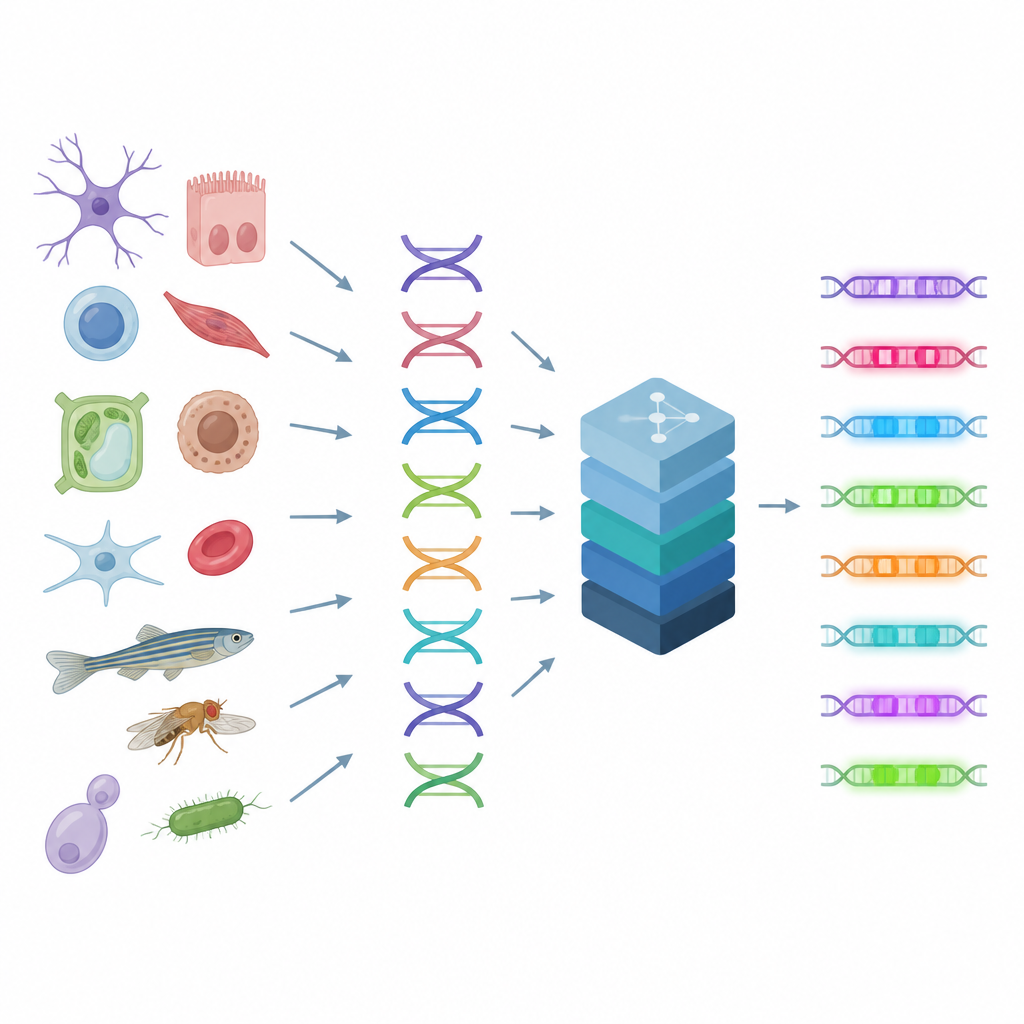
Lire les interrupteurs de contrôle de la cellule
Les enhancers fonctionnent comme des boutons sur une table de mixage, combinant des signaux de nombreuses protéines pour ajuster finement l’activité des gènes selon le type cellulaire. Parce que plusieurs motifs d’ADN peuvent produire des résultats similaires, les règles qui gouvernent les enhancers sont complexes et difficiles à deviner à l’œil nu. Les auteurs s’appuient sur une technique qui mesure à quel point chaque segment d’ADN est ouvert ou fermé dans des milliers de cellules individuelles, un indice révélant où se situent les enhancers actifs dans le génome. CREsted prend ces mesures, les relie aux séquences d’ADN sous-jacentes et entraîne des modèles d’apprentissage profond pour prédire la probabilité d’accessibilité de chaque région dans de nombreux types cellulaires simultanément. Cela transforme la séquence brute en une carte d’activité régulatrice.
Une boîte à outils allant des données à l’intelligence
CREsted est plus qu’un modèle unique : c’est un pipeline de bout en bout. Il nettoie d’abord et reformate les données unicellulaires pour réduire les biais techniques entre types cellulaires. Puis il entraîne des réseaux neuronaux flexibles qui peuvent soit classer les régions actives, soit prédire des valeurs d’accessibilité graduées. Surtout, CREsted ne s’arrête pas à la prédiction. Il peut zoomer pour identifier quelles lettres individuelles de l’ADN importent le plus pour un type cellulaire donné, regrouper les motifs récurrents et associer ces motifs aux protéines régulatrices probables à l’aide de bases de données existantes et de données d’expression génique. Enfin, il inclut des outils de conception qui « évoluent » itérativement des séquences d’ADN synthétiques afin que le modèle prévoie une forte activité dans un type cellulaire choisi et peu d’activité ailleurs.
Tester la boîte à outils dans le cerveau, le sang, le cancer et le poisson
Les auteurs illustrent CREsted sur plusieurs ensembles de données riches. Dans le cortex moteur de la souris, leurs modèles prédisent avec une grande précision quelles régions d’ADN sont ouvertes dans différents types de neurones et de cellules de soutien, surpassant un cadre général de référence. En mettant en évidence des motifs de séquence clés, CREsted retrouve des protéines régulatrices connues pour des classes neuronales spécifiques et peut même expliquer comment un changement d’une seule lettre dans un motif peut basculer l’activité entre sous-types neuronaux. Chez les cellules sanguines humaines, un modèle connexe redécouvre de nombreux sites de liaison déjà testés dans des enhancers immunitaires classiques et s’aligne bien avec des expériences indépendantes de liaison protéine-ADN, ce qui confirme que les motifs appris ont une signification biologique.
CREsted explore aussi des questions plus appliquées. En cancérologie, il compare un état cellulaire « de type mésenchymateux » qui apparaît à la fois dans le mélanome et le glioblastome, en utilisant des modèles entraînés sur des lignées cellulaires et sur des échantillons tumoraux de patients. Les motifs d’enhancers montrent des thèmes partagés mais aussi des différences importantes, comme des motifs spécifiques présents uniquement dans les tumeurs. Dans un autre test, les auteurs se demandent si des modèles « foundation » spécialisés, entraînés sur d’immenses jeux de données génomiques, surpassent réellement des modèles plus petits, focalisés sur une tâche. Après un ajustement fin attentif, ces grands modèles peinent encore à atteindre la résolution spécifique aux types cellulaires de l’architecture de CREsted, ce qui suggère que l’entraînement dédié sur des données unicellulaires de haute qualité demeure crucial.
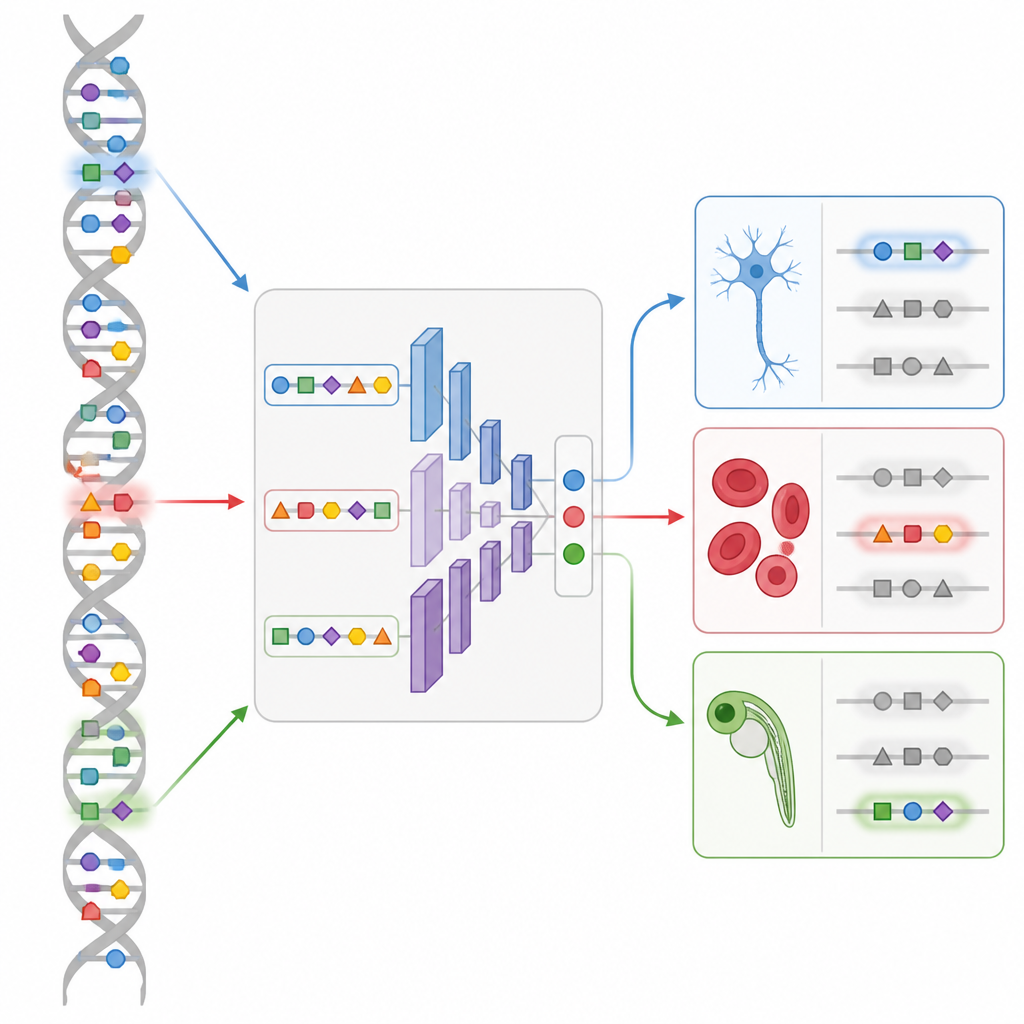
Concevoir de nouveaux interrupteurs dans un embryon vivant
La démonstration la plus frappante vient du développement du poisson zèbre. En utilisant une carte unicellulaire de l’accessibilité de l’ADN à travers de nombreux stades embryonnaires, l’équipe entraîne un modèle CREsted appelé DeepZebrafish. Ils laissent ensuite le module de conception générer des enhancers entièrement synthétiques prédits pour s’activer uniquement dans le muscle cardiaque, uniquement dans le muscle corporel, uniquement dans l’endothélium vasculaire, ou dans des combinaisons contrôlées cœur–muscle. Lorsque ces séquences artificielles sont placées devant un gène rapporteur fluorescent et injectées dans des œufs de poisson, beaucoup s’allument exactement dans les tissus visés. L’analyse de leurs séquences révèle des motifs reconnaissables pour des régulateurs développementaux majeurs, confirmant que le modèle a capturé une « grammaire » signifiative plutôt que des bizarreries aléatoires.
Ce que cela signifie pour la compréhension et l’ingénierie des génomes
Pour un non-spécialiste, CREsted peut être vu comme un microscope pour la couche régulatrice du génome et comme un outil de conception pour de nouvelles pièces génétiques. Il traduit des segments d’ADN en prédictions sur les types cellulaires susceptibles de les utiliser, indique les lettres et motifs clés qui gouvernent ce comportement et peut proposer de nouvelles séquences devant se comporter comme souhaité. En travaillant à travers le cerveau, le sang, le cancer et des animaux en développement complets, l’étude montre qu’une approche unifiée peut révéler à la fois des règles partagées et des règles spécifiques aux types cellulaires du contrôle des gènes. À long terme, de tels outils pourraient aider les chercheurs à construire des marqueurs génétiques plus précis, améliorer les modèles de maladies et mieux comprendre comment de petites modifications de l’ADN peuvent se répercuter à travers cellules et tissus.
Citation: Kempynck, N., De Winter, S., Blaauw, C.H. et al. CREsted: modeling genomic and synthetic cell-type-specific enhancers across tissues and species. Nat Methods 23, 946–959 (2026). https://doi.org/10.1038/s41592-026-03057-2
Mots-clés: modélisation d’enhancers, génomique et apprentissage profond, chromatine unicellulaire, éléments régulateurs cis, enhancers synthétiques