Clear Sky Science · pl
CREsted: modelowanie genomowych i syntetycznych wzmacniaczy specyficznych dla typów komórek w tkankach i gatunkach
Dlaczego drobne przełączniki w DNA mają znaczenie
Każda komórka w twoim ciele nosi te same DNA, a mimo to komórki mózgowe, krwi i mięśni zachowują się zupełnie inaczej. Istotną przyczyną jest ukryta warstwa kontroli złożona z krótkich przełączników DNA zwanych wzmacniaczami, które decydują, kiedy i gdzie geny się włączają. Artykuł prezentuje CREsted, pakiet programów wykorzystujący nowoczesną sztuczną inteligencję do odczytywania tych przełączników bezpośrednio z sekwencji DNA, a nawet projektowania nowych. Praca pokazuje, jak możemy przejść od prostego katalogowania części genetycznych do aktywnego rozumienia i inżynierii tych elementów w różnych tkankach i gatunkach.
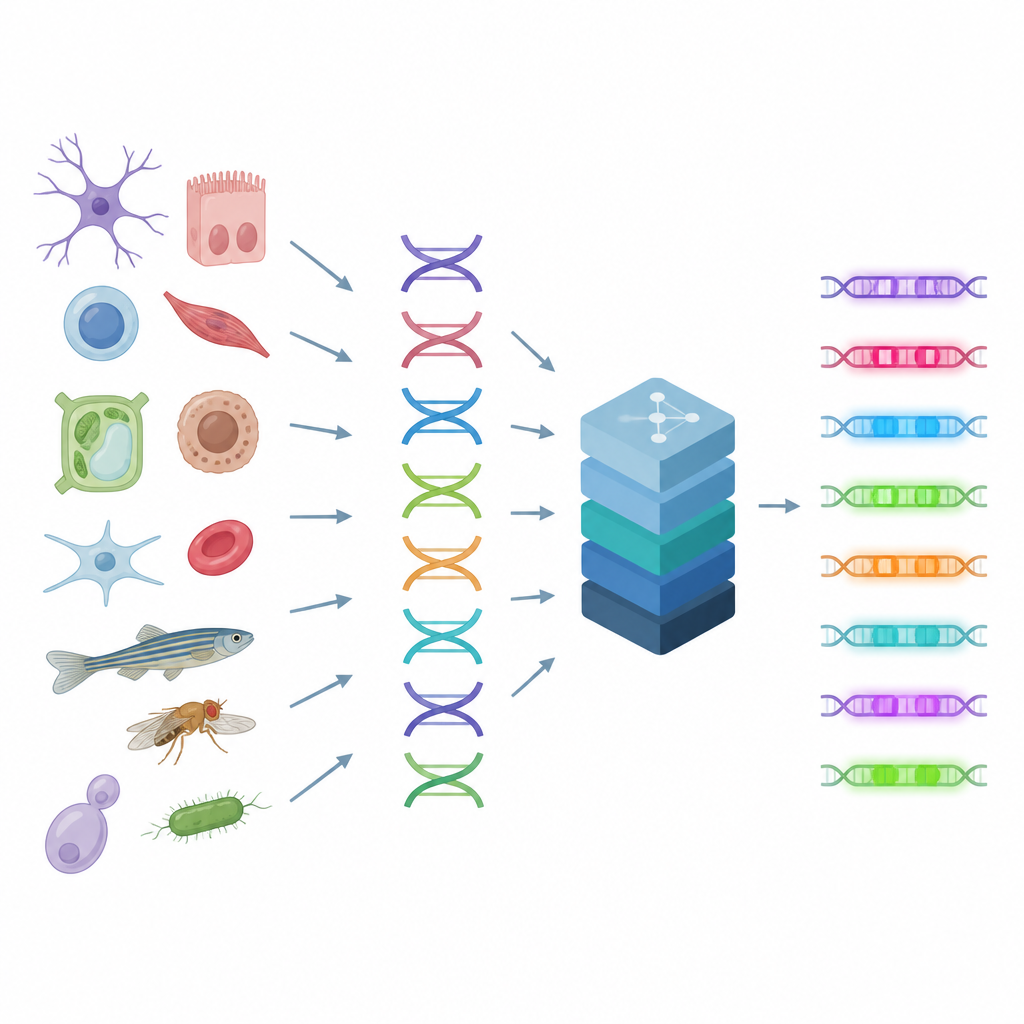
Odczytywanie przełączników kontroli komórki
Wzmacniacze działają jak pokrętła na konsole mikserskiej, łącząc sygnały od wielu białek, by precyzyjnie dostroić aktywność genów w każdym typie komórki. Ponieważ różne wzorce DNA mogą prowadzić do podobnych efektów, zasady rządzące wzmacniaczami są złożone i trudne do odgadnięcia gołym okiem. Autorzy bazują na technice mierzącej, które fragmenty DNA są otwarte lub zamknięte w tysiącach pojedynczych komórek — wskazówce, która ujawnia, gdzie w genomie znajdują się aktywne wzmacniacze. CREsted łączy te pomiary z odpowiadającymi im sekwencjami DNA i trenuje modele głębokiego uczenia, by przewidywać, jak dostępny będzie każdy region w wielu typach komórek jednocześnie. To przekształca surową sekwencję w mapę aktywności regulacyjnej.
Zestaw narzędzi od danych do wglądu
CREsted to więcej niż pojedynczy model — to kompleksowy pipeline. Najpierw czyści i przekształca dane pojedynczych komórek w formę, która zmniejsza techniczne różnice między typami komórek. Następnie trenuje elastyczne sieci neuronowe, które mogą albo klasyfikować aktywne regiony, albo przewidywać stopniowane wartości dostępności. Co ważne, CREsted nie ogranicza się do przewidywań. Potrafi zagłębić się, by zidentyfikować, które indywidualne nukleotydy DNA mają największe znaczenie dla danego typu komórki, grupować powtarzające się wzorce i dopasowywać je do prawdopodobnych białek regulatorowych przy użyciu istniejących baz danych i danych ekspresji genów. Wreszcie zawiera narzędzia projektowe, które iteracyjnie „ewoluują” syntetyczne sekwencje DNA tak, aby model przewidywał silną aktywność w wybranym typie komórki i niską aktywność w innych.
Testowanie narzędzi w mózgu, krwi, raku i rybach
Autorzy prezentują CREsted na kilku bogatych zestawach danych. W korze ruchowej myszy ich modele z wysoką dokładnością przewidują, które regiony DNA są otwarte w różnych typach neuronów i komórek wspierających, przewyższając czołowe ogólne ramy modelowe. Poprzez wyróżnianie kluczowych wzorców sekwencji, CREsted odtwarza znane białka regulatorowe dla konkretnych klas neuronów i potrafi nawet wyjaśnić, jak pojedyncza zmiana nukleotydu w motywie może przełączyć aktywność między podtypami neuronów. W ludzkich komórkach krwi pokrewny model ponownie odnajduje wiele wcześniej testowanych miejsc wiązania w klasycznych wzmacniaczach układu odpornościowego i dobrze zgadza się z niezależnymi eksperymentami wiązania białek, co potwierdza, że wyuczone wzorce sekwencji mają biologiczne znaczenie.
CREsted bada także bardziej zastosowane pytania. W nowotworach porównuje stan komórkowy „przypominający mezenchymalny”, który pojawia się zarówno w czerniaku, jak i glejakach, używając modeli trenowanych na liniach komórkowych oraz na próbkach guzów od pacjentów. Wzorce wzmacniaczy pokazują wspólne motywy, ale też istotne różnice, jak motywy obecne tylko w guzach. W innym teście autorzy pytają, czy wyspecjalizowane „modele fundamentowe” trenowane na ogromnych zestawach genomowych rzeczywiście przewyższają mniejsze modele ukierunkowane na zadanie. Po starannym dostrojeniu te duże modele nadal mają trudności z osiągnięciem rozdzielczości specyficznej dla typów komórek, jaką daje architektura CREsted, co sugeruje, że dedykowane szkolenie na wysokiej jakości danych pojedynczych komórek pozostaje kluczowe.
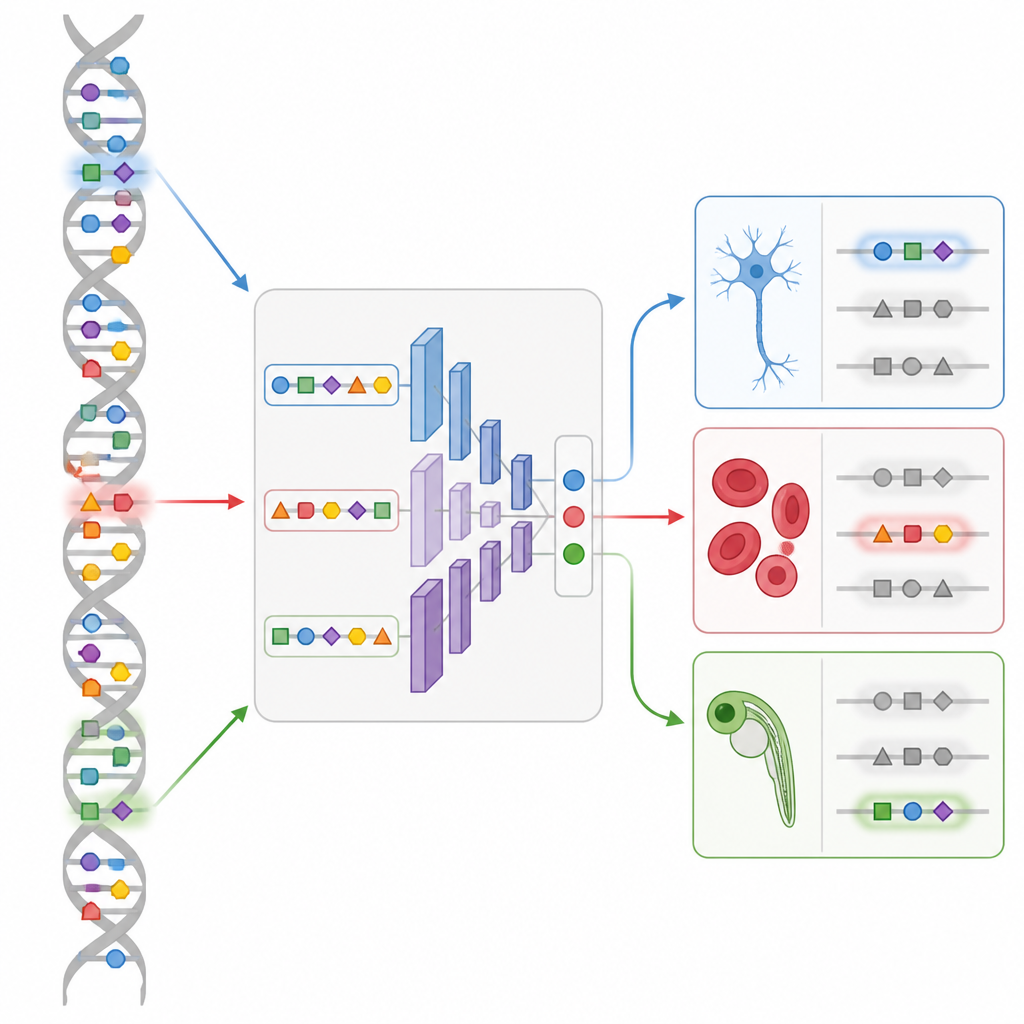
Projektowanie nowych przełączników w żywym embrionie
Najbardziej uderzający pokaz pochodzi z rozwoju zebrafish (danio pręgowany). Wykorzystując mapę dostępności DNA w pojedynczych komórkach przez wiele etapów rozwoju zarodka, zespół trenuje model CREsted nazwany DeepZebrafish. Następnie moduł projektowy generuje całkowicie syntetyczne wzmacniacze przewidywane jako aktywne wyłącznie w mięśniu sercowym, wyłącznie w mięśniach ciała, wyłącznie w śródbłonku naczyń krwionośnych, lub w kontrolowanych kombinacjach mięśnia sercowego i szkieletowego. Gdy te sztuczne sekwencje umieszczono przed fluorescencyjnym reporterem i wstrzyknięto do jaj ryb, wiele z nich zapala się dokładnie w zamierzonych tkankach. Analiza ich sekwencji ujawnia rozpoznawalne wzorce dla głównych regulatorów rozwoju, potwierdzając, że model uchwycił sensowną „gramatykę”, a nie przypadkowe cechy.
Co to oznacza dla zrozumienia i inżynierii genomów
Dla osoby niebędącej specjalistą CREsted można traktować jak mikroskop dla warstwy regulacyjnej genomu i narzędzie do tworzenia nowych części genetycznych. Tłumaczy fragmenty DNA na przewidywania, które typy komórek będą z nich korzystać, wskazuje kluczowe nukleotydy i motywy napędzające to zachowanie oraz może sugerować nowe sekwencje, które powinny zachowywać się w pożądany sposób. Pracując w mózgu, krwi, nowotworach i całych rozwijających się organizmach, badanie pokazuje, że zunifikowane podejście może ujawnić zarówno wspólne, jak i specyficzne dla typów komórek zasady kontroli genów. W dłuższej perspektywie takie narzędzia mogą pomóc badaczom w tworzeniu precyzyjniejszych markerów genetycznych, ulepszaniu modeli chorób i lepszym rozumieniu, jak niewielkie zmiany w DNA mogą rozchodzić się przez komórki i tkanki.
Cytowanie: Kempynck, N., De Winter, S., Blaauw, C.H. et al. CREsted: modeling genomic and synthetic cell-type-specific enhancers across tissues and species. Nat Methods 23, 946–959 (2026). https://doi.org/10.1038/s41592-026-03057-2
Słowa kluczowe: modelowanie wzmacniaczy, genomika głębokiego uczenia, chromatyna pojedynczych komórek, cis elementy regulacyjne, syntetyczne wzmacniacze