Clear Sky Science · de
CREsted: Modellierung genomischer und synthetischer zelltypspezifischer Enhancer über Gewebe und Arten hinweg
Warum winzige Schalter in der DNA wichtig sind
Jede Zelle in Ihrem Körper trägt dieselbe DNA, dennoch verhalten sich Gehirn‑, Blut‑ und Muskelzellen sehr unterschiedlich. Ein wesentlicher Grund ist eine verborgene Kontrollebene aus kurzen DNA‑Schaltern, den Enhancern, die entscheiden, wann und wo Gene angeschaltet werden. Dieser Artikel stellt CREsted vor, ein Software‑Toolkit, das moderne künstliche Intelligenz nutzt, um diese Schalter direkt aus der DNA zu lesen und sogar neue zu entwerfen. Die Arbeit zeigt, wie wir vom bloßen Auflisten genetischer Bausteine zu einem aktiven Verständnis und zur gezielten Gestaltung über Gewebe und Arten hinweg gelangen können.
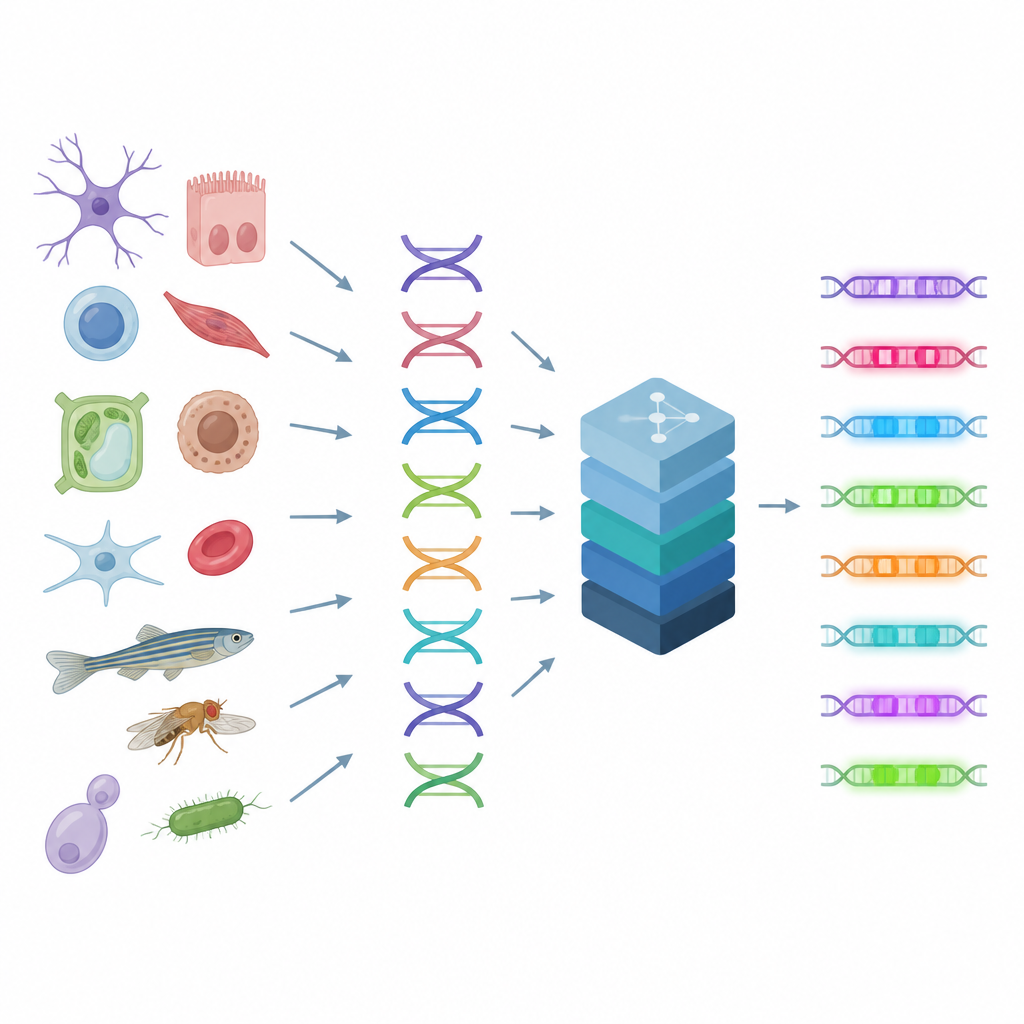
Die Kontrollschalter der Zelle lesen
Enhancer wirken wie Regler an einem Mischpult: Sie kombinieren Signale vieler Proteine, um die Genaktivität in jedem Zelltyp fein zu steuern. Da mehrere DNA‑Muster zu ähnlichen Ergebnissen führen können, sind die Regeln hinter Enhancern komplex und schwer visuell zu erschließen. Die Autoren bauen auf einer Methode auf, die misst, wie offen oder geschlossen jeder DNA‑Abschnitt in tausenden Einzelzellen ist – ein Hinweis darauf, wo aktive Enhancer im Genom liegen. CREsted nimmt diese Messungen, verknüpft sie mit den zugrunde liegenden DNA‑Sequenzen und trainiert Deep‑Learning‑Modelle, die vorhersagen, wie zugänglich jede Region in vielen Zelltypen zugleich sein wird. So wird rohe Sequenz in eine Karte regulatorischer Aktivität verwandelt.
Ein Toolkit von Daten bis Erkenntnis
CREsted ist mehr als ein einzelnes Modell: es ist eine End‑to‑End‑Pipeline. Zuerst bereinigt und transformiert sie Einzelzell‑Daten in eine Form, die technische Verzerrungen zwischen Zelltypen reduziert. Dann trainiert sie flexible neuronale Netze, die entweder aktive Regionen klassifizieren oder abgestufte Zugänglichkeitswerte vorhersagen können. Wichtig ist: CREsted hört nicht bei der Vorhersage auf. Es kann hineinzoomen, um herauszufinden, welche einzelnen DNA‑Basen für einen bestimmten Zelltyp am wichtigsten sind, wiederkehrende Muster clustern und diese Muster anhand bestehender Datenbanken und Genexpressionsdaten mit wahrscheinlichen regulatorischen Proteinen abgleichen. Schließlich enthält das Toolkit Design‑Werkzeuge, die synthetische DNA‑Sequenzen iterativ „evolvieren“ lassen, sodass das Modell starke Aktivität in einem gewählten Zelltyp und geringe Aktivität anderswo vorhersagt.
Testen des Toolkits in Gehirn, Blut, Krebs und Fisch
Die Autoren demonstrieren CREsted an mehreren umfangreichen Datensätzen. Im Maus‑Motorcortex sagen ihre Modelle mit hoher Genauigkeit voraus, welche DNA‑Regionen in verschiedenen Neuronentypen und Stützzellen offen sind, und übertreffen dabei ein führendes allgemeines Framework. Durch das Hervorheben wichtiger Sequenzmuster rekonstruiert CREsted bekannte Regulationsproteine für spezifische Neuronenklassen und kann sogar erklären, wie eine einzelne Basenänderung in einem Motiv die Aktivität zwischen Neuron‑Subtypen umschalten kann. In menschlichen Blutzellen entdeckt ein verwandtes Modell viele zuvor geprüfte Bindungsstellen in klassischen Immun‑Enhancern wieder und stimmt gut mit unabhängigen Proteinbindungs‑Experimenten überein, was dafür spricht, dass die gelernten Sequenzmuster biologisch bedeutsam sind.
CREsted untersucht auch praxisnähere Fragestellungen. In der Krebsforschung vergleichen die Autoren einen „mesenchymal‑ähnlichen“ Zellzustand, der sowohl in Melanom als auch in Glioblastom auftritt, mithilfe von Modellen, die auf Zelllinien und Patientenproben trainiert wurden. Die Enhancer‑Muster zeigen gemeinsame Themen, aber auch wichtige Unterschiede, etwa spezifische Motive, die nur in Tumoren vorkommen. In einem weiteren Test fragen die Autoren, ob spezialisierte „Foundation‑Modelle“, die auf riesigen Genomdatenmengen trainiert wurden, kleineren, aufgabenfokussierten Modellen wirklich überlegen sind. Nach sorgfältigem Feintuning hatten diese großen Modelle weiterhin Schwierigkeiten, die zelltypspezifische Auflösung von CREsted’s eigener Architektur zu erreichen, was nahelegt, dass dediziertes Training auf hochwertigen Einzelzell‑Daten entscheidend bleibt.
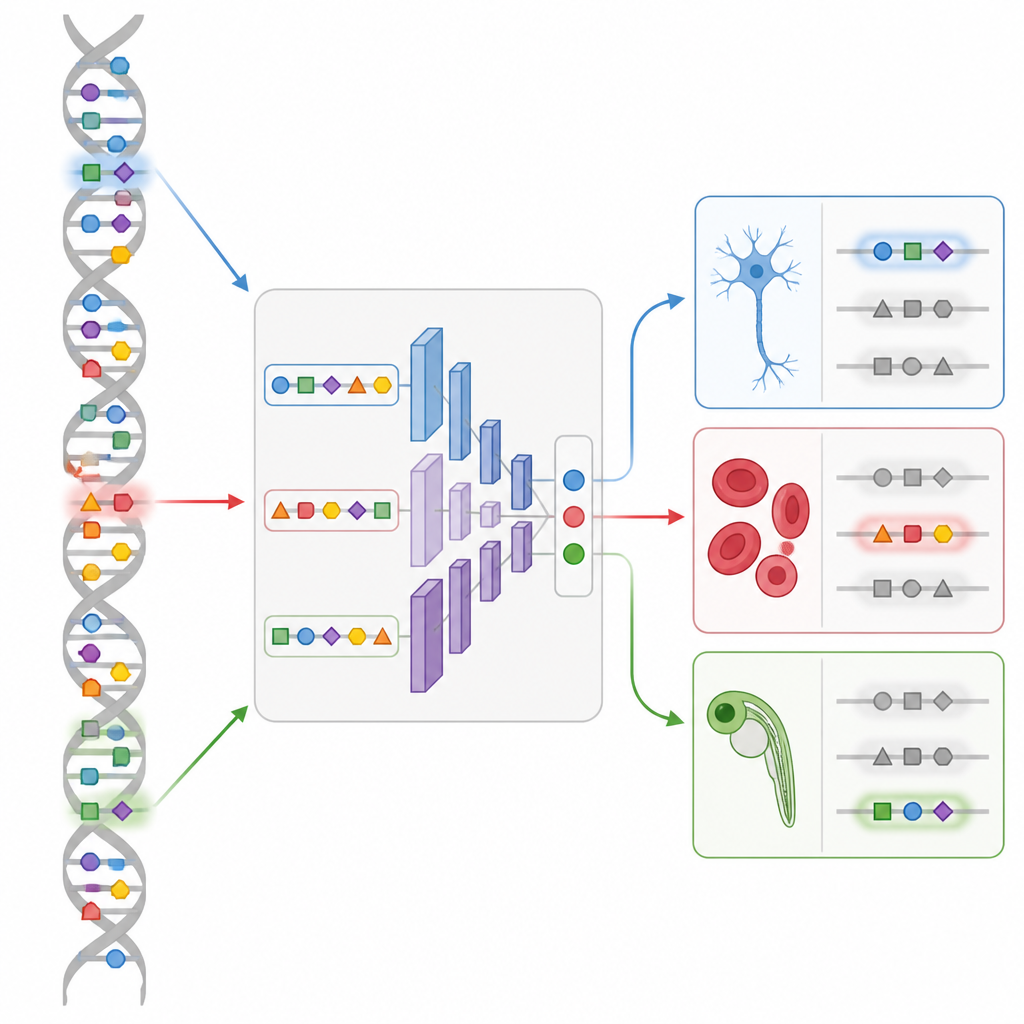
Neue Schalter in einem lebenden Embryo entwerfen
Die eindrücklichste Demonstration stammt aus der Zebrafisch‑Entwicklung. Mit einer Einzelzellkarte der DNA‑Zugänglichkeit über viele Embryonalstadien trainierte das Team ein CREsted‑Modell namens DeepZebrafish. Anschließend ließ das Design‑Modul vollständig synthetische Enhancer erzeugen, die laut Vorhersage nur im Herzmuskel, nur im Körpermuskel, nur im Gefäßendothel oder in kontrollierten Kombinationen von Herz und Muskel aktiv sein sollten. Wenn diese künstlichen Sequenzen vor einen fluoreszenten Reporter gesetzt und in Fisch‑Eier injiziert wurden, leuchteten viele genau in den vorgesehenen Geweben auf. Die Analyse ihrer Sequenzen zeigt erkennbare Muster für wichtige Entwicklungsregulatoren und bestätigt, dass das Modell eine sinnvolle „Grammatik“ erfasst hat und nicht bloß zufällige Besonderheiten.
Was das für das Verständnis und die Gestaltung von Genomen bedeutet
Für Nicht‑Spezialisten lässt sich CREsted als Mikroskop für die regulatorische Ebene des Genoms und als Entwurfswerkzeug für neue genetische Bausteine betrachten. Es übersetzt DNA‑Abschnitte in Vorhersagen darüber, welche Zelltypen sie nutzen werden, weist auf die entscheidenden Basen und Motive hin, die dieses Verhalten antreiben, und kann neue Sequenzen vorschlagen, die sich wie gewünscht verhalten sollten. Indem es über Gehirn, Blut, Krebs und ganze sich entwickelnde Organismen hinweg arbeitet, zeigt die Studie, dass ein einheitlicher Ansatz sowohl gemeinsame als auch zelltypspezifische Regeln der Genregulation offenlegen kann. Langfristig könnten solche Werkzeuge Forschern helfen, präzisere genetische Marker zu entwickeln, Krankheitsmodelle zu verbessern und besser zu verstehen, wie kleine Veränderungen in der DNA Wellen durch Zellen und Gewebe schlagen können.
Zitation: Kempynck, N., De Winter, S., Blaauw, C.H. et al. CREsted: modeling genomic and synthetic cell-type-specific enhancers across tissues and species. Nat Methods 23, 946–959 (2026). https://doi.org/10.1038/s41592-026-03057-2
Schlüsselwörter: Enhancer‑Modellierung, Deep‑Learning‑Genomik, Einzelzell‑Chromatin, cis‑regulatorische Elemente, synthetische Enhancer