Clear Sky Science · nl
CREsted: modellering van genomische en synthetische cel-type-specifieke enhancers over weefsels en soorten
Waarom kleine schakelaars in DNA ertoe doen
Elke cel in je lichaam draagt hetzelfde DNA, maar hersencellen, bloedcellen en spiercellen gedragen zich sterk verschillend. Een belangrijke reden is een verborgen regellaag van korte DNA-schakelaars, enhancers genoemd, die bepalen wanneer en waar genen worden aangezet. Dit artikel presenteert CREsted, een softwaretoolkit die moderne kunstmatige intelligentie gebruikt om deze schakelaars rechtstreeks uit DNA te lezen en zelfs nieuwe te ontwerpen. Het werk toont hoe we kunnen verschuiven van het eenvoudig opsommen van genetische onderdelen naar het actief begrijpen en ontwerpen ervan over weefsels en soorten heen.
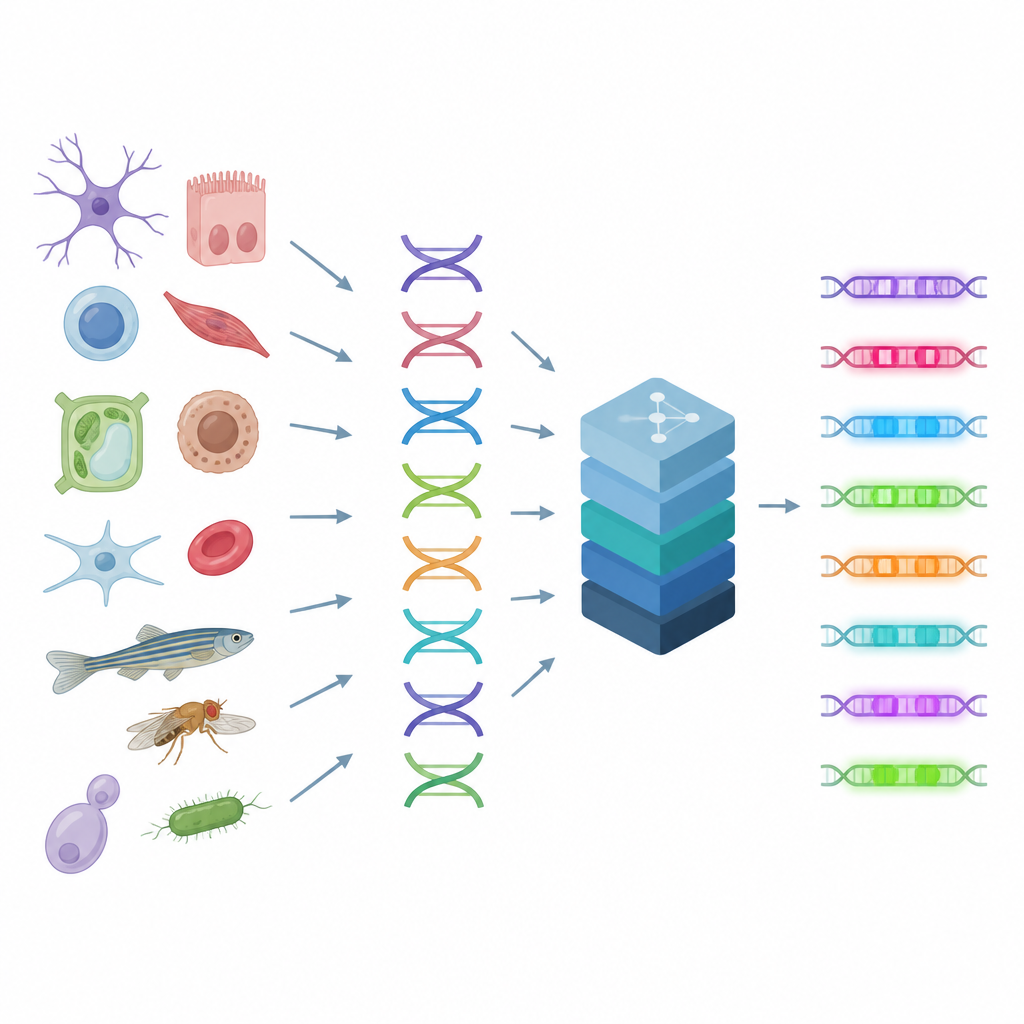
De controle-schakelaars van de cel lezen
Enhancers werken als knoppen op een mengpaneel, waarbij signalen van veel eiwitten worden gecombineerd om de genactiviteit in elk celtype fijn af te stemmen. Omdat meerdere DNA-patronen vergelijkbare uitkomsten kunnen geven, zijn de regels achter enhancers complex en moeilijk visueel te doorgronden. De auteurs bouwen voort op een techniek die meet hoe open of gesloten elk stuk DNA is in duizenden individuele cellen, een aanwijzing die onthult waar actieve enhancers in het genoom zitten. CREsted neemt deze metingen, koppelt ze aan de onderliggende DNA-sequenties en traint deep-learningmodellen om te voorspellen hoe toegankelijk elk gebied zal zijn in veel celtypen tegelijk. Dit verandert ruwe sequentie in een kaart van regulerende activiteit.
Een toolkit van data naar inzicht
CREsted is meer dan één enkel model: het is een end-to-end pijplijn. Eerst reinigt en herschikt het single-cellgegevens tot een vorm die technische bias tussen celtypen vermindert. Vervolgens traint het flexibele neurale netwerken die ofwel actieve gebieden classificeren of graduele toegankelijkheidswaarden voorspellen. Belangrijk is dat CREsted niet stopt bij voorspelling. Het kan inzoomen op welke individuele DNA-letters het belangrijkste zijn voor een bepaald celtype, terugkerende patronen clusteren en deze patronen koppelen aan waarschijnlijke regulerende eiwitten met behulp van bestaande databases en genexpressiegegevens. Ten slotte bevat het ontwerp-tools die iteratief synthetische DNA-sequenties "evolueren" zodat het model sterke activiteit voorspelt in één gekozen celtype en weinig activiteit elders.
De toolkit testen in hersenen, bloed, kanker en vis
De auteurs tonen CREsted op meerdere rijke datasets. In de muismotorische cortex voorspellen hun modellen met hoge nauwkeurigheid welke DNA-regio’s open zijn in verschillende neuron- en ondersteunende celtypen en overtreffen ze een toonaangevend algemeen kader. Door sleutel-sequentiepatronen te benadrukken, herkent CREsted bekende regulator-eiwitten voor specifieke neuronklassen en kan het zelfs uitleggen hoe een enkele letterverandering in een motief activiteit tussen neuron-subtypen kan omzetten. In menselijke bloedcellen herontdekt een verwant model veel eerder geteste bindingsplaatsen in klassieke immuun-enhancers en sluit het goed aan bij onafhankelijke eiwitbindingsexperimenten, wat ondersteunt dat de aangeleerde sequentiepatronen biologisch betekenisvol zijn.
CREsted onderzoekt ook meer toegepaste vragen. Bij kanker vergelijkt het een "mesenchymaal-achtig" celtoestand die verschijnt in zowel melanoom als glioblastoom, met modellen getraind op cellijnen en op patiënttumor-monsters. De enhancerpatronen tonen gedeelde thema’s maar ook belangrijke verschillen, zoals specifieke motieven die alleen in tumoren aanwezig zijn. In een andere test vragen de auteurs of gespecialiseerde "foundation"-modellen, getraind op enorme genomische datasets, echt beter presteren dan kleinere, taakgerichte modellen. Na zorgvuldige fine-tuning hebben deze grote modellen nog steeds moeite om de celtype-specifieke resolutie van CREsted’s eigen architectuur te evenaren, wat suggereert dat toegewijde training op hoogwaardige single-cellgegevens cruciaal blijft.
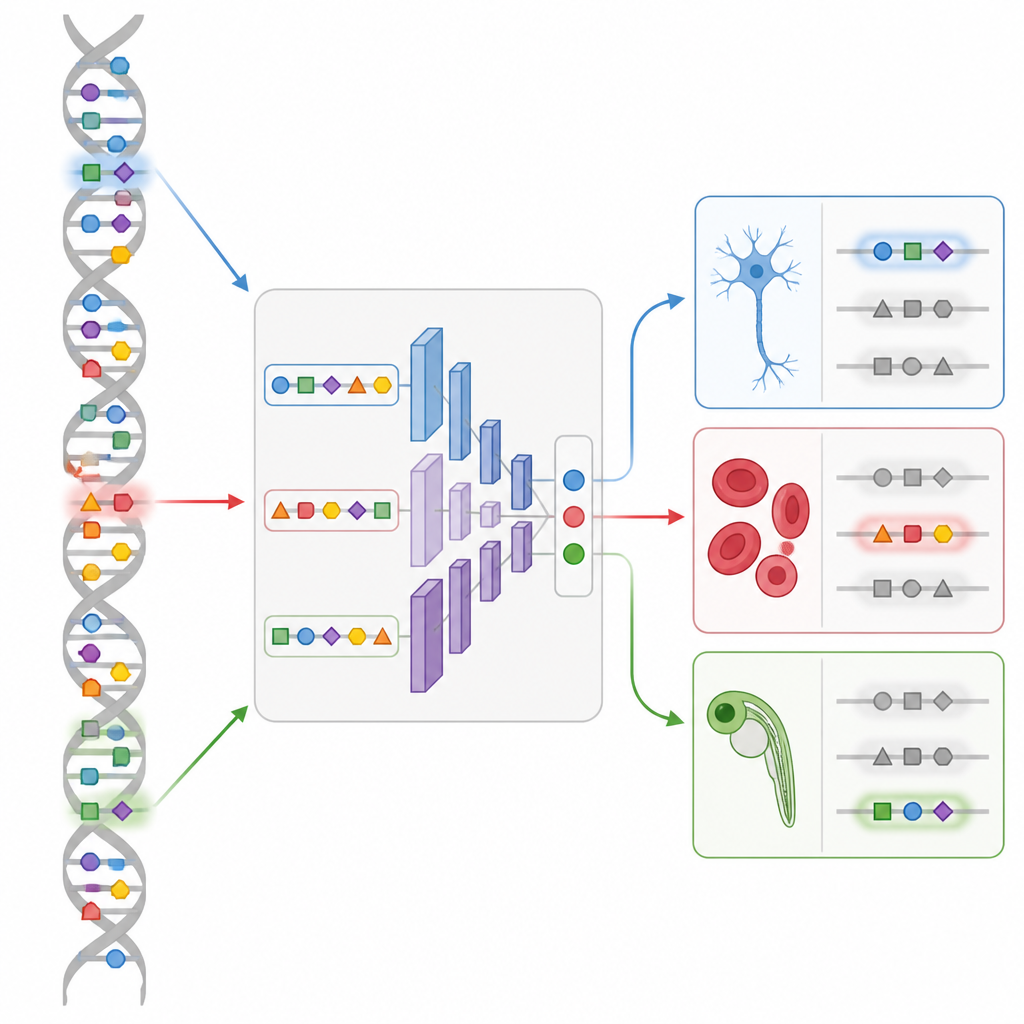
Nieuwe schakelaars ontwerpen in een levend embryo
De meest opvallende demonstratie komt uit de ontwikkeling van zebravis. Met een single-cell-kaart van DNA-toegankelijkheid over veel embryonale stadia traint het team een CREsted-model genaamd DeepZebrafish. Vervolgens laat het ontwerpmodule volledig synthetische enhancers genereren die naar verwachting alleen in hartspier, alleen in lichaamsspier, alleen in het bloedvatendotheel of in gecontroleerde combinaties van hart en spier aan zullen staan. Wanneer deze kunstmatige sequenties voor een fluorescerende reporter worden geplaatst en in vis-eieren worden geïnjecteerd, lichten veel ervan precies op in de bedoelde weefsels. Analyse van hun sequenties onthult herkenbare patronen voor belangrijke ontwikkelingsregulatoren, wat bevestigt dat het model zinvolle "grammatica" heeft vastgelegd in plaats van willekeurige eigenaardigheden.
Wat dit betekent voor het begrijpen en ontwerpen van genomen
Voor niet-specialisten kan CREsted worden gezien als een microscoop voor de regulerende laag van het genoom en als een ontwerptool voor nieuwe genetische onderdelen. Het vertaalt stukken DNA naar voorspellingen over welke celtypen ze zullen gebruiken, wijst op de sleutelletters en motieven die dat gedrag aansturen en kan nieuwe sequenties suggereren die zich op de gewenste manier zouden moeten gedragen. Door te werken over hersenen, bloed, kanker en hele zich ontwikkelende dieren, laat de studie zien dat een eendrachtige aanpak zowel gedeelde als celtype-specifieke regels van genregulatie kan onthullen. Op de lange termijn kunnen dergelijke tools onderzoekers helpen meer precieze genetische markers te bouwen, ziekte modellen te verbeteren en beter te begrijpen hoe kleine veranderingen in DNA zich door cellen en weefsels kunnen voortplanten.
Bronvermelding: Kempynck, N., De Winter, S., Blaauw, C.H. et al. CREsted: modeling genomic and synthetic cell-type-specific enhancers across tissues and species. Nat Methods 23, 946–959 (2026). https://doi.org/10.1038/s41592-026-03057-2
Trefwoorden: modellering van enhancers, deep learning genomica, single-cell chromatine, cis-regulerende elementen, synthetische enhancers