Clear Sky Science · sv
Kemisk fångst av diazo‑metaboliter avslöjar biosyntetisk hydrazon‑oxidation
Varför instabila molekyler spelar roll för oss
Kemister har länge vetat att några av de mest potenta läkemedlen och industriella reagenserna också är de mest sköra. De bryts ner så snabbt att det kan vara som att försöka fånga tvålliknande bubblor i en storm när man letar efter dem i naturen. Denna studie tar sig an en sådan familj av flyktiga molekyler, kallade diazo‑föreningar, som produceras av mikrober och både kan skada celler och driva användbara kemiska reaktioner. Genom att uppfinna ett sätt att ”fånga” dessa instabila molekyler så snart de bildas, avslöjar forskarna ny kemi i en mänsklig lungpatogen och identifierar ett enzym som kan bli ett grönt verktyg för framställning av värdefulla reagenser.
Dolda vapen från små mikrober
Mikroorganismer är mikroskopiska kemiska fabriker. Bland de många föreningar de producerar finns naturliga produkter som innehåller diazo‑grupper, vilka bär ett par kväveatomer redo att slitas isär och frigöra energi. Denna reaktivitet gör att de kan attackera biologiska mål, vilket ger antibiotisk och anticanceraktivitet, och det gör dem också eftertraktade som reagenser i syntetiska kemilabb. Ändå är endast ett fåtal dussin naturliga diazo‑föreningar kända. Gruppens genomgång av genetiska data avslöjade hundratals mikrobiella genkluster som ser ut att kunna producera diazo‑molekyler, utspridda i jordbakterier, marina mikrober och patogener. Diskrepansen mellan den genetiska potentialen och det lilla antalet kända föreningar antydde att många diazo‑molekyler förblir osedda, sannolikt eftersom de är för instabila för vanliga upptäcktsmetoder som förlitar sig på att isolera stabila, rikliga produkter.
Fånga flyktiga molekyler med ett kemiskt krok
För att lösa detta problem vände forskarna på den vanliga sökstrategin. I stället för att fråga om en mikrobs extrakt dödar cancerceller eller bakterier, frågade de om dess metaboliter delar en viss typ av kemisk reaktivitet. De designade en liten probermolekyl baserad på en spänd ringformad alkyne som reagerar selektivt och snabbt med diazo‑grupper och bildar en stabilare ring kallad pyrazol. När den blandas med mikrobiell odlingsvätska fungerar denna sond som en kemisk krok: om någon diazo‑förening finns där, hakar sonden i och omvandlar den till en tyngre, lättare upptäckt produkt. Genom att använda känslig masspektrometri och jämförande metabolomik jämförde teamet prover tagna omedelbart efter tillsats av sonden med prover inkuberade över natten. Signaler som ökade starkt över tid och visade det karaktäristiska dubbla toppmönstret för sondernas produkter pekade ut dolda diazo‑metaboliter.
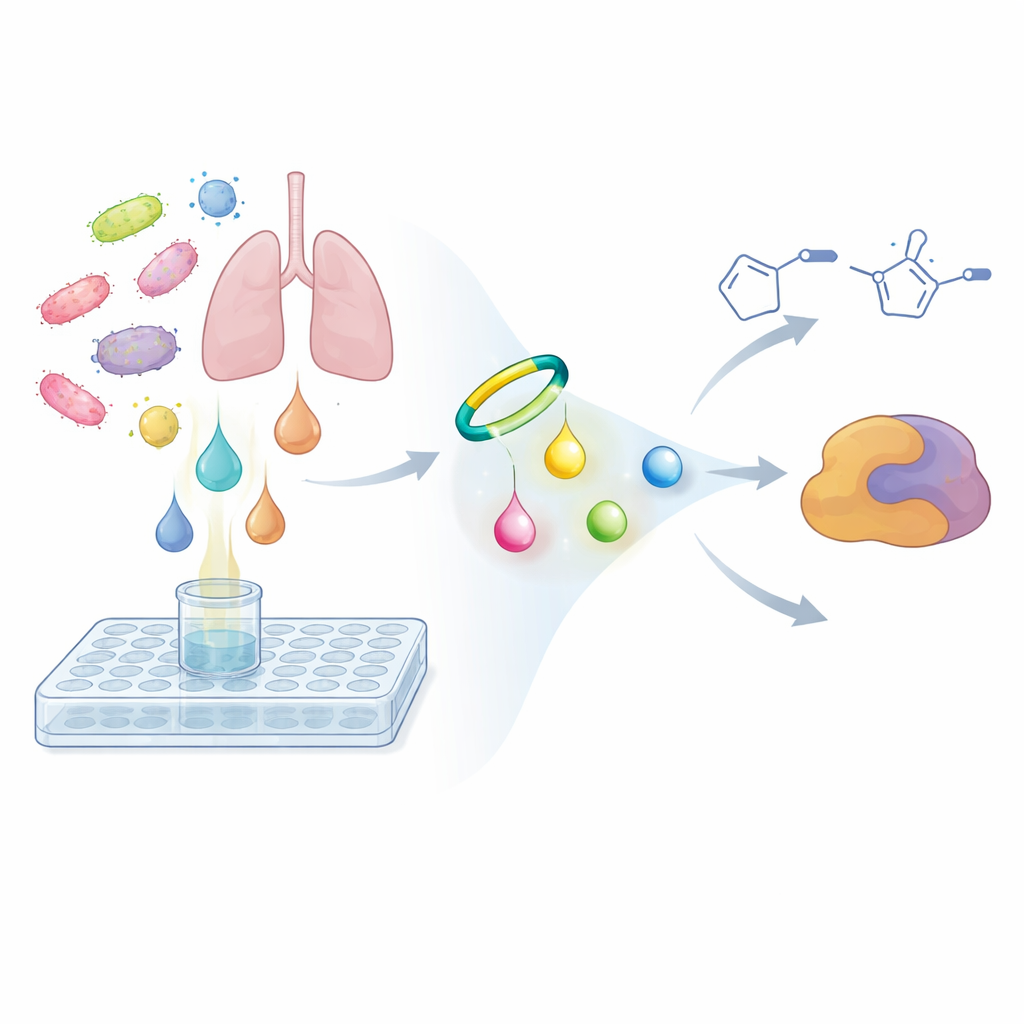
Nya reaktiva molekyler från en lungpatogen
Screening av genetiskt utvalda bakterier med detta sondbaserade arbetsflöde ledde teamet till lungpatogenen Nocardia ninae. I dess odlingsvätska observerade de två par av sond‑härledda produkter som endast framträdde efter inkubation, hade den förväntade kväverika sammansättningen och matchade beteendet för infångade diazo‑föreningar. Genom att subtrahera sondens kända formel och resonera kring de återstående atomerna drog de slutsatsen att de ursprungliga naturliga produkterna var två mycket enkla men tidigare osedda molekyler: 4‑diazo‑3‑oxobutansyra och diazoaceton. Dessa är små byggstenar jämfört med många naturliga produkter, men de är starkt reaktiva. Kontrollförsök visade att de omodifierade molekylerna i princip var osynliga för rutinanalys, medan de sondmärkta versionerna kunde detekteras vid koncentrationer så låga som några hundra delar per miljard, vilket understryker hur lätt sådana metaboliter kan ha missats.
Avslöjande av en ovanlig enzymväg
Att hitta molekylerna var bara halva historien; forskarna spårade sedan hur bakterien tillverkar dem. Genom att granska dess genom identifierade de ett genkluster, döpt dob, som liknade kända vägar för att bygga kväverika enheter kallade hydrazoner, men med extra enzymer som antydde nya steg. Genom att flytta detta genkluster till en annan bakterie och visa att värden började producera samma sondupptäckta produkter bekräftade de dess roll. Detaljerade biokemiska experiment avslöjade ett stegvis monteringsband: vanliga aminosyror omformas till ett hydrazon‑bärande mellanprodukt som förlängs av ett polyketidsyntas‑enzym för att bilda en liten hydrazonsyra. Ett andra enzym, ett metalloenzym kallat Dob3, utför sedan en sällsynt kemisk prestation: det oxiderar hydrazonet till en diazo‑grupp. Denna reaktion, kallad hydrazonoxidation, hade föreslagits tidigare men inte direkt påvisats i naturen.
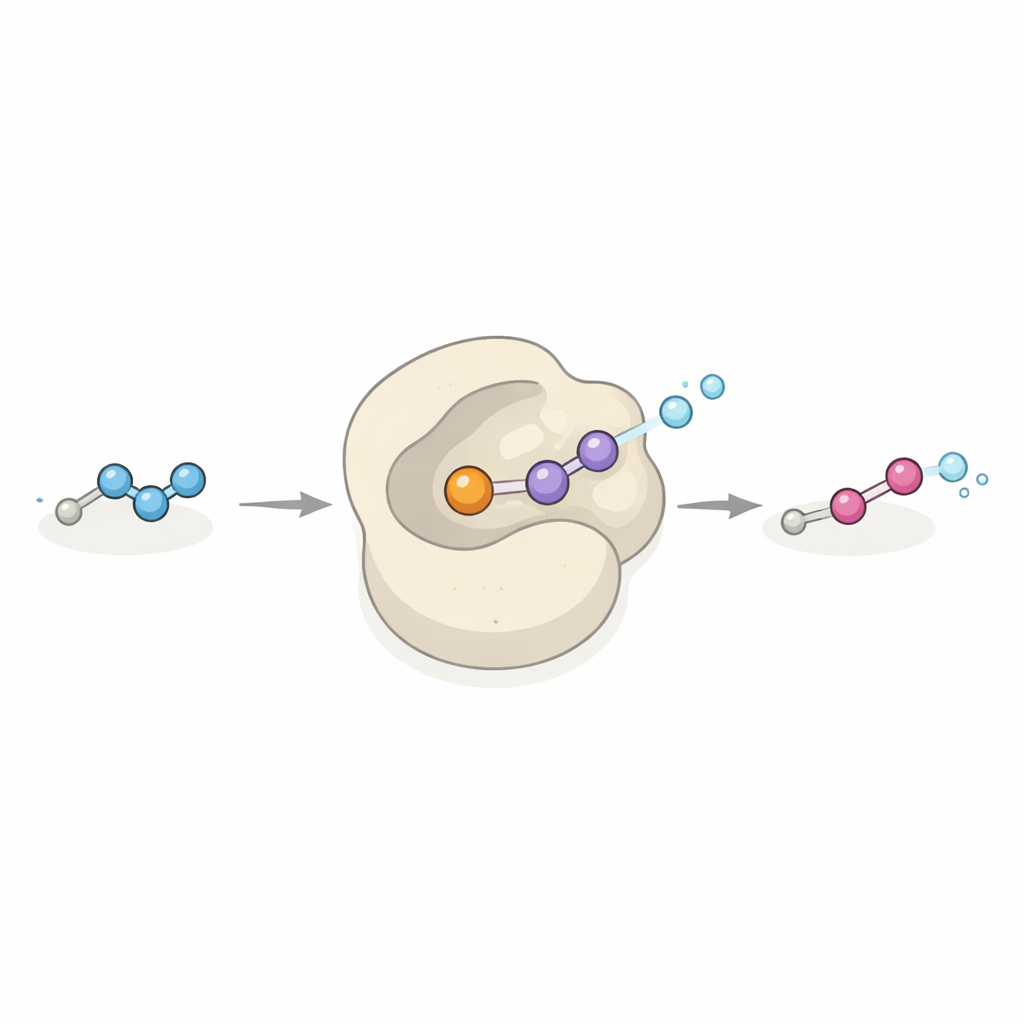
En ny typ av katalysator med industriell potential
Dob3 tillhör en familj proteiner som vanligtvis tillför syreatomer till kol‑väte eller kväve‑vätebindningar med hjälp av ett par järnatomer och syre från luften. Här utvidgar Dob3 den verktygslådan genom att förvandla ett relativt stabilt hydrazon till en högt energirik diazo‑grupp i ett sammankopplat två‑elektrons oxidationssteg. Enzymet accepterar en rad olika hydrazonsubstrat i provrörsexperiment och omvandlar dem till motsvarande diazo‑föreningar. Eftersom många diazo‑reagenser är hörnstenar i modern syntetisk kemi, särskilt för att skapa kol‑kol‑bindningar via så kallade karbenöverföringsreaktioner, skulle Dob3 kunna bli en mångsidig ”grön” katalysator för att framställa dessa reagenser från enkla förstadier under milda, miljövänliga villkor.
Vad detta arbete betyder framöver
För icke‑specialister är huvudbudskapet att kemin som sker inne i mikrober är både rikare och mer ömtålig än vi tidigare kunnat se. Genom att använda reaktivitet själv som en ledstjärna — fånga instabila molekyler i det ögonblick de bildas — avslöjar denna studie nya diazo‑föreningar i en mänsklig patogen och etablerar tydligt hydrazonoxidation som en naturlig väg till dessa reaktiva grupper. Upptäckten av Dob3, ett di‑järn‑enzym som utför denna svåra omvandling, öppnar dörrar för att konstruera mikrober som hållbart kan producera industriella diazo‑reagenser. Mer generellt antyder arbetet att många reaktiva naturliga produkter förblir en del av ett mikrobiellt ”mörkermateria” av kemi, väntande på att upptäckas med liknande smarta, reaktivitetsstyrda sökstrategier.
Citering: Pfeifer, K., Van Cura, D., Wu, K.J.Y. et al. Chemical capture of diazo metabolites reveals biosynthetic hydrazone oxidation. Nature 652, 517–525 (2026). https://doi.org/10.1038/s41586-025-10079-x
Nyckelord: diazo‑naturliga produkter, reaktivitetsbaserad screening, mikrobiella metaboliter, biokatalys, enzymupptäckt